Drinking-water treatment with ozone
1
1987
... 高级氧化技术(AOPs)在处理一些难降解有机物方面表现出效果好、反应彻底、环境友好等特点,具有广阔的应用前景.传统的AOPs指的是能够产生·OH的氧化过程,是由W. H. Glaze 〔1〕在1987年提出.随着技术的发展,将以硫酸根自由基(SO4·-)为主要活性基团氧化降解有机物的技术也归为AOPs.该技术主要是通过活化过硫酸盐产生SO4·-.过硫酸盐(PS,E0=+2.01 V)包括过一硫酸盐(PMS,HSO5-)和过二硫酸盐(PDS,S2O82-),其具有O—O键结构,常温条件下比较稳定,但对污染物的降解能力比较差〔2〕.通过从外部输入能量或者投加催化剂可以使双氧键发生断裂,生成具有一对孤对电子的SO4·-.SO4·-(E0为2.5~3.1 V)相比较于·OH(E0为1.8~2.7 V)具有更高的氧化还原电位,在中性和酸性条件下具有较强的氧化性,从而能够应用于大多数的污水处理〔3〕. ...
过硫酸盐活化方法的研究进展
1
2020
... 高级氧化技术(AOPs)在处理一些难降解有机物方面表现出效果好、反应彻底、环境友好等特点,具有广阔的应用前景.传统的AOPs指的是能够产生·OH的氧化过程,是由W. H. Glaze 〔1〕在1987年提出.随着技术的发展,将以硫酸根自由基(SO4·-)为主要活性基团氧化降解有机物的技术也归为AOPs.该技术主要是通过活化过硫酸盐产生SO4·-.过硫酸盐(PS,E0=+2.01 V)包括过一硫酸盐(PMS,HSO5-)和过二硫酸盐(PDS,S2O82-),其具有O—O键结构,常温条件下比较稳定,但对污染物的降解能力比较差〔2〕.通过从外部输入能量或者投加催化剂可以使双氧键发生断裂,生成具有一对孤对电子的SO4·-.SO4·-(E0为2.5~3.1 V)相比较于·OH(E0为1.8~2.7 V)具有更高的氧化还原电位,在中性和酸性条件下具有较强的氧化性,从而能够应用于大多数的污水处理〔3〕. ...
1
... 高级氧化技术(AOPs)在处理一些难降解有机物方面表现出效果好、反应彻底、环境友好等特点,具有广阔的应用前景.传统的AOPs指的是能够产生·OH的氧化过程,是由W. H. Glaze 〔1〕在1987年提出.随着技术的发展,将以硫酸根自由基(SO4·-)为主要活性基团氧化降解有机物的技术也归为AOPs.该技术主要是通过活化过硫酸盐产生SO4·-.过硫酸盐(PS,E0=+2.01 V)包括过一硫酸盐(PMS,HSO5-)和过二硫酸盐(PDS,S2O82-),其具有O—O键结构,常温条件下比较稳定,但对污染物的降解能力比较差〔2〕.通过从外部输入能量或者投加催化剂可以使双氧键发生断裂,生成具有一对孤对电子的SO4·-.SO4·-(E0为2.5~3.1 V)相比较于·OH(E0为1.8~2.7 V)具有更高的氧化还原电位,在中性和酸性条件下具有较强的氧化性,从而能够应用于大多数的污水处理〔3〕. ...
Mechanism of base activation of persulfate
1
2010
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Kinetic and mechanistic investigations of the degradation of sulfamethazine in heat-activated persulfate oxidation process
1
2015
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Core-shell Fe-Fe2O3 nanostructures as effective persulfate activator for degradation of methyl orange
1
2013
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Degradation of p-nitrophenol by heat and metal ions co-activated persulfate
1
2015
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Removal of 2-MIB and geosmin using UV/persulfate: Contributions of hydroxyl and sulfate radicals
1
2015
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Enhanced activation process of persulfate by mesoporous carbon for degradation of aqueous organic pollutants: Electron transfer mechanism
1
2018
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Activation of peroxydisulfate on carbon nanotubes: Electron-transfer mechanism
1
2019
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Degradation of pentachlorophenol by hydroxyl radicals and sulfate radicals using electrochemical activation of peroxomonosulfate, peroxodisulfate and hydrogen peroxide
1
2014
... 目前,活化过硫酸盐的方法有碱活化〔4〕、热活化〔5〕、过渡金属活化〔6-7〕、紫外光活化〔8〕和碳材料活化〔9-10〕等.其中,电化学活化过硫酸盐由于具有反应体系简单、效率高以及可协同其他技术的优点,得到人们的广泛关注.研究表明,向电化学体系中加入过硫酸盐对污染物的降解有着明显的促进作用,过硫酸盐在阴极通过电子转移形式产生SO4·-,同时在阳极(BDD、PbO2、SnO2)表面会产生·OH,共同达到降解污染物的目的〔11〕.笔者综述了不同材料电极在电活化过硫酸盐降解水中有机污染物方面的研究进展,以期为电化学活化过硫酸盐技术在实际中的应用提供参考. ...
Precise control of iron activating persulfate by current generation in an electrochemical membrane reactor
1
2019
... 电化学活化过硫酸盐可以通过外部电能的输入使得双氧键断裂(见式1),同时过硫酸盐在阴极发生电子转移产生SO4·-(见式2)〔12-13〕. ...
Modeling and optimization study on sulfamethoxazole degradation by electrochemically activated persulfate process
1
2018
... 电化学活化过硫酸盐可以通过外部电能的输入使得双氧键断裂(见式1),同时过硫酸盐在阴极发生电子转移产生SO4·-(见式2)〔12-13〕. ...
Degradation of azo dye orange G in aqueous solutions by persulfate with ferrous ion
1
2010
... 活化过硫酸盐高级氧化技术被默认为是基于SO4·-,但在电化学活化过硫酸盐的过程中,由于电极材料和pH的不同,还会有·OH生成.其主要来源分为2个部分:一是具有高析氧电位的阳极会发生电解水产生·OH;二是在中性或碱性条件下SO4·-会与水或OH-之间发生反应生成·OH(见式3、式4)〔14-15〕. ...
Kinetics and modeling of the Fe(Ⅲ)/H2O2 system in the presence of sulfate in acidic aqueous solutions
1
2005
... 活化过硫酸盐高级氧化技术被默认为是基于SO4·-,但在电化学活化过硫酸盐的过程中,由于电极材料和pH的不同,还会有·OH生成.其主要来源分为2个部分:一是具有高析氧电位的阳极会发生电解水产生·OH;二是在中性或碱性条件下SO4·-会与水或OH-之间发生反应生成·OH(见式3、式4)〔14-15〕. ...
Simultaneous oxidation and reduction of arsenic by zero-valent iron nanoparticles: Understanding the significance of the core-shell structure
1
2009
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
Identification of sulfate and hydroxyl radicals in thermally activated persulfate
1
2009
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
Electro-activated persulfate oxidation of malachite green by boron-doped diamond (BDD) anode: Effect of degradation process parameters
1
2020
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
Degradation of atrazine by electrochemically activated persulfate using BDD anode: Role of radicals and influencing factors
3
2018
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Lingjun Bu等〔19〕对BDD电极活化PS降解阿特拉津(ATZ)进行了研究,结果表明,在该体系中污染物的降解是·OH、SO4·-和非自由基共同作用的结果,但是对于非自由基的作用方式没有进行探讨.同时该研究还对不同阴离子的影响进行了对比,结果显示,H2PO4-、HCO3-和NO3-对污染物的降解均有抑制作用,且抑制效果为HCO3- > H2PO4- > NO3-.L. W.Matzek等〔38〕采用BDD电极分别在过硫酸盐和硫酸盐电解液中活化PS,结果表明,在过硫酸盐电解液中,阳极室的PS浓度并不随污染物的降解而变化,这表明PS在BDD阳极没有发生转化,污染物降解可能是因为阳极表面的直接氧化;而在硫酸盐电解液中,PS浓度随污染物的减少而缓慢增加,说明过硫酸盐会在BDD阳极再生.Jing Ding等〔57〕通过实验对比了BDD/PS体系和DSA/PS体系在降解双酚A上的差异,结果表明,在ClO4-电解液中,BDD/PS体系对污染物的降解效果远高于DSA/PS体系,污染物降解率分别可达到74%和35%;在SO42-溶液中,二者对污染物的的降解率都在50%左右,表明在该介质下BDD/PS体系受到抑制,这可能是由于BDD表面的活性位点有限,高浓度的SO42-(30 mmol/L)与低浓度的PS(1 mmol/L)出现竞争;在Cl-介质中,处理9 min后,BDD/PS体系和DSA/PS体系对污染物的降解率分别可达到100%和60%,完全高于单独电解的降解效果(BDD为88%、DSA为48%),这是由于Cl-和·OH/SO4·-反应产生了含氯自由基(Cl·-、ClO·-和Cl2·-),而它们与酚类化合物的反应比·OH、SO4·-更快,从而促进了污染物的降解.总体而言,BDD电极在活化PS中的表现要明显优于DSA电极. ...
Indirect decolorization of azo dye Disperse Blue 3 by electro-activated persulfate
2
2017
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
... Kaixuan Wang等〔47〕采用Ti/SnO2-Sb为阳极活化PMS降解水中全氟辛酸(PFOA),结果表明,在电流密度为10 mA/cm2,PMS浓度为5 mmol/L,PFOA初始质量浓度为20 mg/L,电解时间为90 min的条件下,电/PMS系统对PFOA的降解率达到96.5%;且此时的反应速率kPFOA为不加PMS的3.84倍,这表明PMS成功被电化学活化.J. E. Silveira等〔20〕利用Ti/IrO2-Ta2O5为阳极并结合热活化PS对水中分散蓝3进行脱色实验,并与电/PS系统的处理效果进行了对比.结果表明,在常温(30 ℃)下,电/PS的脱色率能达到47%,当温度升高到50 ℃时,脱色率达到96%,表明电/PS结合热具有明显的协同效应.Jing Li等〔48〕利用Ti/RuO2-IrO2为阳极耦合颗粒活性炭(GAC)活化PMS降解酸性橙7,并与电/PMS系统的处理效果进行了对比.结果表明,在一定的实验条件下,电/PMS系统的脱色率可达到72.7%,而电/GAC/PMS系统的脱色率能够达到93.9%;在对PMS的激活程度上,电/PMS分解掉27%左右的PMS,而电/GAC/PMS激活了大约36%的PMS.该实验同样表明了电化学/PMS/GAC有着协同作用.Jun Li等〔36〕在利用电/CuFe2O4/PS系统降解污染物以及Chun Cai等〔35〕在利用电/Fe-SBA-15/PS系统降解污染物的研究中均发现,利用DSA电极联合其他物质活化PS的效果要好于电化学活化的效果,这也进一步表明了协同效应的存在. ...
Mineralization of aniline in aqueous solution by electrochemical activation of persulfate
2
2015
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
Electrochemical activation of persulfates at BDD anode: Radical or nonradical oxidation?
4
2018
... 在降解污染物的过程中二者都会参加反应,至于哪种物质占据主导地位还与污染物种类和pH有关.有研究表明〔16-17〕,当溶液呈酸性时SO4·-为主要的活性物质,当溶液为碱性尤其是pH > 10时,·OH是主要的反应物质.虽然在不同pH下主要的活性物质不同,但是酸性条件下的处理效果要优于碱性条件,这是因为碱性条件下·OH不能维持高的氧化能力〔18〕.铁电极作为阳极活化PS时,在弱酸性条件下就会产生氢氧化物,不仅会降低活化效果而且限制了该电极的应用;而采用BDD作阳极活化PS时,酸性条件下的阳极析氧电位要高于碱性条件,从而可提高PS的活化效率和污染物降解效率〔19〕.而在J. E. Silveira等〔20〕的研究中发现,碱性条件下污染物的降解效果要高于酸性条件,这是因为在碱性条件下PS水解产生了HO2-,然后进一步产生SO4·-、·OH和O2·-等活性物质.在酸性条件下,使用不同电极活化过硫酸盐,主要的活性物质也有可能不同.W. S. Chen等〔21〕利用Pt电极活化过硫酸盐降解苯胺,发现SO4·-是主要的反应物质,同时观测到H2O2也参与了反应.Haoran Song等〔22〕在利用BDD电极活化过硫酸盐降解卡马西平时发现,·OH是主要的活性物质,同时也发现有非自由基氧化存在. ...
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
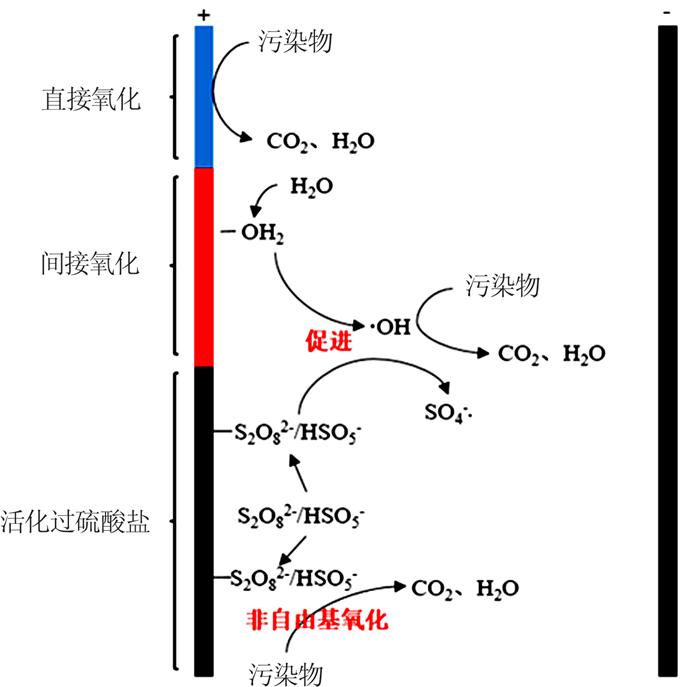
... BDD电极(Boron Doped Diamond)又称掺硼金刚石电极,具有电催化活性高、析氧电位高、稳定性好的优点,是很好的阳极材料之一,在电化学氧化污染物中应用广泛〔51-52〕.BDD电极由于硼原子的掺杂,使其与单质形式的碳材料在各个方面都有较大的差异.BDD电极活化PS降解污染物是一个复杂的过程,其中包含吸附、电解、PS的活化、污染物的氧化、解吸以及其他的一些反应,可能的活化机理〔22〕见图 1. ...
... Haoran Song等〔22〕在采用BDD阳极活化PS降解污染物的研究中,分别进行了自由基猝灭实验和自由基探针实验.结果表明,在BDD电极活化PS的过程中,阳极放电可以将吸附的PDS或PMS分子转化为特殊的过渡态结构,这种过渡结构具有非常强的活性,能够通过非自由基的形式降解污染物.在该研究中,BDD电极在没有施加电流的情况下并不能活化PS,说明本研究的活性物质均来自电活化过程而非电极中的碳材料活化.A. Farhat等〔54〕认为,这种非自由基氧化现象类似于碳纳米管活化PS的过程.类似的过渡态也在CuO/PDS系统〔55〕、纳米碳/PS系统〔56〕中发现. ...
In situ chemical oxidation of contaminated soil and groundwater using persulfate: A review
1
2010
... PS的活化方式是研究体系的重点,但自由基对污染物的作用机制研究是关键.采用电化学活化过硫酸盐,SO4·-和·OH都具有重要的研究意义,且二者与污染物作用机理不完全相同.目前,已经验证的自由基作用方式为氢提取、加成和电子转移,其中SO4·-倾向于电子转移的方式,而·OH更倾向于加成和氢提取的方式〔23〕.E. Mousset等〔24〕在利用电Fenton法降解CCl4时发现,·OH存在原位取代的反应方式,这表明·OH与污染物存在第4种作用方式.而在实际水处理中自由基作用方式与污染物种类密切相关,如SO4·-与芳香类化合物反应时主要是通过电子转移(见式5),与酯类化合物及醇类、醚、烷烃主要是通过氢提取的反应方式(见式6),与不饱和烯烃类化合物主要是通过加成的反应方式(见式7)〔25-28〕. ...
An unprecedented route of·OH radical reactivity evidenced by an electrocatalytical process: Ipso-substitution with perhalogenocarbon compounds
1
2018
... PS的活化方式是研究体系的重点,但自由基对污染物的作用机制研究是关键.采用电化学活化过硫酸盐,SO4·-和·OH都具有重要的研究意义,且二者与污染物作用机理不完全相同.目前,已经验证的自由基作用方式为氢提取、加成和电子转移,其中SO4·-倾向于电子转移的方式,而·OH更倾向于加成和氢提取的方式〔23〕.E. Mousset等〔24〕在利用电Fenton法降解CCl4时发现,·OH存在原位取代的反应方式,这表明·OH与污染物存在第4种作用方式.而在实际水处理中自由基作用方式与污染物种类密切相关,如SO4·-与芳香类化合物反应时主要是通过电子转移(见式5),与酯类化合物及醇类、醚、烷烃主要是通过氢提取的反应方式(见式6),与不饱和烯烃类化合物主要是通过加成的反应方式(见式7)〔25-28〕. ...
Rate constants for reactions of SO4·-radicals in acetonitrile
1
1993
... PS的活化方式是研究体系的重点,但自由基对污染物的作用机制研究是关键.采用电化学活化过硫酸盐,SO4·-和·OH都具有重要的研究意义,且二者与污染物作用机理不完全相同.目前,已经验证的自由基作用方式为氢提取、加成和电子转移,其中SO4·-倾向于电子转移的方式,而·OH更倾向于加成和氢提取的方式〔23〕.E. Mousset等〔24〕在利用电Fenton法降解CCl4时发现,·OH存在原位取代的反应方式,这表明·OH与污染物存在第4种作用方式.而在实际水处理中自由基作用方式与污染物种类密切相关,如SO4·-与芳香类化合物反应时主要是通过电子转移(见式5),与酯类化合物及醇类、醚、烷烃主要是通过氢提取的反应方式(见式6),与不饱和烯烃类化合物主要是通过加成的反应方式(见式7)〔25-28〕. ...
Radiation chemical oxidation of benzaldehyde, acetophenone, and benzophenone
0
1997
Reactivity of selected volatile organic compounds(VOCs) toward the sulfate radical(SO4·-)
0
2001
金属有机骨架及其衍生材料活化过硫酸盐在水处理中的应用进展
1
2019
... PS的活化方式是研究体系的重点,但自由基对污染物的作用机制研究是关键.采用电化学活化过硫酸盐,SO4·-和·OH都具有重要的研究意义,且二者与污染物作用机理不完全相同.目前,已经验证的自由基作用方式为氢提取、加成和电子转移,其中SO4·-倾向于电子转移的方式,而·OH更倾向于加成和氢提取的方式〔23〕.E. Mousset等〔24〕在利用电Fenton法降解CCl4时发现,·OH存在原位取代的反应方式,这表明·OH与污染物存在第4种作用方式.而在实际水处理中自由基作用方式与污染物种类密切相关,如SO4·-与芳香类化合物反应时主要是通过电子转移(见式5),与酯类化合物及醇类、醚、烷烃主要是通过氢提取的反应方式(见式6),与不饱和烯烃类化合物主要是通过加成的反应方式(见式7)〔25-28〕. ...
Electrolytic manipulation of persulfate reactivity by iron electrodes for trichloroethylene degradation in groundwater
2
2014
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Songhu Yuan等〔29〕利用铁作阳极活化PS降解地下水中的三氯乙烯(TEC),研究表明,通过调节施加在铁电极上的电流,可以定量地加速或抑制TCE的降解,且降解过程遵循k1=0.000 53Iv + 0.059(k1为伪一级速率常数,Iv为电流密度);·OH与SO4·-的贡献率分别为68.8%、10.4%,而·OH的来源可能是由于PS与水反应产生H2O2,在Fe2+存在时发生了Fenton反应〔41〕.P. Jeon等〔30〕通过研究发现,对电流密度的控制可以影响Fe2+的生成量.Lingjun Bu等〔42〕用铁作电极活化过硫酸盐降解水中奥卡西平,实验表明,在低电流密度时,增加电流,污染物的去除速率也会增加;高电流密度时,增加电流,反而会降低降解速率.这可能是由于在高电流下产生了过量的Fe2+,其与SO4·-发生了猝灭反应(见式11),从而使得污染物的降解速率下降.Jun Li等〔43〕在利用铁电极活化过硫酸盐降解二硝基苯的研究中同样观测到上述现象;同时在该研究中作者比较了单独PS、单独电化学和电化学/PS结合3种体系去除COD的效果,发现电化学/PS结合(63%) > 电化学(23%) > PS(3.6%),这表明电化学与过硫酸盐具有明显的协同作用. ...
Controlled release of iron for activation of persulfate to oxidize orange G using iron anode
2
2017
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Songhu Yuan等〔29〕利用铁作阳极活化PS降解地下水中的三氯乙烯(TEC),研究表明,通过调节施加在铁电极上的电流,可以定量地加速或抑制TCE的降解,且降解过程遵循k1=0.000 53Iv + 0.059(k1为伪一级速率常数,Iv为电流密度);·OH与SO4·-的贡献率分别为68.8%、10.4%,而·OH的来源可能是由于PS与水反应产生H2O2,在Fe2+存在时发生了Fenton反应〔41〕.P. Jeon等〔30〕通过研究发现,对电流密度的控制可以影响Fe2+的生成量.Lingjun Bu等〔42〕用铁作电极活化过硫酸盐降解水中奥卡西平,实验表明,在低电流密度时,增加电流,污染物的去除速率也会增加;高电流密度时,增加电流,反而会降低降解速率.这可能是由于在高电流下产生了过量的Fe2+,其与SO4·-发生了猝灭反应(见式11),从而使得污染物的降解速率下降.Jun Li等〔43〕在利用铁电极活化过硫酸盐降解二硝基苯的研究中同样观测到上述现象;同时在该研究中作者比较了单独PS、单独电化学和电化学/PS结合3种体系去除COD的效果,发现电化学/PS结合(63%) > 电化学(23%) > PS(3.6%),这表明电化学与过硫酸盐具有明显的协同作用. ...
Degradation of sulfamethoxazole by electrochemically activated persulfate using iron anode
1
2019
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
Degradation of diuron by electrochemically activated persulfate
1
2016
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
Improved degradation of anthraquinone dye by electrochemical activation of PDS
2
2019
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... 除了铁电极外,也有研究用Pt电极和Ti/Pt电极活化PS降解水中污染物.Pt电极是一种贵金属电极,其在电化学氧化中常被用作为阳极,但处理污染物的效果一般,这是由于Pt电极析氧电位过低所导致.但是将该电化学氧化与活化PS相结合,能进一步增强有机物的降解能力.W. Chen等〔44〕对Pt作阳极活化PS处理水中二硝基甲苯进行了研究,该研究通过引入氮气减少氧气的含量,避免了阳极电解产生的氧气和S2O82-在阴极争夺电子,从而使得SO4·-能够尽可能多地生成.在该研究中活性物质有SO4·-、·OH和H2O2,其中SO4·-起主要作用,而H2O2的贡献非常微小;最佳反应条件:电压6 V,温度318 K,N2流量150 mL/min,pH=0.5,PS投加质量分数为1.7%,在此条件下TOC去除率达到95%.Xue Li等〔33〕在利用Pt作阳极活化PS降解水中活性艳蓝的研究中发现,分别采用含NO3-、Cl-和SO42-的溶液作为电解液,处理60 min后,污染物降解率分别为92.08%、97.95%和59.66%.由于Cl-在降解过程中可能会和污染物结合生成具有毒性的氯代物,因此以含NO3-的可溶盐作为最佳电解质.以含NO3-的可溶盐作为电解质,NO3-和SO4·-反应会产生NO3·,进而与水反应产生·OH,从而可促进污染物的降解.同时在后续的自由基猝灭实验中发现,SO4·-与·OH在反应中的贡献率分别为17.19%、70.86%,没有发现NO3·的存在.Ti/Pt电极很少用于活化PS,但在现有的研究中发现,该电极活化PS产生的是非自由基氧化.Haoran Song等〔34〕在研究中发现,在利用Ti/Pt作阳极活化PDS时并没有自由基的产生,而是PDS在阳极表面形成一种具有高活性的过渡态结构.这种高活性的过渡态结构存在的时间很短暂,能够快速与污染物发生反应.由于缺乏合适的表征手段,该过渡态的结构并没有被深入研究.由于目前Pt电极作为阳极活化PS的研究很少,所以实验中存在的非自由基氧化,以及形成机制不具有代表性. ...
Nonradical oxidation from electrochemical activation of peroxydisulfate at Ti/Pt anode: Efficiency, mechanism and influencing factors
2
2017
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... 除了铁电极外,也有研究用Pt电极和Ti/Pt电极活化PS降解水中污染物.Pt电极是一种贵金属电极,其在电化学氧化中常被用作为阳极,但处理污染物的效果一般,这是由于Pt电极析氧电位过低所导致.但是将该电化学氧化与活化PS相结合,能进一步增强有机物的降解能力.W. Chen等〔44〕对Pt作阳极活化PS处理水中二硝基甲苯进行了研究,该研究通过引入氮气减少氧气的含量,避免了阳极电解产生的氧气和S2O82-在阴极争夺电子,从而使得SO4·-能够尽可能多地生成.在该研究中活性物质有SO4·-、·OH和H2O2,其中SO4·-起主要作用,而H2O2的贡献非常微小;最佳反应条件:电压6 V,温度318 K,N2流量150 mL/min,pH=0.5,PS投加质量分数为1.7%,在此条件下TOC去除率达到95%.Xue Li等〔33〕在利用Pt作阳极活化PS降解水中活性艳蓝的研究中发现,分别采用含NO3-、Cl-和SO42-的溶液作为电解液,处理60 min后,污染物降解率分别为92.08%、97.95%和59.66%.由于Cl-在降解过程中可能会和污染物结合生成具有毒性的氯代物,因此以含NO3-的可溶盐作为最佳电解质.以含NO3-的可溶盐作为电解质,NO3-和SO4·-反应会产生NO3·,进而与水反应产生·OH,从而可促进污染物的降解.同时在后续的自由基猝灭实验中发现,SO4·-与·OH在反应中的贡献率分别为17.19%、70.86%,没有发现NO3·的存在.Ti/Pt电极很少用于活化PS,但在现有的研究中发现,该电极活化PS产生的是非自由基氧化.Haoran Song等〔34〕在研究中发现,在利用Ti/Pt作阳极活化PDS时并没有自由基的产生,而是PDS在阳极表面形成一种具有高活性的过渡态结构.这种高活性的过渡态结构存在的时间很短暂,能够快速与污染物发生反应.由于缺乏合适的表征手段,该过渡态的结构并没有被深入研究.由于目前Pt电极作为阳极活化PS的研究很少,所以实验中存在的非自由基氧化,以及形成机制不具有代表性. ...
Electro-assisted heterogeneous activation of persulfate by Fe/SBA-15 for the degradation of OrangeⅡ
2
2016
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Kaixuan Wang等〔47〕采用Ti/SnO2-Sb为阳极活化PMS降解水中全氟辛酸(PFOA),结果表明,在电流密度为10 mA/cm2,PMS浓度为5 mmol/L,PFOA初始质量浓度为20 mg/L,电解时间为90 min的条件下,电/PMS系统对PFOA的降解率达到96.5%;且此时的反应速率kPFOA为不加PMS的3.84倍,这表明PMS成功被电化学活化.J. E. Silveira等〔20〕利用Ti/IrO2-Ta2O5为阳极并结合热活化PS对水中分散蓝3进行脱色实验,并与电/PS系统的处理效果进行了对比.结果表明,在常温(30 ℃)下,电/PS的脱色率能达到47%,当温度升高到50 ℃时,脱色率达到96%,表明电/PS结合热具有明显的协同效应.Jing Li等〔48〕利用Ti/RuO2-IrO2为阳极耦合颗粒活性炭(GAC)活化PMS降解酸性橙7,并与电/PMS系统的处理效果进行了对比.结果表明,在一定的实验条件下,电/PMS系统的脱色率可达到72.7%,而电/GAC/PMS系统的脱色率能够达到93.9%;在对PMS的激活程度上,电/PMS分解掉27%左右的PMS,而电/GAC/PMS激活了大约36%的PMS.该实验同样表明了电化学/PMS/GAC有着协同作用.Jun Li等〔36〕在利用电/CuFe2O4/PS系统降解污染物以及Chun Cai等〔35〕在利用电/Fe-SBA-15/PS系统降解污染物的研究中均发现,利用DSA电极联合其他物质活化PS的效果要好于电化学活化的效果,这也进一步表明了协同效应的存在. ...
Improving the degradation of atrazine in the three-dimensional (3D) electrochemical process using CuFe2O4 as both particle electrode and catalyst for persulfate activation
2
2019
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Kaixuan Wang等〔47〕采用Ti/SnO2-Sb为阳极活化PMS降解水中全氟辛酸(PFOA),结果表明,在电流密度为10 mA/cm2,PMS浓度为5 mmol/L,PFOA初始质量浓度为20 mg/L,电解时间为90 min的条件下,电/PMS系统对PFOA的降解率达到96.5%;且此时的反应速率kPFOA为不加PMS的3.84倍,这表明PMS成功被电化学活化.J. E. Silveira等〔20〕利用Ti/IrO2-Ta2O5为阳极并结合热活化PS对水中分散蓝3进行脱色实验,并与电/PS系统的处理效果进行了对比.结果表明,在常温(30 ℃)下,电/PS的脱色率能达到47%,当温度升高到50 ℃时,脱色率达到96%,表明电/PS结合热具有明显的协同效应.Jing Li等〔48〕利用Ti/RuO2-IrO2为阳极耦合颗粒活性炭(GAC)活化PMS降解酸性橙7,并与电/PMS系统的处理效果进行了对比.结果表明,在一定的实验条件下,电/PMS系统的脱色率可达到72.7%,而电/GAC/PMS系统的脱色率能够达到93.9%;在对PMS的激活程度上,电/PMS分解掉27%左右的PMS,而电/GAC/PMS激活了大约36%的PMS.该实验同样表明了电化学/PMS/GAC有着协同作用.Jun Li等〔36〕在利用电/CuFe2O4/PS系统降解污染物以及Chun Cai等〔35〕在利用电/Fe-SBA-15/PS系统降解污染物的研究中均发现,利用DSA电极联合其他物质活化PS的效果要好于电化学活化的效果,这也进一步表明了协同效应的存在. ...
Degradation of clofibric acid in aqueous solution by an EC/Fe3+/PMS process
1
2014
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
Understanding electrochemically activated persulfate and its application to ciprofloxacin abatement
2
2018
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... Lingjun Bu等〔19〕对BDD电极活化PS降解阿特拉津(ATZ)进行了研究,结果表明,在该体系中污染物的降解是·OH、SO4·-和非自由基共同作用的结果,但是对于非自由基的作用方式没有进行探讨.同时该研究还对不同阴离子的影响进行了对比,结果显示,H2PO4-、HCO3-和NO3-对污染物的降解均有抑制作用,且抑制效果为HCO3- > H2PO4- > NO3-.L. W.Matzek等〔38〕采用BDD电极分别在过硫酸盐和硫酸盐电解液中活化PS,结果表明,在过硫酸盐电解液中,阳极室的PS浓度并不随污染物的降解而变化,这表明PS在BDD阳极没有发生转化,污染物降解可能是因为阳极表面的直接氧化;而在硫酸盐电解液中,PS浓度随污染物的减少而缓慢增加,说明过硫酸盐会在BDD阳极再生.Jing Ding等〔57〕通过实验对比了BDD/PS体系和DSA/PS体系在降解双酚A上的差异,结果表明,在ClO4-电解液中,BDD/PS体系对污染物的降解效果远高于DSA/PS体系,污染物降解率分别可达到74%和35%;在SO42-溶液中,二者对污染物的的降解率都在50%左右,表明在该介质下BDD/PS体系受到抑制,这可能是由于BDD表面的活性位点有限,高浓度的SO42-(30 mmol/L)与低浓度的PS(1 mmol/L)出现竞争;在Cl-介质中,处理9 min后,BDD/PS体系和DSA/PS体系对污染物的降解率分别可达到100%和60%,完全高于单独电解的降解效果(BDD为88%、DSA为48%),这是由于Cl-和·OH/SO4·-反应产生了含氯自由基(Cl·-、ClO·-和Cl2·-),而它们与酚类化合物的反应比·OH、SO4·-更快,从而促进了污染物的降解.总体而言,BDD电极在活化PS中的表现要明显优于DSA电极. ...
Electrochemical activation of peroxymonosulfate with ACF cathode: Kinetics, influencing factors, mechanism, and application potential
2
2019
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
... 除BDD电极外,也有研究采用其他碳材料电极活化PS降解有机污染物,并且取得了良好的效果.这些电极不但可以作为阳极还可以做阴极,但是作为阴极活化PS时与阳极的反应略有不同,除了在阴极上得电子外,还会有其他活性物质作为中间体参与活化(见式20、式21).Zhen Liu等〔39〕采用活性炭纤维(ACF)作为阴极活化PMS降解水中卡马西平,研究表明,在降解过程中活性物质起主要作用,占78.02%(其中·OH、SO4·-和1O2分别占29.27%、58.86%和11.87%),而非自由基氧化仅占1.36%.其中·OH和SO4·-在阴极与阳极均有产生,而1O2主要是通过阴极上·OH与PMS的反应生成(见式22).Lingjun Bu等〔58〕在研究中发现,由于S2O82-与石墨毡阴极之间的静电斥力,不太容易在阴极得电子产生SO4·-,通过自由基猝灭实验可知,在阴极产生的O2·-在阴极活化PS中扮演了重要的角色,其主要来源是电解产生的O2在阴极得电子形成. ...
Degradation of aniline by electrochemical activation of peroxydisulfate at MWCNT cathode: The proofed concept of nonradical oxidation process
1
2018
... 不同材料电极在活化过硫酸盐处理水中有机污染物的应用现状
| 污染物 | 阳极 | 阴极 | 氧化剂及投加量 | 时间/min | 去除率/% | 文献 |
| 三氯乙烯 | 铁 | MMO | PDS,2 mmol/L | 30 | 100 | 〔29〕 |
| 橙黄G | 铁 | Ti | PDS,5 mmol/L | 240 | 100 | 〔30〕 |
| 磺胺甲恶唑 | 铁 | 石墨 | PDS,3.5 mmol/L | 60 | >80 | 〔31〕 |
| 敌草隆 | 铁 | 铁 | PDS,1 mmol/L | 15 | >60 | 〔32〕 |
| 苯胺 | Pt | Pt | PDS,质量分数3% | 420 | >70 | 〔21〕 |
| 蒽醌染料 | Pt | 石墨 | PDS,10 mmol/L | 60 | 93.75 | 〔33〕 |
| 卡马西平 | Ti/Pt | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔34〕 |
| 酸性橙(Orange Ⅱ) | Ti/RuO2-IrO2 | 不锈钢 | PDS,4.2 mmol/L | 60 | 89 | 〔35〕 |
| 阿特拉津 | Ti/RuO2-IrO2 | 不锈钢 | PDS,4 mmol/L | 60 | >99 | 〔36〕 |
| 氯贝酸(clofibric acid) | Ti/RuO2-IrO2 | 不锈钢 | PMS,10 mmol/L | 60 | 82 | 〔37〕 |
| 卡马西平 | BDD | 不锈钢 | PDS,5 mmol/L | 30 | >80 | 〔22〕 |
| 阿特拉津 | BDD | 不锈钢 | PDS,1 mmol/L | 30 | 78.2 | 〔19〕 |
| 环丙沙星 | BDD | 石墨 | PDS,22 mmol/L | 120 | 84 | 〔38〕 |
| 卡马西平 | Ti/Pt | 活性碳毡 | PMS,50 mmol/L | 40 | 100 | 〔39〕 |
| 苯胺 | 石墨 | 碳纳米管 | PDS,5.55 mmol/L | 150 | >90 | 〔40〕 |
2.1 金属电极2.1.1 铁电极金属铁具有来源广泛、价格低廉、还原速度快等优点,很早就被用作电极活化过硫酸盐.采用铁电极活化过硫酸盐的原理:作为阳极的铁在通入电流后失去电子转化为Fe2+,Fe2+再进一步与过硫酸盐反应产生SO4·-,该原理就是利用Fe2+活化过硫酸盐(见式8、式9).采用铁电极作阳极活化PS,过硫酸盐在阴极通过电子转移被活化产生SO4·-(见式2),同时在阴极Fe3+会通过得电子产生Fe2+(见式10),但这一过程与阴极活化过硫酸盐会互相竞争电子,从而导致阴极活化效率低.利用铁作阳极不仅可以降低能耗,而且还可以提高过硫酸盐与Fe2+的利用效率,能够有效避免副反应的发生(见式11). ...
Response to comment on "Electrolytic manipulation of persulfate reactivity by iron electrodes for TCE degradation in groundwater"
1
2014
... Songhu Yuan等〔29〕利用铁作阳极活化PS降解地下水中的三氯乙烯(TEC),研究表明,通过调节施加在铁电极上的电流,可以定量地加速或抑制TCE的降解,且降解过程遵循k1=0.000 53Iv + 0.059(k1为伪一级速率常数,Iv为电流密度);·OH与SO4·-的贡献率分别为68.8%、10.4%,而·OH的来源可能是由于PS与水反应产生H2O2,在Fe2+存在时发生了Fenton反应〔41〕.P. Jeon等〔30〕通过研究发现,对电流密度的控制可以影响Fe2+的生成量.Lingjun Bu等〔42〕用铁作电极活化过硫酸盐降解水中奥卡西平,实验表明,在低电流密度时,增加电流,污染物的去除速率也会增加;高电流密度时,增加电流,反而会降低降解速率.这可能是由于在高电流下产生了过量的Fe2+,其与SO4·-发生了猝灭反应(见式11),从而使得污染物的降解速率下降.Jun Li等〔43〕在利用铁电极活化过硫酸盐降解二硝基苯的研究中同样观测到上述现象;同时在该研究中作者比较了单独PS、单独电化学和电化学/PS结合3种体系去除COD的效果,发现电化学/PS结合(63%) > 电化学(23%) > PS(3.6%),这表明电化学与过硫酸盐具有明显的协同作用. ...
Iron electrode as efficient persulfate activator for oxcarbazepine degradation: Performance, mechanism, and kinetic modeling
1
2017
... Songhu Yuan等〔29〕利用铁作阳极活化PS降解地下水中的三氯乙烯(TEC),研究表明,通过调节施加在铁电极上的电流,可以定量地加速或抑制TCE的降解,且降解过程遵循k1=0.000 53Iv + 0.059(k1为伪一级速率常数,Iv为电流密度);·OH与SO4·-的贡献率分别为68.8%、10.4%,而·OH的来源可能是由于PS与水反应产生H2O2,在Fe2+存在时发生了Fenton反应〔41〕.P. Jeon等〔30〕通过研究发现,对电流密度的控制可以影响Fe2+的生成量.Lingjun Bu等〔42〕用铁作电极活化过硫酸盐降解水中奥卡西平,实验表明,在低电流密度时,增加电流,污染物的去除速率也会增加;高电流密度时,增加电流,反而会降低降解速率.这可能是由于在高电流下产生了过量的Fe2+,其与SO4·-发生了猝灭反应(见式11),从而使得污染物的降解速率下降.Jun Li等〔43〕在利用铁电极活化过硫酸盐降解二硝基苯的研究中同样观测到上述现象;同时在该研究中作者比较了单独PS、单独电化学和电化学/PS结合3种体系去除COD的效果,发现电化学/PS结合(63%) > 电化学(23%) > PS(3.6%),这表明电化学与过硫酸盐具有明显的协同作用. ...
Electrolysis assisted persulfate with annular iron sheet as anode for the enhanced degradation of 2, 4-dinitrophenol in aqueous solution
1
2018
... Songhu Yuan等〔29〕利用铁作阳极活化PS降解地下水中的三氯乙烯(TEC),研究表明,通过调节施加在铁电极上的电流,可以定量地加速或抑制TCE的降解,且降解过程遵循k1=0.000 53Iv + 0.059(k1为伪一级速率常数,Iv为电流密度);·OH与SO4·-的贡献率分别为68.8%、10.4%,而·OH的来源可能是由于PS与水反应产生H2O2,在Fe2+存在时发生了Fenton反应〔41〕.P. Jeon等〔30〕通过研究发现,对电流密度的控制可以影响Fe2+的生成量.Lingjun Bu等〔42〕用铁作电极活化过硫酸盐降解水中奥卡西平,实验表明,在低电流密度时,增加电流,污染物的去除速率也会增加;高电流密度时,增加电流,反而会降低降解速率.这可能是由于在高电流下产生了过量的Fe2+,其与SO4·-发生了猝灭反应(见式11),从而使得污染物的降解速率下降.Jun Li等〔43〕在利用铁电极活化过硫酸盐降解二硝基苯的研究中同样观测到上述现象;同时在该研究中作者比较了单独PS、单独电化学和电化学/PS结合3种体系去除COD的效果,发现电化学/PS结合(63%) > 电化学(23%) > PS(3.6%),这表明电化学与过硫酸盐具有明显的协同作用. ...
Mineralization of dinitrotoluenes in industrial wastewater by electro-activated persulfate oxidation
1
2014
... 除了铁电极外,也有研究用Pt电极和Ti/Pt电极活化PS降解水中污染物.Pt电极是一种贵金属电极,其在电化学氧化中常被用作为阳极,但处理污染物的效果一般,这是由于Pt电极析氧电位过低所导致.但是将该电化学氧化与活化PS相结合,能进一步增强有机物的降解能力.W. Chen等〔44〕对Pt作阳极活化PS处理水中二硝基甲苯进行了研究,该研究通过引入氮气减少氧气的含量,避免了阳极电解产生的氧气和S2O82-在阴极争夺电子,从而使得SO4·-能够尽可能多地生成.在该研究中活性物质有SO4·-、·OH和H2O2,其中SO4·-起主要作用,而H2O2的贡献非常微小;最佳反应条件:电压6 V,温度318 K,N2流量150 mL/min,pH=0.5,PS投加质量分数为1.7%,在此条件下TOC去除率达到95%.Xue Li等〔33〕在利用Pt作阳极活化PS降解水中活性艳蓝的研究中发现,分别采用含NO3-、Cl-和SO42-的溶液作为电解液,处理60 min后,污染物降解率分别为92.08%、97.95%和59.66%.由于Cl-在降解过程中可能会和污染物结合生成具有毒性的氯代物,因此以含NO3-的可溶盐作为最佳电解质.以含NO3-的可溶盐作为电解质,NO3-和SO4·-反应会产生NO3·,进而与水反应产生·OH,从而可促进污染物的降解.同时在后续的自由基猝灭实验中发现,SO4·-与·OH在反应中的贡献率分别为17.19%、70.86%,没有发现NO3·的存在.Ti/Pt电极很少用于活化PS,但在现有的研究中发现,该电极活化PS产生的是非自由基氧化.Haoran Song等〔34〕在研究中发现,在利用Ti/Pt作阳极活化PDS时并没有自由基的产生,而是PDS在阳极表面形成一种具有高活性的过渡态结构.这种高活性的过渡态结构存在的时间很短暂,能够快速与污染物发生反应.由于缺乏合适的表征手段,该过渡态的结构并没有被深入研究.由于目前Pt电极作为阳极活化PS的研究很少,所以实验中存在的非自由基氧化,以及形成机制不具有代表性. ...
Preparation and characterization of a Pd modified Ti/SnO2-Sb anode and its electrochemical degradation of Ni-EDTA
1
2017
... 金属氧化物电极(MMO)又称为形稳型阳极(DSA),因其具有良好的电催化特性及稳定性被广泛应用于难降解废水的处理〔45〕.采用DSA电极单独处理污染物时需要施加高电流以达到降解效果,但将其与过硫酸盐相结合,施加较小的电流便可以获得更好的效果.DSA电极除了在阴极通过电子转移活化过硫酸盐产生SO4·-外,在阳极产生的·OH也可以间接活化过硫酸盐(见式12)〔46〕.已有的研究表明,在采用DSA电极活化过硫酸盐中,阴极除了有过硫酸盐的活化外,还会发生O2的还原(见式13),这会形成互相争夺电子的局面,使得过硫酸盐的活化效率降低.因此,在利用DSA电极活化过硫酸盐时,多会选择与其他活化技术联合使用. ...
Electrochemical oxidation of ofloxacin using a TiO2-based SnO2-Sb/polytetrafluoroethylene resin-PbO2 electrode: Reaction kinetics and mass transfer impact
1
2017
... 金属氧化物电极(MMO)又称为形稳型阳极(DSA),因其具有良好的电催化特性及稳定性被广泛应用于难降解废水的处理〔45〕.采用DSA电极单独处理污染物时需要施加高电流以达到降解效果,但将其与过硫酸盐相结合,施加较小的电流便可以获得更好的效果.DSA电极除了在阴极通过电子转移活化过硫酸盐产生SO4·-外,在阳极产生的·OH也可以间接活化过硫酸盐(见式12)〔46〕.已有的研究表明,在采用DSA电极活化过硫酸盐中,阴极除了有过硫酸盐的活化外,还会发生O2的还原(见式13),这会形成互相争夺电子的局面,使得过硫酸盐的活化效率降低.因此,在利用DSA电极活化过硫酸盐时,多会选择与其他活化技术联合使用. ...
Enhanced perfluorooctanoic acid degradation by electrochemical activation of peroxymonosulfate in aqueous solution
1
2020
... Kaixuan Wang等〔47〕采用Ti/SnO2-Sb为阳极活化PMS降解水中全氟辛酸(PFOA),结果表明,在电流密度为10 mA/cm2,PMS浓度为5 mmol/L,PFOA初始质量浓度为20 mg/L,电解时间为90 min的条件下,电/PMS系统对PFOA的降解率达到96.5%;且此时的反应速率kPFOA为不加PMS的3.84倍,这表明PMS成功被电化学活化.J. E. Silveira等〔20〕利用Ti/IrO2-Ta2O5为阳极并结合热活化PS对水中分散蓝3进行脱色实验,并与电/PS系统的处理效果进行了对比.结果表明,在常温(30 ℃)下,电/PS的脱色率能达到47%,当温度升高到50 ℃时,脱色率达到96%,表明电/PS结合热具有明显的协同效应.Jing Li等〔48〕利用Ti/RuO2-IrO2为阳极耦合颗粒活性炭(GAC)活化PMS降解酸性橙7,并与电/PMS系统的处理效果进行了对比.结果表明,在一定的实验条件下,电/PMS系统的脱色率可达到72.7%,而电/GAC/PMS系统的脱色率能够达到93.9%;在对PMS的激活程度上,电/PMS分解掉27%左右的PMS,而电/GAC/PMS激活了大约36%的PMS.该实验同样表明了电化学/PMS/GAC有着协同作用.Jun Li等〔36〕在利用电/CuFe2O4/PS系统降解污染物以及Chun Cai等〔35〕在利用电/Fe-SBA-15/PS系统降解污染物的研究中均发现,利用DSA电极联合其他物质活化PS的效果要好于电化学活化的效果,这也进一步表明了协同效应的存在. ...
Degradation of Acid Orange 7 using peroxymonosulfate catalyzed by granulated activated carbon and enhanced by electrolysis
1
2017
... Kaixuan Wang等〔47〕采用Ti/SnO2-Sb为阳极活化PMS降解水中全氟辛酸(PFOA),结果表明,在电流密度为10 mA/cm2,PMS浓度为5 mmol/L,PFOA初始质量浓度为20 mg/L,电解时间为90 min的条件下,电/PMS系统对PFOA的降解率达到96.5%;且此时的反应速率kPFOA为不加PMS的3.84倍,这表明PMS成功被电化学活化.J. E. Silveira等〔20〕利用Ti/IrO2-Ta2O5为阳极并结合热活化PS对水中分散蓝3进行脱色实验,并与电/PS系统的处理效果进行了对比.结果表明,在常温(30 ℃)下,电/PS的脱色率能达到47%,当温度升高到50 ℃时,脱色率达到96%,表明电/PS结合热具有明显的协同效应.Jing Li等〔48〕利用Ti/RuO2-IrO2为阳极耦合颗粒活性炭(GAC)活化PMS降解酸性橙7,并与电/PMS系统的处理效果进行了对比.结果表明,在一定的实验条件下,电/PMS系统的脱色率可达到72.7%,而电/GAC/PMS系统的脱色率能够达到93.9%;在对PMS的激活程度上,电/PMS分解掉27%左右的PMS,而电/GAC/PMS激活了大约36%的PMS.该实验同样表明了电化学/PMS/GAC有着协同作用.Jun Li等〔36〕在利用电/CuFe2O4/PS系统降解污染物以及Chun Cai等〔35〕在利用电/Fe-SBA-15/PS系统降解污染物的研究中均发现,利用DSA电极联合其他物质活化PS的效果要好于电化学活化的效果,这也进一步表明了协同效应的存在. ...
Electrochemical synthesis of peroxodisulfates from dilute sulfate solutions for detoxification of biological media
1
2008
... 研究表明〔49-50〕,在硫酸盐电解液中过硫酸盐可以在DSA阳极再生(见式14、式15).在目前的研究中硫酸盐被认为是惰性的,通常在电活化PS中被用作电解质,但是很少有研究这个过程中PS在阳极再生的情况.如果在污染物降解的同时,PS在阳极获得再生,这会使得污染物与活性物质之间的反应更加具有持久性. ...
Indirect electrochemical synthesis of active oxygen in dilute sulfate solutions
1
2009
... 研究表明〔49-50〕,在硫酸盐电解液中过硫酸盐可以在DSA阳极再生(见式14、式15).在目前的研究中硫酸盐被认为是惰性的,通常在电活化PS中被用作电解质,但是很少有研究这个过程中PS在阳极再生的情况.如果在污染物降解的同时,PS在阳极获得再生,这会使得污染物与活性物质之间的反应更加具有持久性. ...
Electrochemical oxidation of perfluorooctane sulfonate(PFOS) substitute by modified boron doped diamond(BDD) anodes
1
2020
... BDD电极(Boron Doped Diamond)又称掺硼金刚石电极,具有电催化活性高、析氧电位高、稳定性好的优点,是很好的阳极材料之一,在电化学氧化污染物中应用广泛〔51-52〕.BDD电极由于硼原子的掺杂,使其与单质形式的碳材料在各个方面都有较大的差异.BDD电极活化PS降解污染物是一个复杂的过程,其中包含吸附、电解、PS的活化、污染物的氧化、解吸以及其他的一些反应,可能的活化机理〔22〕见图 1. ...
Electrochemical oxidation of dibenzothiophene compounds on BDD electrode in acetonitrile-water medium
1
2019
... BDD电极(Boron Doped Diamond)又称掺硼金刚石电极,具有电催化活性高、析氧电位高、稳定性好的优点,是很好的阳极材料之一,在电化学氧化污染物中应用广泛〔51-52〕.BDD电极由于硼原子的掺杂,使其与单质形式的碳材料在各个方面都有较大的差异.BDD电极活化PS降解污染物是一个复杂的过程,其中包含吸附、电解、PS的活化、污染物的氧化、解吸以及其他的一些反应,可能的活化机理〔22〕见图 1. ...
Challenges and opportunities for electrochemical processes as next-generation technologies for the treatment of contaminated water
1
2015
... 在BDD电极活化PS中,SO4·-的产生包括PS的活化和阳极硫酸根的直接氧化(见式16),形成的自由基除了降解污染物外,还会相互结合生成过硫酸盐(见式17)〔53〕. ...
Removal of persistent organic contaminants by electrochemically activated sulfate
1
2015
... Haoran Song等〔22〕在采用BDD阳极活化PS降解污染物的研究中,分别进行了自由基猝灭实验和自由基探针实验.结果表明,在BDD电极活化PS的过程中,阳极放电可以将吸附的PDS或PMS分子转化为特殊的过渡态结构,这种过渡结构具有非常强的活性,能够通过非自由基的形式降解污染物.在该研究中,BDD电极在没有施加电流的情况下并不能活化PS,说明本研究的活性物质均来自电活化过程而非电极中的碳材料活化.A. Farhat等〔54〕认为,这种非自由基氧化现象类似于碳纳米管活化PS的过程.类似的过渡态也在CuO/PDS系统〔55〕、纳米碳/PS系统〔56〕中发现. ...
Efficient peroxydisulfate activation process not relying on sulfate radical generation for water pollutant degradation
1
2014
... Haoran Song等〔22〕在采用BDD阳极活化PS降解污染物的研究中,分别进行了自由基猝灭实验和自由基探针实验.结果表明,在BDD电极活化PS的过程中,阳极放电可以将吸附的PDS或PMS分子转化为特殊的过渡态结构,这种过渡结构具有非常强的活性,能够通过非自由基的形式降解污染物.在该研究中,BDD电极在没有施加电流的情况下并不能活化PS,说明本研究的活性物质均来自电活化过程而非电极中的碳材料活化.A. Farhat等〔54〕认为,这种非自由基氧化现象类似于碳纳米管活化PS的过程.类似的过渡态也在CuO/PDS系统〔55〕、纳米碳/PS系统〔56〕中发现. ...
Occurrence of radical and nonradical pathways from carbocatalysts for aqueous and nonaqueous catalytic oxidation
1
2016
... Haoran Song等〔22〕在采用BDD阳极活化PS降解污染物的研究中,分别进行了自由基猝灭实验和自由基探针实验.结果表明,在BDD电极活化PS的过程中,阳极放电可以将吸附的PDS或PMS分子转化为特殊的过渡态结构,这种过渡结构具有非常强的活性,能够通过非自由基的形式降解污染物.在该研究中,BDD电极在没有施加电流的情况下并不能活化PS,说明本研究的活性物质均来自电活化过程而非电极中的碳材料活化.A. Farhat等〔54〕认为,这种非自由基氧化现象类似于碳纳米管活化PS的过程.类似的过渡态也在CuO/PDS系统〔55〕、纳米碳/PS系统〔56〕中发现. ...
Electrochemical activation of persulfate on BDD and DSA anodes: Electrolyte influence, kinetics and mechanisms in the degradation of bisphenol A
1
2020
... Lingjun Bu等〔19〕对BDD电极活化PS降解阿特拉津(ATZ)进行了研究,结果表明,在该体系中污染物的降解是·OH、SO4·-和非自由基共同作用的结果,但是对于非自由基的作用方式没有进行探讨.同时该研究还对不同阴离子的影响进行了对比,结果显示,H2PO4-、HCO3-和NO3-对污染物的降解均有抑制作用,且抑制效果为HCO3- > H2PO4- > NO3-.L. W.Matzek等〔38〕采用BDD电极分别在过硫酸盐和硫酸盐电解液中活化PS,结果表明,在过硫酸盐电解液中,阳极室的PS浓度并不随污染物的降解而变化,这表明PS在BDD阳极没有发生转化,污染物降解可能是因为阳极表面的直接氧化;而在硫酸盐电解液中,PS浓度随污染物的减少而缓慢增加,说明过硫酸盐会在BDD阳极再生.Jing Ding等〔57〕通过实验对比了BDD/PS体系和DSA/PS体系在降解双酚A上的差异,结果表明,在ClO4-电解液中,BDD/PS体系对污染物的降解效果远高于DSA/PS体系,污染物降解率分别可达到74%和35%;在SO42-溶液中,二者对污染物的的降解率都在50%左右,表明在该介质下BDD/PS体系受到抑制,这可能是由于BDD表面的活性位点有限,高浓度的SO42-(30 mmol/L)与低浓度的PS(1 mmol/L)出现竞争;在Cl-介质中,处理9 min后,BDD/PS体系和DSA/PS体系对污染物的降解率分别可达到100%和60%,完全高于单独电解的降解效果(BDD为88%、DSA为48%),这是由于Cl-和·OH/SO4·-反应产生了含氯自由基(Cl·-、ClO·-和Cl2·-),而它们与酚类化合物的反应比·OH、SO4·-更快,从而促进了污染物的降解.总体而言,BDD电极在活化PS中的表现要明显优于DSA电极. ...
Unraveling different mechanisms of persulfate activation by graphite felt anode and cathode to destruct contaminants of emerging concern
1
2019
... 除BDD电极外,也有研究采用其他碳材料电极活化PS降解有机污染物,并且取得了良好的效果.这些电极不但可以作为阳极还可以做阴极,但是作为阴极活化PS时与阳极的反应略有不同,除了在阴极上得电子外,还会有其他活性物质作为中间体参与活化(见式20、式21).Zhen Liu等〔39〕采用活性炭纤维(ACF)作为阴极活化PMS降解水中卡马西平,研究表明,在降解过程中活性物质起主要作用,占78.02%(其中·OH、SO4·-和1O2分别占29.27%、58.86%和11.87%),而非自由基氧化仅占1.36%.其中·OH和SO4·-在阴极与阳极均有产生,而1O2主要是通过阴极上·OH与PMS的反应生成(见式22).Lingjun Bu等〔58〕在研究中发现,由于S2O82-与石墨毡阴极之间的静电斥力,不太容易在阴极得电子产生SO4·-,通过自由基猝灭实验可知,在阴极产生的O2·-在阴极活化PS中扮演了重要的角色,其主要来源是电解产生的O2在阴极得电子形成. ...
Enhanced degradation of antibiotic sulfamethoxazole by electrochemical activation of PDS using carbon anodes
1
2018
... Haoran Song等〔59〕利用4种碳材料(多壁碳纳米管、石墨、黑炭和颗粒活性炭)作为阳极活化PDS降解磺胺甲恶唑(SMX),结果显示,4种材料电极均能活化PDS并降解污染物,其中石墨电极的活化降解效果最好;在该研究中污染物刚开始降解时存在一个诱导阶段,这个阶段持续的时间与电极材料有关,此阶段后污染物会迅速被降解,这个诱导阶段可能是由于碳材料的吸附性所形成;在该研究中阳极活化PS产生了·OH、SO4·-与一种过渡态的高活性过硫酸盐,过渡态的形成可能与电流激活吸附在电极表面过硫酸盐有关.此外,Haoran Song等〔60〕还研究了碳阳极(石墨、多壁碳纳米管)在活化PS中的作用,结果显示,在这个过程中没有发现初始诱导阶段的存在.在活化PMS中,SO4·-氧化占据主导,其贡献率在64.93%,并且没有发现·OH的作用;而在活化PDS体系中,非自由基氧化占据主导作用,其贡献率在95.79%.采用相同的电极材料活化PMS与PDS,2种体系的主要活性物存在较大区别,这可能与他们自身的分子结构有关.PDS的双氧键要比PMS更稳定一些,因此PMS体系更有可能产生SO4·-,而PDS体系在阳极形成的过渡态结构更容易发生非自由基氧化. ...
Electrochemically activated PMS and PDS: Radical oxidation versus nonradical oxidation
1
2020
... Haoran Song等〔59〕利用4种碳材料(多壁碳纳米管、石墨、黑炭和颗粒活性炭)作为阳极活化PDS降解磺胺甲恶唑(SMX),结果显示,4种材料电极均能活化PDS并降解污染物,其中石墨电极的活化降解效果最好;在该研究中污染物刚开始降解时存在一个诱导阶段,这个阶段持续的时间与电极材料有关,此阶段后污染物会迅速被降解,这个诱导阶段可能是由于碳材料的吸附性所形成;在该研究中阳极活化PS产生了·OH、SO4·-与一种过渡态的高活性过硫酸盐,过渡态的形成可能与电流激活吸附在电极表面过硫酸盐有关.此外,Haoran Song等〔60〕还研究了碳阳极(石墨、多壁碳纳米管)在活化PS中的作用,结果显示,在这个过程中没有发现初始诱导阶段的存在.在活化PMS中,SO4·-氧化占据主导,其贡献率在64.93%,并且没有发现·OH的作用;而在活化PDS体系中,非自由基氧化占据主导作用,其贡献率在95.79%.采用相同的电极材料活化PMS与PDS,2种体系的主要活性物存在较大区别,这可能与他们自身的分子结构有关.PDS的双氧键要比PMS更稳定一些,因此PMS体系更有可能产生SO4·-,而PDS体系在阳极形成的过渡态结构更容易发生非自由基氧化. ...



























 津公网安备 12010602120337号
津公网安备 12010602120337号