有机合成染料广泛应用于染料、造纸、纺织品和塑料等行业的生产中。由于有机合成染料一般具有毒性和难生物降解性,其产生的废水若不经处理直接排放,会对人类健康和生态环境带来严重威胁〔1〕。目前尽管有很多方法可用于去除废水中的染料,如凝聚〔1〕、电絮凝〔2〕、膜分离〔3〕、化学和电化学氧化〔4〕等,但相较于上述几种方法,吸附法因其易于实施、去除效率高、操作条件温和且能耗低,应用更为广泛〔5-6〕。工业上常用的吸附剂主要有活性炭〔7〕、沸石〔8〕、粉煤灰〔9〕、聚合物〔10〕和黏土矿物〔11〕等,这些吸附剂虽然具有很强的吸附能力,但仍存在一些缺陷,如吸附速率较慢、后处理复杂及选择性吸附能力较差等,难以得到大规模应用。因此,有必要开发新型吸附剂用以去除废水中的有机污染物。多孔金属氧化物由于具有比表面积高、扩散能力强和吸附性能优异等优势引起了研究者广泛的关注〔12〕。
1 实验部分
1.1 试剂与仪器
试剂:六水硫酸镍(NiSO4·6H2O)、尿素、无水乙醇、丁二酮肟、过硫酸铵、氢氧化钠和氧化镍,分析纯,国药集团化学试剂有限公司;镍标准溶液来自国家有色金属及电子材料分析测试中心。实验用水为去离子水。
仪器:D/Max-RB X射线衍射仪,日本Rigaku公司;S-4800型扫描电镜仪,日本Hitachi公司;ASAP 2020粉体氮吸附仪,美国麦克公司;IRAffinity-1型红外光谱仪、UV-2550紫外可见光谱仪,日本岛津公司。
1.2 吸附剂制备
向200 mL去离子水中加入0.48 mmol NiSO4·6H2O、0.96 mmol尿素,搅拌10 min,然后置于90 ℃恒温烘箱中反应48 h。取沉淀物,用去离子水及乙醇洗涤3次,然后于80 ℃下真空干燥6 h,再在300 ℃下以1 ℃/min的升温速度煅烧5 h,得到NiO样品。用购买的商业NiO试剂作为对比样品,记为NiO-C。
实验制备的NiO及对比样品NiO-C的相关参数如表 1所示。
表1 NiO与NiO-C的物理参数
| 样品 | 形貌 | 晶粒尺寸/nm | 孔体积/(cm3·g-1) | SeEr/(m2·g-1) |
| NiO | 花状微球 | 5.5 | 0.26 | 202 |
| NiO-C | 颗粒状 | 46.3 | 0.009 | 2.6 |
1.3 实验方法
将一定量的吸附剂加入到25 mL一定浓度的刚果红溶液中,搅拌反应一定时间。取样,在4 000 r/min下离心后,取上清液用紫外可见光谱仪在最大吸收波长(497 nm)处测定刚果红含量。以NiO-C作吸附剂进行对比实验。所有实验均在常温、pH为7的条件下进行。
1.4 镍离子溶出实验
将50 mg吸附剂分别加入到25 mL去离子水和刚果红溶液中,搅拌反应一定时间,然后取10 mL上层清液进行镍离子浓度测试。取样后分别补充10 mL去离子水或刚果红溶液,以保持固液比不变。镍离子浓度采用丁二酮肟分光光度法进行测定。
2 结果与讨论
2.1 XRD表征
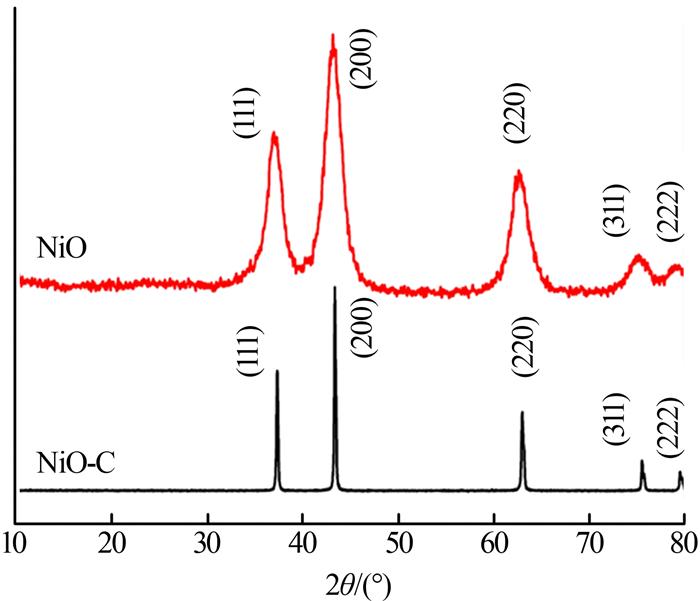
NiO与NiO-C的XRD表征结果如图 1所示。
图1
由图 1可见,NiO和NiO-C均在37.2°、43.3°、62.9°、75.4°和79.4°处出现衍射峰,分别对应(111)、(200)、(220)、(311)和(222)晶面,与立方相的NiO衍射谱(标准卡片JCPDS 71-1179)一致。表明实验制备的NiO具有立方晶系结构,且没有其他杂质相存在,为晶化较好的单相NiO晶体。而NiO-C对应的衍射峰强度较大,半峰宽较窄,说明其晶粒尺寸较大,Scherrer公式计算为46.3 nm。
2.2 SEM分析
NiO和NiO-C的SEM表征结果如图 2所示。
图2
2.3 N2吸附研究
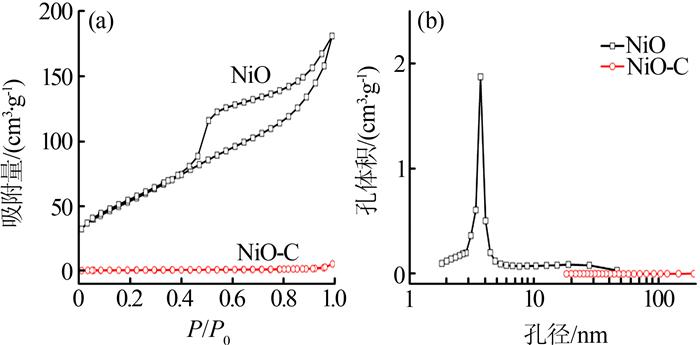
图 3为NiO和NiO-C的N2吸附脱附等温线及对应的孔径分布曲线。
图3
由图 3可见,NiO和NiO-C的N2吸附脱附等温线均为Ⅳ型。相对压力范围较高(0.9<P/P0<1)时,曲线有1个大的滞后环,表明存在很多介孔(2~ 50 nm)。由IUPAC分类可知,该滞后环为H3型,即介孔为典型狭缝状孔。该表征结果与SEM表征一致。
NiO的孔径分布为单峰分布,其最大孔容的孔径分布峰在4.0 nm处,介孔来自花状NiO微球中纳米片间形成的孔。NiO-C的最大孔径分布峰约在60 nm处,其大孔来自NiO-C中较大颗粒形成的孔。NiO和NiO-C的BET比表面积分别为202、2.6 m2/g,说明所制备的分等级花状NiO微球具有很大的比表面积。
2.4 吸附动力学
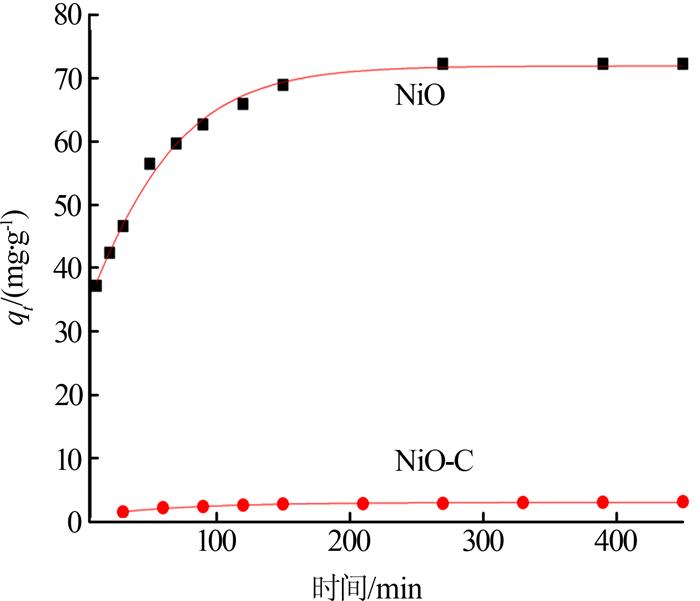
在刚果红初始质量浓度为25 mg/L的条件下进行吸附动力学实验,结果如图 4所示。
图4
表2 NiO及NiO-C的吸附动力学参数
| 样品 | qe(exp)/(mg·g-1) | 准一级动力学方程 | 准二级动力学方程 | |||||
| qe(cal)/(mg·g-1) | K1/10-3min-1 | R2 | qe(cal)/(mg·g-1) | K2/10-4·mg-1·min-1 | R2 | |||
| NiO | 81.3 | 44.2 | 3.92 | 0.984 8 | 89.7 | 3.68 | 0.997 5 | |
| NiO-C | 3.2 | 1.6 | 3.73 | 0.988 0 | 3.4 | 9.72 | 0.999 9 | |
由表 2可以看出,吸附剂对刚果红的吸附过程更加符合准二级动力学方程。NiO吸附刚果红过程主要是依赖吸附剂与吸附质之间的相互作用,限速步骤可能为化学吸附过程。
2.5 吸附等温线
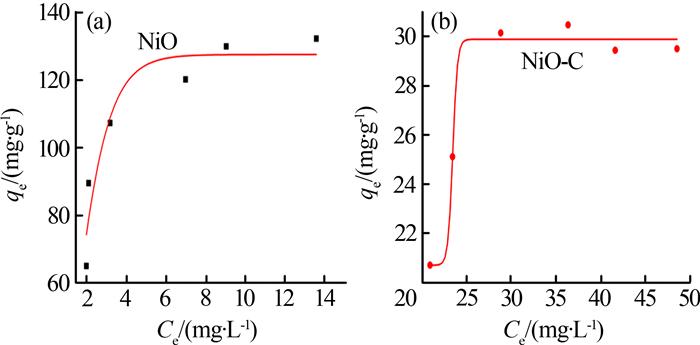
在初始刚果红质量浓度分别为25、30、35、40、45、50 mg/L,吸附时间为450 min的条件下进行等温吸附实验,结果如图 5所示。
图5
采用Langmuir、Freundlich模型对实验数据进行拟合,结果如表 3所示。
表3 NiO和NiO-C的吸附等温曲线拟合参数
| 样品 | Langmuir等温线模型 | Freundlich等温线模型 | ||||||
| qmax/(mg·g-l) | K1/(L·g-l) | R2 | RL | KF | n | R2 | ||
| NiO | 155.9 | 0.55 | 0.950 | 0.035 | 65.7 | 3.39 | 0.884 | |
| NiO-C | 38.5 | 0.07 | 0.947 | 0.22 | 7.9 | 2.51 | 0.789 | |
由表 3可见,与Freundlich模型相比,Langmuir表 3 NiO和NiO-C的吸附等温曲线拟合参数模型对NiO微球吸附刚果红有较好的适用性。NiO和NiO-C对刚果红的最大吸附量分别为155.9、38.5 mg/g,分等级花状NiO微球的吸附能力明显比NiO-C要好。
2.6 选择吸附性能
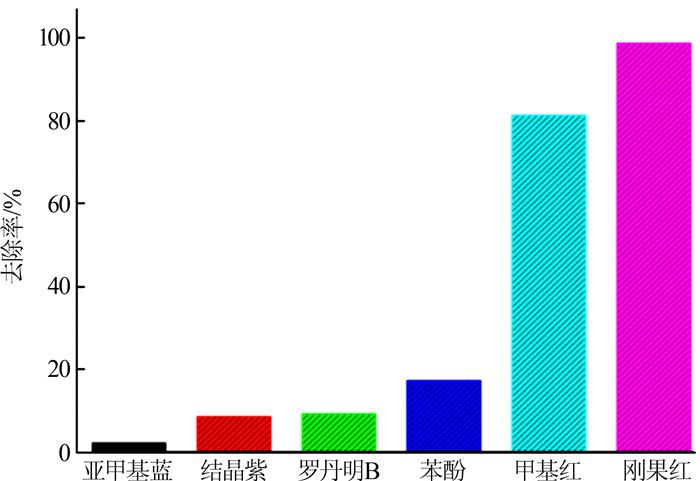
为考察所制备花状磁性NiO微球的选择吸附性能,选择不同的污染物(25 mL 50 mg/L亚甲基蓝、25 mL 50 mg/L结晶紫、25 mL 50 mg/L罗丹明B、25 mL 0.001 mol/L苯酚、25 mL 50 mg/L甲基红和25 mL 50 mg/L刚果红)进行吸附实验,吸附时间为450 min,结果如图 6所示。
图6
2.7 IR分析
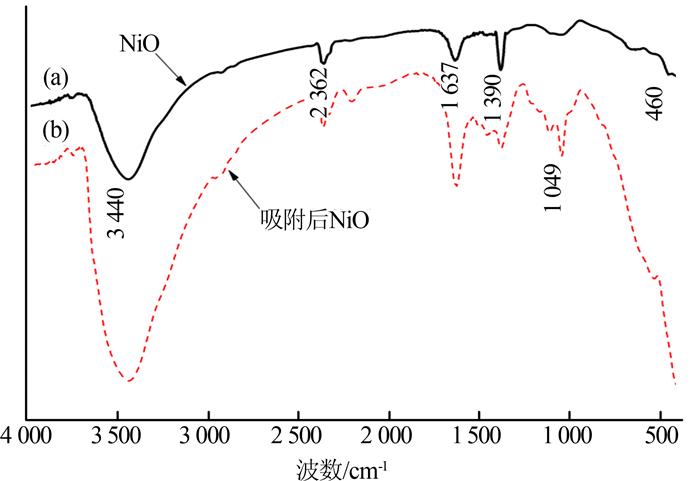
吸附刚果红前后的NiO的IR表征结果见图 7。
图7
2.8 磁性研究
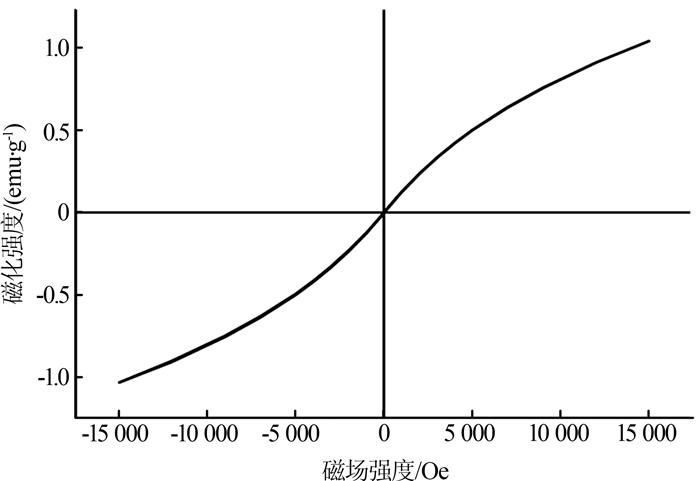
室温下测得的NiO的磁滞回线曲线如图 8所示。
图8
2.9 吸附机理研究
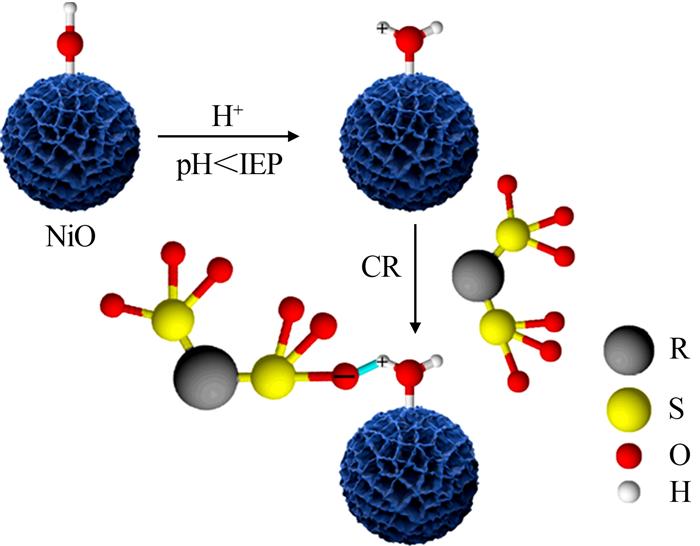
刚果红在分等级花状磁性NiO表面的吸附机理为静电吸附,如图 9所示。其中R代表除-SO3-基团外的刚果红分子。花状磁性NiO微球分散在水性悬浮液中时,其表面存在大量羟基(-OH),其可发生质子化和去质子化。当溶液pH低于等电点时,表面羟基易质子化,从而使NiO表面带有正电荷。因此,刚果红带负电荷的-SO3-会通过静电相互作用被吸引到带正电荷的花状磁性NiO微球表面。
图9
2.10 镍离子溶出浓度
分等级花状磁性NiO微球表现出优异的吸附性能,而NiO微球进入环境水体后,其表面裸露的镍原子有可能会溶出到环境水体中。为避免造成二次污染,有必要对吸附剂在水体中溶出镍离子的浓度进行评价。在固液比为2 g/L的条件下,应用丁二酮肟分光光度法测定磁性NiO微球及购买的商业NiO试剂分别在去离子水和质量浓度为35 mg/L的刚果红溶液中的镍离子溶出浓度,结果如表 4所示。
表4 NiO和NiO-C在去离子水和刚果红溶液中的镍离子溶出浓度
| 样品 | 溶剂 | 镍离子溶出质量浓度/(mg·L-1) | ||
| 搅拌12h | 搅拌24h | 搅拌48h | ||
| NiO | 去离子水 | 0.092 | 0.15 | 0.16 |
| NiO | 刚果红溶液 | 0.088 | 0.13 | 0.14 |
| NiO-C | 去离子水 | 0.006 3 | 0.007 0 | 0.006 8 |
| NiO-C | 刚果红溶液 | 0.005 8 | 0.006 9 | 0.006 1 |
3 结论
以硫酸镍为镍源,通过简单溶液法制备得到分等级花状磁性NiO微球。该NiO微球具有分等级多孔结构和相对较大直径(约2 μm),对刚果红的吸附性能较好,可通过磁铁快速从溶液中分离回收,并对阴离子染料具有选择吸附性能,是去除废水中阴离子染料污染物的理想吸附剂。花状磁性NiO微球对刚果红的吸附过程符合准二级动力学方程;Langmuir等温线模型能很好地描述NiO微球对刚果红的吸附,其最大吸附量达155.9 mg/g。上述结果说明,该材料在实际应用中有较好的前景。
参考文献
Porous carbon with small mesoporesas an ultra-high capacity adsorption medium
[J].DOI:10.1016/j.apsusc.2017.05.112 [本文引用: 2]
Decolorization of basic dye solutions by electrocoagulation: An investigation of the effect of operational parameters
[J].DOI:10.1016/j.jhazmat.2005.08.033 [本文引用: 1]
Polymeric nanofiltration membranes for textile dye wastewater treatment: Preparation, performance evaluation, transport modelling, and fouling control-A review
[J].
A comparative study on oxidation of disperse dyes by electrochemical process, ozone, hypochlorite and fenton reagent
[J].DOI:10.1016/S0043-1354(00)00487-5 [本文引用: 1]
A simple fabrication for sulfur doped graphitic carbon nitride porous rods with excellent photocatalytic activity degrading RhB dye
[J].
Superb adsorption capacity of hierarchical calcined Ni/Mg/Al layered double hydroxides for Congo red and Cr(Ⅵ) ions
[J].DOI:10.1016/j.jhazmat.2016.09.070 [本文引用: 1]
Effect of solution pH, ionic strength, and temperature on adsorption behavior of reactive dyes on activated carbon
[J].DOI:10.1016/j.dyepig.2007.03.001 [本文引用: 1]
Application of MCM-41 for dyes removal from wastewater
[J].DOI:10.1016/j.jhazmat.2007.01.130 [本文引用: 1]
Removal of dyes from aqueous solution using fly ash and red mud
[J].DOI:10.1016/j.watres.2004.09.011 [本文引用: 1]
Ammonium-functionalized hollow polymer particles as a pH-responsive adsorbent for selective removal of acid dye
[J].
Kinetic study and equilibrium isotherm analysis of Congo Red adsorption by clay materials
[J].
Synthesis of mesoporous NiO nanoparticles and their application in the adsorption of Cr(Ⅵ)
[J].DOI:10.1016/j.cej.2013.10.102 [本文引用: 1]
Self-assembled hierarchical 3D-NiO microspheres with ultra-thin porous nanoflakes for lithiumion batteries
[J].DOI:10.1016/j.jpowsour.2015.10.044 [本文引用: 1]
Lotus pollen derived 3-dimensional hierarchically porous NiO microspheres for NO2 gas sensing
[J].DOI:10.1016/j.snb.2015.12.104 [本文引用: 1]
Ultrathin mesoporous NiO nanosheet-anchored 3D nickel foam as an advanced electrode for supercapacitors
[J].DOI:10.1039/C5TA05313G [本文引用: 1]
Facile synthesis of unique NiO nanostructures for efficiently catalytic conversion of CH4 at low temperature
[J].DOI:10.1016/j.apsusc.2015.11.213 [本文引用: 1]
The isoelectric points of solid oxides, solid hydroxides, and aqueous hydroxo complex systems
[J].DOI:10.1021/cr60234a002 [本文引用: 2]
磁性纳米吸附剂制备及在水处理中的应用研究进展
[J].DOI:10.11894/iwt.2019-0391 [本文引用: 1]
The adsorption of gases on plane surfaces of glass, mica and platinum
[J].DOI:10.1021/ja02242a004 [本文引用: 1]
Preparation of mesoporous nickel oxide of sheet particles and its characterization
[J].DOI:10.1016/j.matchemphys.2008.08.066 [本文引用: 1]
Adsorption properties of Congo red from aqueous solution onto surfactant-modified montmorillonite
[J].DOI:10.1016/j.jhazmat.2008.02.104 [本文引用: 1]
Nanoparticles Ni and NiO: Synthesis, characterization and magnetic properties
[J].DOI:10.1016/j.jallcom.2008.09.121 [本文引用: 1]






 津公网安备 12010602120337号
津公网安备 12010602120337号