脂环胺是一种非芳香族胺类化合物,其环烷烃上含有一个氮原子。脂环胺作为试剂或前体化合物被广泛应用于工业化学品生产中,如燃料、杀虫剂、橡胶和食品等〔1〕。脂环胺很容易随工业废水直接或间接排放到环境中,导致环境污染以及危害人类健康〔2-3〕。因此研究者们开发了多种方法用于降解废水中的脂环胺。常见的方法有电化学降解〔4〕、化学氧化降解〔5〕、光催化氧化降解〔6〕和热脱附降解〔7〕。近年来,光催化产氢同时伴随有机胺降解的方法也相继被报道〔8〕。然而,传统物化方法降解脂环胺具有投资大、程序复杂和产生二次污染的局限性。而生物降解作为一种可靠的方法,具有成本低、实际可行和环境友好的优点,逐渐成为废水处理领域的研究热点〔9〕。1999年H. IWAKI等首次从土壤中分离出1株革兰氏阳性菌Brevibacterium oxydans IH-35A,对环己胺具有高效的降解能力〔10〕。近十几年,陆续又有革兰氏阴性菌(Pseudomonas plecoglossicida NyZ12〔11〕,Aci-netobacter sp. YT-02〔12〕)和革兰氏阳性菌(Pseudox-anthomonas sp. YT-01〔13〕)被从土壤中分离出来,均对环己胺具有良好的降解效果。工业废水中除了脂环胺外,高浓度盐通常也是其主要成分。据估计,世界上5%的工业废水是盐水或高盐水〔14〕,生物法处理此类废水仍存在一定的难度。耐盐微生物在代谢生长过程中因需要摄入盐(NaCl),在处理高盐工业废水中表现出极大的发展潜力〔15〕。目前,高盐环境下主要报道了微生物降解芳香酸、烷烃、氯代烃、多环芳烃和苯酚等有机污染物〔16〕,对脂环胺降解的报道却很少。
笔者通过富集培养,从土壤环境中首次筛选到1株耐盐环己胺降解菌。通过16S rDNA测序对该菌株进行了菌种鉴定。对影响菌株生长和环己胺去除的外在因素(如pH、温度、盐浓度、环己胺浓度)进行了考察。同时,在高盐条件下,对不同胺类化合物的去除效果进行了研究。
1 材料与方法
1.1 实验材料
筛选环己胺降解菌所用土壤样品来自太原理工大学明向校区周边。苯胺、苯甲胺、苯已胺、环戊胺、环己胺、环庚胺、苯乙胺、反式-2-氨基环己醇、N-甲基环己胺、环己醇、环己酮、环己内酯,购于上海阿拉丁生化科技股份有限公司;其他化学品和有机试剂为分析纯并可商业获得。Ezup柱式细菌基因组DNA抽提试剂盒和PCR所用的分子试剂购自上海生工生物工程股份有限公司,引物合成以及基因测序通过上海生物工程股份有限公司完成。
基本盐培养基(BSM)配方:1.0 g NH4NO3,0.5 g KH2PO4,5.24 g K2HPO4·3H2O,0.2 g MgSO4·7H2O,2.0 mL质量分数1%的CaCl2,200 μL质量分数5%的NaCl,200 μL质量分数1%的FeCl3,5.0 mL质量分数1%的酵母提取物,5.0 mL微量元素溶液,加蒸馏水至1 000 mL,调节pH为7.0,121 ℃灭菌20 min。调整后的基本盐培养基(MBSM)配方:在BSM基础上,加入1%~7%(质量分数,下同)的NaCl和10~50 mmol/L环己胺盐酸盐。
1.2 实验方法
1.2.1 耐盐环己胺降解菌株的富集与分离
初筛:称取5.0 g土壤样品于50.0 mL MBSM培养基中(含10 mmol/L环己胺和1% NaCl),于30 ℃、150 r/min的摇床中培养7 d。移取1.0 mL富集液于新鲜MBSM培养基中(含20 mmol/L环己胺和1% NaCl),富集培养7 d。连续富集培养3次后,通过稀释涂布平板法进行初筛,将1 mL富集液稀释后,取0.1 mL涂布于含有10 mmol/L环己胺和1% NaCl的MBSM固体培养基上,于30 ℃下培养24~48 h后挑取单菌落进行下一步复筛。
复筛:将初筛得到的菌落种子液分别接种于含有20 mmol/L环己胺和1% NaCl的5.0 mL MBSM培养基中,于30 ℃、150 r/min的摇床中培养24 h,考察初筛菌落对环己胺的去除率,筛选去除率高于50%的优势菌落。
1.2.2 菌种鉴定
菌株的基因组DNA使用Ezup柱式细菌基因组DNA抽提试剂盒进行抽提,通过细菌16S rDNA通用引物(上游引物27F:5’-AGAGTTTGATCCTGGC- TCAG-3’和下游引物1492R:5’-GGTTACCTTGTT- ACGACTT-3’)进行PCR扩增。PCR反应体系:5.0 μL 10×Taq缓冲液、1.0 μL上下游引物、1.0 μL模板DNA、1.0 μL dNTP和1.0 μL DNA聚合酶,最后加40.0 μL无菌水补足至50 μL。PCR反应条件为:95 ℃预变性5 min,95 ℃变性30 s、55 ℃退火30 s、72 ℃引物延伸1.5 min循环30次,72 ℃延伸10 min。PCR产物用质量分数1%的琼脂糖凝胶进行电泳分析,染色后用凝胶成像仪查看PCR结果。最后将PCR纯化产物送至上海生工生物工程股份有限公司进行测序,将测序产物在NCBI基因文库中进行序列比对与登记。
1.2.3 影响菌株生长及环己胺去除的因素
将培养24 h的菌株种子液于10 000 r/min下离心15 min,用0.85%的NaCl溶液冲洗细胞2次以洗去残余碳源,然后用BSM培养基将细胞制成OD600=1.0的细胞悬液。分析不同因素(培养基pH、温度、环己胺浓度、NaCl浓度)对菌株生长及环己胺去除率的影响。
(1)pH的影响。取1.0 mL细胞悬液接种于含有20 mmol/L环己胺和1% NaCl的50 mL MBSM培养基中,通过酸碱调节pH在4.0~10.0,在30 ℃、200 r/min的摇床中培养72 h后,检测环己胺浓度和微生物生长。
(2)温度的影响。取1.0 mL细胞悬液接种于含有20 mmol/L环己胺和1% NaCl的50 mL MBSM培养基(pH=7.0)中,在不同温度(20~45 ℃)的摇床上、200 r/min培养48 h后,检测环己胺浓度和微生物生长。
(3)环己胺浓度的影响。取1.0 mL细胞悬液接种于含有10~50 mmol/L环己胺和1% NaCl的50 mL MBSM培养基(pH=7.0)中,在30 ℃、200 r/min的摇床中培养48 h后,检测环己胺浓度和微生物生长。
(4)NaCl浓度。取1.0 mL细胞悬液接种于含有10 mmol/L环己胺和1%~7% NaCl的50 mL MBSM培养基(pH=7.0)中,在30 ℃、200 r/min的摇床中培养72~120 h后,在不同时间取样,检测环己胺浓度和微生物生长。
1.2.4 菌株对不同碳源的去除
移取1.0 mL菌株种子液(OD600=1.0)于含有10 mmol/L不同类型碳源(苯胺、苄胺、苯乙胺、环戊胺、环己胺、环庚胺、α-甲基苄胺、反式-2-氨基环己醇、N-甲基环己胺、环己醇、环己酮、环己内酯、己二酸)和1% NaCl的50 mL MBSM培养基中(pH=7.0),在30 ℃、200 r/min的摇床中培养72 h,检测不同碳源浓度和微生物生长。
1.2.5 分析方法
取0.5 mL 1.2.3和1.2.4章节最终培养液,12 000 r/min离心5 min,加入10 μL 10 mol/L NaOH溶液使样品pH > 10.0,NaCl饱和后,加入0.5 mL乙酸乙酯(含有20 mmol/L十二烷作为内标)对样品进行萃取,12 000 r/min离心5 min,乙酸乙酯相加入无水硫酸钠进行干燥后,气相色谱检测不同类型碳源浓度。微生物的生长通过紫外分光光度计(岛津UV-1900)在波长600 nm下进行检测。
气相色谱检测方法为:HP-5柱(D 30 m× 0.320 mm×0.25 μm;Agilent Technologies,lnc.),进样口温度250 ℃;检测器温度250 ℃;柱温120 ℃。
2 结果与讨论
2.1 耐盐脂环胺降解菌的富集和分离
按1.2.1进行了菌株的筛选,最终获得6株耐盐环己胺降解菌株,对环己胺的去除率都在60%以上,其中菌株TYUT105具有最高的环己胺去除能力以及在MBSM培养基中最快的生长速率,48 h内就可完全去除20 mmol/L的环己胺(去除率100%),同时,OD600可以达到3.0。因此,菌株TYUT105被选为最终研究对象,进行下一步实验研究。16S rDNA测序结果表明,其与蜡样芽孢杆菌属(Bacillus cereus strain GO-ACSMMS11)的一致性高达98.2%,初步认定此株菌为蜡样芽孢杆菌属,并命名为Bacillus cereus TYUT105。
2.2 菌株TYUT105生长曲线以及对环己胺的降解
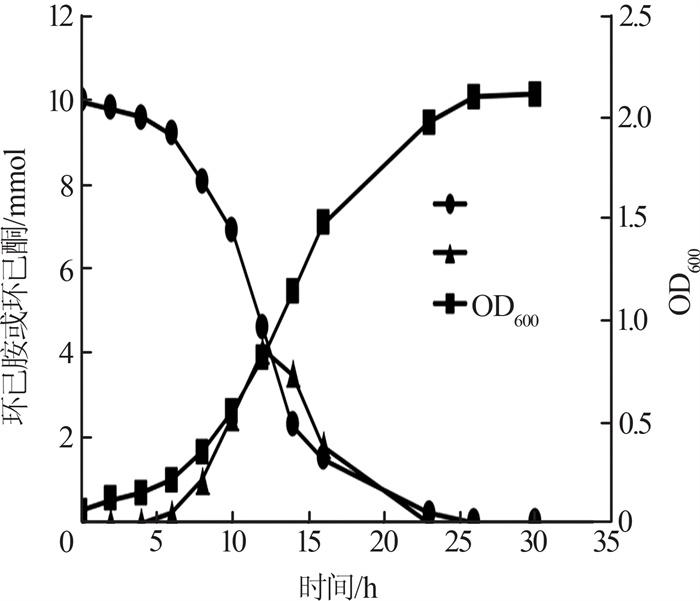
考察了菌株TYUT105在含有10 mmol/L环己胺和1% NaCl的MBSM培养基中的生长趋势以及对环己胺的去除情况,如图 1所示。在温度30 ℃,pH=7.0条件下,菌株TYUT105的生长呈典型的S型生长曲线,前6 h菌株生长较慢,处于延滞期状态,从第6 h开始,菌株进入对数生长期,直到第24 h,菌株生长开始减缓,进入稳定生长期和衰亡期。对环己胺的去除,前6 h去除较慢,从第6小时至第16小时,环己胺被快速去除,第26小时时,环己胺被完全去除。而环己胺的去除过程中有环己酮的生成,到第12小时时,环己酮的量达到最高,之后被迅速降解。由此可初步推测TYUT105菌降解环己胺是经过环己酮中间途径降解。
图1
图1
菌株TYUT105生长曲线以及对环己胺的去除过程
Fig.1
The time curve of cell growth of TYUT105 and CHAM degradation
2.3 TYUT105去除环己胺的影响因素
2.3.1 pH
考察了菌株TYUT105在不同pH条件下的生长状况以及对环己胺的去除情况,结果如图 2所示。该菌在pH为6.0~9.0范围内生长良好,最佳生长pH为7.0。当pH低于6.0,该菌在MSBM培养基中基本不生长;当pH为10.0时,该菌在MSBM培养基中生长较缓慢。在pH为6.0~9.0范围内,该菌对环己胺的去除率高于80%。
图2
图2
pH对菌株生长以及环己胺去除的影响
Fig.2
The effect of pH on the cell growth and CHAM degradation
2.3.2 温度
考察了菌株在不同温度下的生长状况以及对环己胺的去除情况,如图 3所示。该菌在温度为20~35 ℃范围内生长良好,最佳的生长温度为30 ℃。当温度高于35 ℃,该菌在含环己胺的MSBM培养基中基本不生长。在20~35 ℃范围内,环己胺的去除率在70%以上。而温度高于35 ℃,环己胺的去除率低于10%。
图3
图3
温度对菌株生长及环己胺去除的影响
Fig.3
The effect of temperature on the cell growth and CHAM degradation
2.3.3 环己胺浓度
图4
图4
环已胺浓度对环已胺去除的影响
Fig.4
The effect of concentration of CHAM on CHAM degradation
2.3.4 NaCl浓度
对该菌株的耐盐性进行了考察,将菌株分别接种至含有10 mmol/L环己胺以及3%~7% NaCl的MBSM培养基中,在不同时间取样,检测环己胺的去除情况以及菌株的生长情况,如图 5所示。
图5
图5
NaCl含量对菌株生长以及环己胺去除的影响
Fig.5
The effect of concentrations of NaCl on CHAM degradation
菌株TYUT105可在含有3%和5% NaCl的培养基中正常生长,在含有3% NaCl的培养基中,前10 h菌株生长处于延滞期,之后进入对数生长期,一直到28 h,菌株生长进入到稳定期;而在含有5% NaCl的培养基中,菌株生长明显变慢,前12 h处于延滞期,之后进入到对数生长期,一直到60 h菌株进入稳定期;当NaCl质量分数增加至7%时,菌株基本停止生长。对环己胺降解方面,3% NaCl存在下,完全去除10 mmol/L的环己胺需要36 h;而在5% NaCl存在下,完全去除10 mmol/L的环己胺需要72 h。该菌株能在含有5% NaCl的培养基中生长并能完全去除环己胺,说明该菌是1株可耐受高盐浓度的菌株。据报道,质量分数高于1%的NaCl溶液被称为盐水,而高于3.5%可被称为高盐水〔17〕。
2.4 菌株对不同底物的去除
进一步考察了菌株TYUT105对10 mmol/L不同有机胺类化合物的去除情况,如图 6所示。
图6
该菌株对脂环胺类化合物具有良好的去除性能,培养48 h,可将环戊胺、环己胺、环庚胺和反式-2-氨基环己醇完全去除。对N-甲基环己胺的去除率也达到80%。而对其他胺类化合物(如苯胺、苄胺、苯乙胺、α-甲基苄胺)的去除率明显下降,去除率低于30%。进一步检测了该菌株对环己醇、环己酮、环己内酯和己二酸的去除情况。该菌株可完全去除环己醇、环己酮和环己内酯,但无法在己二酸中生长。由此可推断该菌株降解环己胺的途径为:首先通过脱胺酶将环己胺转化为环己酮,然后环己酮被单加氧酶氧化为环己内酯。这与之前报道的环己胺降解菌株Pseudoxanthomonas sp. YT-01代谢途径非常类似〔13〕,而与环己胺降解菌株Brevibacterium oxydans IH-35A的代谢途径有所不同〔10〕,其代谢途径不经过己二酸。而环己醇能被降解,说明该菌株可能含有1种环己醇脱氢酶可将环己醇氧化为环己酮,而环己酮可被菌株进一步代谢。
3 结论
(1)从土壤中筛选、分离、纯化出1株耐盐脂环胺降解菌TYUT105,通过16S rDNA测序比对鉴定出该菌为蜡样芽孢杆菌(Bacillus cereus)。
(2)TYUT105在pH为6.0~9.0、温度为20~35 ℃范围内生长良好。TYUT105可在48 h内完全去除10~20 mmol/L环己胺,120 h内完全去除50 mmol/L环己胺,在环己胺降解过程中可检测到环己酮的生成,环己酮被菌株迅速降解。
(4)TYUT105可在含质量分数5%的NaCl的MBSM培养基中生长,并完全去除环己胺,证明该菌为1株耐盐菌株。
(5)TYUT105可完全去除不同类型的脂环胺,对其他有机胺去除效果差。对环己酮和环己内酯的降解可初步推断该菌株对环己胺的代谢途径为环己胺→环己酮→环己内酯。相关的代谢途径还需通过对相关酶的研究以及分子克隆进一步证明。
参考文献
Long term toxicity and reproduction study (including a teratogenicity study) with cyclamate, saccharin and cyclohexylamine
[J].DOI:10.1016/0300-483X(77)90100-7 [本文引用: 1]
Bladder tumors in rats fed cyclohexylamine or high goses of a mixture of cyclamate and saccharin
[J].DOI:10.1126/science.167.3921.1131 [本文引用: 1]
Chemical degradation of aromatic amines by Fenton's reagent
[J].DOI:10.1016/S0043-1354(96)00344-2 [本文引用: 1]
Photocatalytic processes with polyoxotungstates: Oxidation of cyclohexylamine
[J].DOI:10.1021/ic00091a041 [本文引用: 1]
Thermal desorption-degradation of cyclohexylamine over Ni2+- and Al3+-exchanged bentonite studied using evolved gas analysis(TG-EGA) and diffuse refle ctance spectroscopy (DRIFTS)
[J].DOI:10.1039/b003587o [本文引用: 1]
Photocatalytic hydrogen production by RGO/ZnIn2S4 under visible light with simultaneous organic amine degradation
[J].DOI:10.1021/acsomega.9b01034 [本文引用: 1]
Minimization of excess sludge production for biological wastewater treatment
[J].DOI:10.1016/S0043-1354(03)00441-X [本文引用: 1]
Biodegradation of cyclohexylamine by Brevibacterium oxydans IH-35A
[J].DOI:10.1128/AEM.65.5.2232-2234.1999 [本文引用: 2]
Degradation of cyclohexylamine by a new isolate of Pseudomonas plecoglossicida
[J].DOI:10.1007/s11274-007-9651-9 [本文引用: 1]
Draft genome sequence of cyclohexylamine-degrading strain Acinetobacter sp.YT-02 isolated
[J].DOI:10.1007/s00284-017-1377-9 [本文引用: 1]
Biodegradation of organic pollutants by halophilic bacteria and archaea
[J].
Biotechnological applications and potentialities of halophilic microorganisms
[J].DOI:10.1007/BF00339138 [本文引用: 1]
Biodegradation and bioremediation of hydrocarbons in extreme environments
[J].
Treatment of organic pollution in industrial saline wastewater: A literature review
[J].DOI:10.1016/j.watres.2006.08.027 [本文引用: 1]










 津公网安备 12010602120337号
津公网安备 12010602120337号