在铅的冶炼过程中,需要使用铝粉置换镉预排液:水和含镉铅的冶炼烟灰按比例混合,浸出一定时间后经压滤机压滤,压滤后的液体在除杂罐中经高锰酸钾、少量铝粉去除杂质后再经压滤机压滤,得到硫酸镉液体,之后在置换罐中用铝粉置换提取海绵镉。提取海绵镉后的废液中含有Zn2+、Cd2+、Al3+、Fe3+等金属离子,成分复杂,若外排会对环境和人体造成严重的污染和危害〔1〕。笔者针对该废水,将不同的处理技术组合应用,在处理该废水的同时,对其中的金属进行资源化回收。
1 试验材料及方法
1.1 实验原料及仪器
废水取自当地某铅冶炼企业,废水pH为2.81,主要成分包括(mg/L):Al3+ 12 020、Zn2+ 17 500、Cd2+ 3 130、Fe2+ 498、Fe3+ 26、Cu2+ 0.07、Ni2+ 0.55、Pb2+ 2.56。将企业的废水母液真空抽滤(中速定量滤纸,孔径30~50 μm,直径9 cm,下同),过滤掉不溶性杂质,得到的滤液即作为本实验的反应原液。
主要试剂:硫酸铵(99%,天津科密欧化学试剂有限公司),氨水(25%~28%,上海阿拉丁生化科技股份有限公司),浓硫酸(98%,洛阳市昊华化学试剂有限公司),均为分析纯;P204〔二(2-乙基己基)磷酸酯,99%,郑州合成新材料科技有限公司〕。本实验采用电导率小于10 μS/cm的蒸馏水。
主要仪器:DFY型恒温结晶装置(巩义市京华仪器有限公司);MYP2011-50型电动搅拌器(上海梅颖浦仪器仪表制造有限公司);雷磁pHS-3C型pH计(上海仪电科学仪器股份有限公司);X-射线衍射仪(荷兰帕纳科公司);AA-7050型原子吸收分光光度计(北京东西分析仪器有限公司);ICPE- 9820型电感耦合等离子体发射光谱仪(岛津公司)。
1.2 实验流程
实验通过降温结晶-化学沉淀-溶剂萃取的方法对工厂实际废水中的金属进行分离和回收,以期实现资源的循环利用。实验工艺流程见图 1。
图1
该废水中的主要金属离子有Zn2+、Cd2+、Al3+、Fe3+、Fe2+等。首先,利用废水中的Al3+,通过降温结晶的方法制备得到铵明矾(硫酸铝铵);之后,采用H2O2将Fe2+氧化为Fe3+,再采用化学沉淀的方法回收废水中剩余的Al3+、Fe3+,得到铝和铁的氢氧化物;最后,通过P204萃取剂分离Zn2+、Cd2+。整个实验流程中只引入了NH4+,最后废水中的主要成分为(NH4)2SO4,便于回用处理。过程中所有的实验,包括结晶、沉淀和溶剂萃取,均做了3组平行实验,结果取平均值,以确保工艺流程的可靠性。
1.3 试验方法
1.3.1 铝的分离及回收
取200 mL废水原液置于烧杯中,水浴加热至60 ℃,搅拌的同时按照化学计量比加入硫酸铵,待其完全溶解后将其置于低温(5 ℃)水浴槽中冷却,该温度下硫酸铝铵的溶解度为3.3 g。
反应到达预定时间2 h后,快速抽滤分离晶体,用无水乙醇洗涤数次,置于干燥器中干燥,称量总重。对固体产品进行化学分析,测定滤液中的铝浓度,计算去除率。
1.3.2 剩余铝铁的去除
降温结晶除掉了废水中大部分铝,还需将剩余铝铁去除。降温结晶后废水的pH为3.2左右,加入H2O2将废水中的Fe2+完全氧化为Fe3+。随后,采用加入氨水调节pH的方法去除剩余铝铁,产生的沉淀为Al(OH)3、Fe(OH)3的混合物,过滤后将其干燥,回收后用来制备无机絮凝剂聚合硫酸铝铁(PFAS)。
1.3.3 锌和镉的萃取分离
采用工业常用的有机磷酸类萃取剂P204从前处理的废水中选择性回收锌。用磺化煤油作稀释剂降低有机相的黏度。在萃取步骤前,为了维持水相pH在一定范围内,需使用氨水皂化有机相来提高萃取效率。萃取后,萃取液用一定浓度的硫酸进行反萃,得到高纯度的ZnSO4溶液。Cd2+留在萃余液中,通过沉淀法收集。实验探究了皂化率、O/A比(有机相/水相)、萃取混合时间、萃取剂浓度等因素对分离效果的影响。
1.4 分析检测方法
2 结果与讨论
2.1 化学沉淀实验
通过实验考察了293 K温度下Zn2+、Al3+、Cd2+、Fe3+和Fe2+浓度和pH的溶解度平衡关系,结果表明,水溶液中的Cd2+、Fe2+和Zn2+在pH为6.5~9.0左右发生共沉淀。采用NaOH溶液调节废水原液pH,探究了溶液中不同金属离子的沉淀特性,结果见图 2。
图2
图2
废水原液金属离子质量浓度与pH的关系
Fig.2
The relationship between the metal ion concentration of wastewater and pH
当初始pH为1.0~3.5时,铁的质量浓度从525 mg/L降至485 mg/L,主要为Fe3+的沉淀;在pH为4.0~7.0时,铁质量浓度变化不大;当pH达到7.0以上,铁质量浓度迅速降低;当pH达到9.0以上,铁几乎全部沉淀,pH>7主要为Fe2+的沉淀。Al3+在pH>5时沉淀完全。废水样品中铁和铝沉淀的实验pH范围与理论范围相似。当pH > 3.5时,Zn2+开始沉淀,pH在4.0~7.0时,Zn2+的质量浓度从16 200 mg/L降至10 mg/L,与理论值相差较大,原因可能是因为废水中Zn2+、Al3+的质量浓度较高,Al3+沉淀形成较快,部分Zn2+或母液被包埋在其中,发生共沉淀导致Zn2+浓度降低。Cd2+的质量浓度在pH为1.0~5.0范围时变化不大,在pH > 5.5时开始沉淀,并在pH > 7.0时完全沉淀,与理论值差异较大,这是因为高浓度的Zn2+在沉淀的同时,夹带了部分Cd2+。上述结果表明,废水中Zn2+、Al3+、Cd2+、Fe3+、Fe2+在一定pH范围内会发生共沉淀,说明这4种金属不能通过化学沉淀的方法完全分离。
2.2 废水中铝的回收
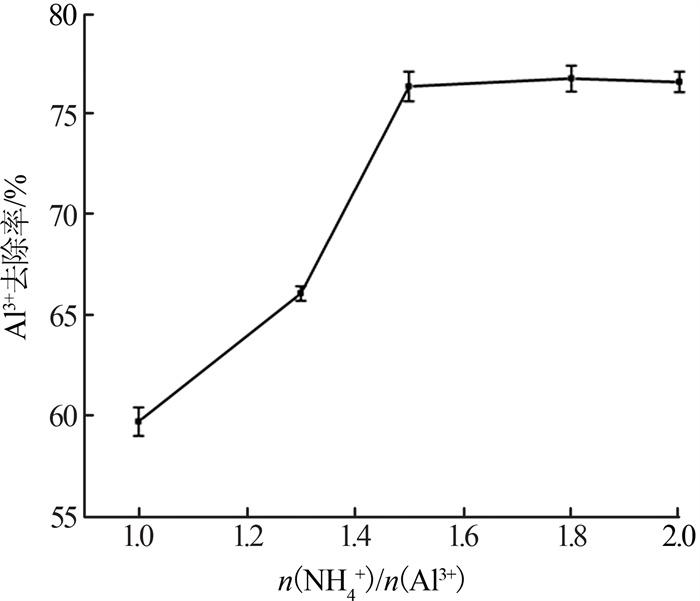
依据硫酸铝铵的溶解度曲线,试验探究了5 ℃下n(NH4+)/n(Al3+)对废水中铝去除率的影响,结果见图 3。
图3
图3
n(NH4+)/n(Al3+)对废水中铝的去除率的影响
Fig.3
Effect of n(NH4+)/n(Al3+)on the removal rate of aluminum in wastewater
由图 3可知,当n(NH4+)/n(Al3+) < 1.5时,铝去除率随n(NH4+)/n(Al3+)增大而提高较快;n(NH4+)/n(Al3+) > 1.5后,继续增加n(NH4+)/n(Al3+),铝去除率增加不大,因此选择n(NH4+)/n(Al3+)=1.5,此时铝的去除率为77.53%。
依据1.3.1节,取200 mL废水,加入理论量1.5倍的硫酸铵,反应后在5 ℃下降温结晶,干燥后得到产物28.671 g,对产物进行XRD分析的结果表明,晶体为硫酸铝铵,测定计算得到硫酸铝铵的纯度为99.43%,符合铵明矾产品标准要求。
2.3 废水剩余铝铁的回收
结晶后的废水中仍含有部分的铝,锌、镉、铁在结晶过程中都没有出现损失,后续欲通过萃取的方法分离剩余金属。考虑到铝和铁的存在会影响锌、镉的分离效果,所以需先对废水中的铝和铁进行去除,而Fe3+的沉淀pH远低于Fe2+,所以要先将Fe2+氧化,之后通过化学沉淀法得到铝和铁的氢氧化物。表 1列出了沉淀时使用不同碱对锌损失量的影响。
表1 沉淀时使用不同碱对锌损失量的影响
Table 1
| 样品 | 碱 | 终点pH | 锌的损失率/% |
| 结晶后废水 | 质量分数40% NaOH | 5.0 | 32.81 |
| 质量分数5% NaOH | 5.08 | 27.46 | |
| 浓氨水 | 5.17 | 6.78 | |
| 氨水(1+1) | 5.1 | 5.1 | |
| 质量分数10%石灰乳 | 5.2 | 37.28 |
图4
图4
氨水用量对铝、铁去除率及沉淀干重的影响
Fig.4
The influence of the amount of ammonia water on the removal rate of aluminum and iron and the dry weight of precipitation
由图 4可知,随着氨水用量的增加,铝、铁去除率先逐渐增加,后趋于平衡;当选择实验氨水用量为21~23 mL/L;时,铝、铁的去除率分别为98.14%和99.51%。沉淀产物可用来制备聚合硫酸铝铁(PAFS)。
2.4 溶剂萃取法分离锌镉
因为锌和镉的沉淀pH较为相近,化学性质也类似。采用一般方法并不能将二者分离,考虑通过溶剂萃取的方法将二者分离,萃取剂选用工业常见的D2EHPA(P204),稀释剂用磺化煤油。
实验首先采用控制单一变量的方法探究了皂化率、P204有机相组成、O/A相比和萃取混合时间对萃取率的影响,结果见图 5。
图5
由图 5可得,最佳萃取条件为:通过两段萃取有机相组成(30% P204+70%磺化煤油),用氨水进行皂化(皂化率40%),相比O/A为1∶1,混合时间15 min。此时,Zn2+、Cd2+的萃取率分别为98.34%、8.69%。
在最佳萃取条件下探究不同平衡pH下对金属的萃取效果,计算萃取率,结果如图 6所示。
图6
图6
不同平衡pH下Zn2+、Cd2+的萃取率
Fig.6
Extraction rate of Zn2+ and Cd2+ under different equilibrium pH
实验以上述沉淀后的废水为样品(废液中仍含有大量锌镉),调节初始pH为5.0~5.1,萃取过程中加入稀硫酸或氨水来调节pH(1~5),达到平衡后分离水相、有机相,计算分配系数,结果见表 2。
表2 平衡pH下Zn2+、Cd2+的分配比和分离系数
Table 2
| 平衡pH | DZn | DCd | SZn/Cd |
| 1 | 0.355 | 0 | ∞ |
| 1.49 | 1.639 | 0.018 | 92.965 |
| 1.8 | 2.095 | 0.023 | 91.458 |
| 2.0 | 3.414 | 0.043 | 79.422 |
| 2.15 | 4.056 | 0.080 | 50.554 |
| 3.02 | 58.172 | 0.097 | 599.878 |
| 3.98 | 999 | 1.514 | 659.642 |
| 5.04 | 999 | 45.729 | 21.846 |
通过萃取分离的方法将Zn2+回收之后,溶液中的金属只剩下Cd2+,加入氨水调节pH使其生成沉淀。过滤后洗涤沉淀,之后干燥得到Cd(OH)2。对剩余滤液中的金属离子进行分析检测可知,废液中金属离子的浓度达到相应标准,可经过处理后回用。
通过上述工艺对废水进行处理后,废水中Zn2+、Cd2+、Al3+、Fe3+质量浓度分别为12.27、8.31、1.52、0.5 mg/L,计算得到废水中锌、镉、铝、铁的去除率分别为99.81%、98.48%、99.52%、99.89%。
3 经济效益
按照废水日排放量100 m3预算,采用该工艺进行锌镉铝铁分离回收所需相应设备投资约40万元。根据废水中的金属含量对成本进行分析,处理废水的成本在500元/m3左右,回收产品的价值为650元/m3左右。重金属废水经过本工艺的处理后,减少了其对环境的影响,同时还具有一定的经济效益。
4 结论
提出了以降温结晶法-化学沉淀法-溶剂萃取法相结合的综合处理工艺,从工业废水中依次分离并回收了铝、铁、锌、镉这些金属。使用的是当地企业所排放的工业废水。试验研究结果表明:
(1)由于废水Zn2+、Cd2+和Fe2+的氢氧化物沉淀曲线相近,不能选择性分离,此外高浓度的Zn2+将与Al3+发生共沉淀,影响分离效果。故不能采用化学沉淀的方法对废水中主要的4种金属进行选择性分离。
(2)试验采用降温结晶的方法回收溶液中的铝,制得铵明矾;之后废水中剩余的铝和铁通过化学沉淀的方法去除,沉淀混合物可用来制备PAFS;最后使用P204萃取剂对锌和镉进行分离,反萃之后得到锌的硫酸盐溶液,镉以氢氧化镉的形式得到回收。废水中锌、镉、铝、铁的去除率分别为99.81%、98.48%、99.52%、99.89%。经联合工艺最终处理后的废水中金属离子浓度符合回用的标准,废水中主要成分为硫酸铵,可将其进行回收并重复利用。
参考文献
A research study on Cr(Ⅵ) removal from electroplating wastewater using chemically modified coconut shell-based activated carbon and treated zeolite
[J].DOI:10.2175/193864703784343758 [本文引用: 1]
Present status of treatment and utilization of heavy metal wastewater
[J].
国内外重金属废水处理新技术的研究进展
[J].DOI:10.3969/j.issn.1673-9108.2007.07.002
New trends in removing heavy metals from wastewater
[J].
Chemical precipitation granular sludge(CPGS) formation for copper removal from wastewater
[J].
离子交换法处理含Cr(Ⅵ)废水的研究
[J].DOI:10.3969/j.issn.1671-3206.2007.01.007
Removal of chromium from water and wastewater by ion exchange resins
[J].
Integrating membrane filtration into bioelectrochemical systems as next generation energy-efficient wastewater treatment technologies for water reclamation: A review
[J].DOI:10.1016/j.biortech.2015.05.058
EDTA络合滴定法连续测定铁矿石中铝铅锌
[J].DOI:10.3969/j.issn.1000-7571.2011.11.014 [本文引用: 1]
EDTA滴定法快速连续测定锌镉
[J].DOI:10.3321/j.issn:1001-4020.2000.12.019 [本文引用: 1]
微波溶样-自动电位滴定法测定铁矿石中全铁量
[J].DOI:10.3969/j.issn.0254-5357.2007.05.017 [本文引用: 1]










 津公网安备 12010602120337号
津公网安备 12010602120337号