甲基橙(Methyl Orange,MO)等偶氮类染料在特殊条件下能分解产生多种致癌物,对人体健康存在极大的潜在危害。目前,废水中MO染料的处理方法主要有吸附法、光降解法〔1〕等,吸附法由于操作简单、分离效率高且固液易分离等优势得到广泛应用。
近年来,以改性生物质材料〔2〕、改性聚合物材料〔3〕、改性无机材料〔4〕等作为吸附剂处理MO的报道很多,但这些类型的吸附材料普遍吸附容量小,且加入的改性剂对环境不友好。层状双金属氢氧化物(LDHs)因其特殊的记忆效应、层间距可调控、层间阴离子可交换等性质,在吸附领域得到了广泛应用。Na LI等〔5〕采用低共熔溶剂(DESs)一步水热法合成Mg2Al-Cl LDH,S. SAGHIR等〔6〕将金属有机框架材料与水滑石复合制得ZIF-67@LDH,上述水滑石及改性水滑石对MO等阴离子染料具有良好的吸附性能,但均是以可溶性金属盐及碱为原料通过共沉淀法制备的。共沉淀法的制备过程中原子利用率较低,会产生大量高浓度含盐废水,易对环境造成二次污染。
本研究以金属氢氧化物代替可溶性金属盐为原料,通过诱导水解清洁制备钙铝类水滑石,滤液可重复使用,减少了废水排放。探讨了不同制备方法(共沉淀法、清洁法)对钙铝类水滑石吸附MO性能的影响,并通过吸附动力学和等温吸附模型拟合,结合吸附前后样品的IR、XRD和SEM图谱,探究了钙铝类水滑石的吸附机理。
1 材料与方法
1.1 实验材料
Ca(OH)2(质量分数96%);Al(OH)3、Na2CO3、甲基橙、CaCl2、NaAlO2、NaOH均为分析纯;自制蒸馏水。
1.2 钙铝类水滑石的制备
(1)清洁法:取0.16 mol Ca(OH)2、0.04 mol Al(OH)3和0.01 mol Na2CO3固体于三颈烧瓶中,加入热蒸馏水200 mL,保持油浴温度80 ℃,机械搅拌反应2 h;将反应液转至晶化釜中,80 ℃晶化17 h;抽滤,洗涤滤饼3次,再将滤饼于80 ℃烘箱内烘干,将得到的产物研磨,过75 μm标准筛,装袋,记为Ca4Al-LDHs-1。
(2)共沉淀法:取0.16 mol CaCl2、0.04 mol NaAlO2和0.01 mol Na2CO3溶于120 mL蒸馏水配得A液,取适量NaOH固体溶于120 mL蒸馏水配得B液;将A、B两溶液同时滴入装有60 mL蒸馏水的三颈烧瓶中,控制油浴温度80 ℃,保持釜内pH为10左右,液体滴加时长约1 h,滴加完毕再机械搅拌反应1 h;将反应液转至晶化釜中,80 ℃晶化17 h;抽滤,洗涤滤饼3次,再将滤饼于80 ℃烘箱内烘干,将得到的产物研磨,过75 μm标准筛,装袋,记为Ca4Al-LDHs-2。
1.3 材料表征
采用Bruke D8 Advance型X射线粉末衍射仪对样品的物相进行分析;利用Thermo Scientific Nicolet iS5型红外光谱仪测定吸附前后样品的分子结构(波数600~1 750 cm-1);比表面积采用康塔AUTOSORB IQ全自动比表面积分析仪分析;样品的形貌及Ca、Al元素的相对含量采用德国ZEISS Gemini 500场发射扫描电子显微镜分析(附X射线能谱仪,德国Bruker);采用722型可见分光光度计测定溶液中MO的浓度。
1.4 吸附实验
取50 mL一定质量浓度(100~600 mg/L)的MO溶液于锥形瓶中,将锥形瓶置于一定温度(293~303 K)的恒温振荡仪内振荡数分钟,称取50 mg钙铝类水滑石于锥形瓶内,同时开始振荡吸附。隔一段时间取样、过滤,于464 nm下测定上清液的吸光度,吸附后溶液中MO的浓度根据标准曲线y=0.070 79x+0.0194(R2=0.999 68)计算。
2 结果与讨论
2.1 表征分析
2 种不同方法合成的类水滑石、MO、Ca4Al-LDHs-1吸附MO后的红外光谱如图1所示。
图1
图1
Ca4Al-LDHs,MO和Ca4Al-LDHs-1吸附MO后的红外光谱
Fig. 1
IR of Ca4Al-LDHs,MO and Ca4Al-LDHs-1 after MO adsorption
由图1可知,Ca4Al-LDHs-1吸附MO后的样品中出现了MO的特征吸收峰,820 cm-1和1 120 cm-1分别为苯环C—H键平面外和平面内弯曲振动峰,1 032 cm-1和1 171 cm-1是—SO3-和S
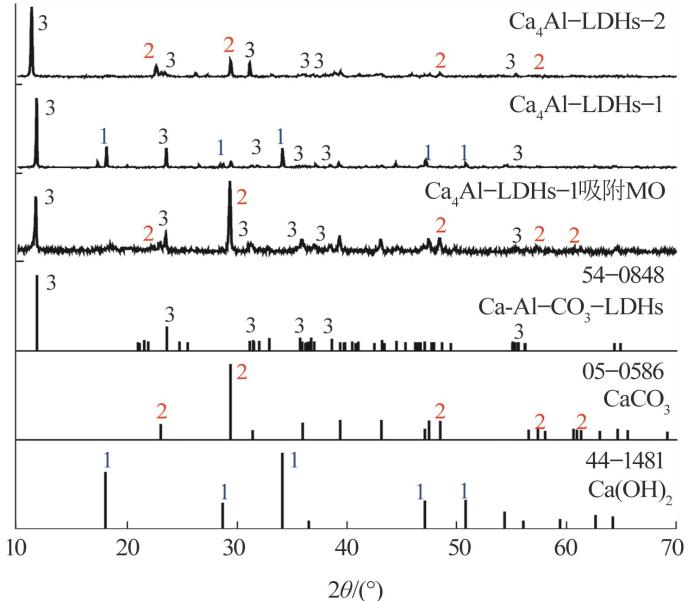
图2为采用不同方法合成的钙铝类水滑石以及Ca4Al-LDHs-1吸附MO后的XRD图谱。
图2
图2
Ca4Al-LDHs,Ca4Al-LDHs-1吸附MO后的XRD
Fig. 2
XRD patterns of Ca4Al-LDHs and Ca4Al-LDHs-1 after MO adsorption
由图2可知,3种样品均具有较尖锐的衍射峰,说明类水滑石在吸附前后均保持较好的结晶状态,但吸附MO后的样品衍射峰有明显的变宽现象,可能是MO插入类水滑石层间,使得类水滑石结晶度有所降低〔9〕;对比类水滑石与PDF卡片中的特征衍射峰,采用清洁法合成的Ca4Al-LDHs-1和共沉淀法合成的Ca4Al-LDHs-2均至少有2个物相,其中Ca4Al-LDHs-1主要包含插层了CO32-的类水滑石和Ca(OH)2,而Ca4Al-LDHs-2则主要由插层了CO32-的类水滑石和CaCO3组成,且Ca4Al-LDHs-2的特征衍射峰与对应的标准卡片特征衍射峰的位置及强度偏差较小,这可能是由于共沉淀法制备的类水滑石其层间阴离子不仅有CO32-,同时也有Cl-(其特征衍射峰与PDF #44-0616也很相似)。值得重点指出的是,Ca4Al-LDHs-1吸附MO后出现了CaCO3的特征衍射峰,且峰强度很大,而Ca(OH)2的特征峰基本消失,说明Ca4Al-LDHs-1吸附MO的过程发生了化学变化,而这一化学反应极可能成为Ca4Al-LDHs-1具有较强MO吸附性能的关键原因。
图3为采用清洁法和共沉淀法合成的钙铝类水滑石以及Ca4Al-LDHs-1吸附MO后的SEM图。
图3
图3
Ca4Al-LDHs,Ca4Al-LDHs-1吸附MO后的SEM
(a)Ca4Al-LDHs-1;(b)Ca4Al-LDHs-2;(c)Ca4Al-LDHs-1吸附MO后
Fig. 3
SEM images of Ca4Al-LDHs and Ca4Al-LDHs-1 after MO adsorption
图4是能谱仪通过点分析获得的Ca4Al-LDHs-1和Ca4Al-LDHs-2的元素分布情况。
图4
图4
Ca4Al-LDHs-1(a)和Ca4Al-LDHs-2(b)的EDS分析
Fig. 4
EDS analysis of Ca4Al-LDHs-1(a) and Ca4Al-LDHs-2(b)
从图4可知,2种方法合成的类水滑石中Ca、Al、C、O元素分布均匀,且Ca4Al-LDHs-2中均匀分布Cl元素,说明Ca4Al-LDHs-2层间既有CO32-又有Cl-〔11〕,与XRD分析结果一致。
Ca4Al-LDHs-1和Ca4Al-LDHs-2比表面积及孔结构测试结果如表1所示。
表1 Ca4Al-LDHs的比表面积及孔结构
Table 1
| 样品 | SBET/(m2·g-1) | 孔容/(cm3·g-1) | 孔径/nm |
|---|---|---|---|
| Ca4Al-LDHs-1 | 3.987 | 0.011 | 3.078 |
| Ca4Al-LDHs-2 | 6.536 | 0.021 | 3.840 |
2.2 制备方法对Ca4Al-LDHs吸附性能的影响
在MO初始质量浓度为100 mg/L,吸附剂用量为1 g/L,吸附温度为30 ℃,吸附时间为90 min时,考察了清洁法和传统共沉淀法制备的类水滑石对MO去除效果的差异,结果见图5。
图5
图5
制备方法对类水滑石吸附MO性能的影响
Fig. 5
Effect of preparation method of Ca4Al-LDHs on MO adsorption
如图5所示,清洁法制备的Ca4Al-LDHs-1对MO的去除率达90.4%,是传统共沉淀法制备的Ca4Al-LDHs-2的5.5倍,这与史月月等〔13-14〕提到的情况相似,材料的吸附性能与材料的比表面积和孔容非正相关。究其原因,主要取决于材料的吸附机理。目前,关于 MO的吸附机理包括:与材料本身的比表面积和孔径结构相关的物理吸附,以及与材料表面的官能团或材料层间特殊作用相关的物理/化学吸附〔11,15〕。钙铝类水滑石由于制备过程中易团聚〔9〕或产生其他杂质,因而比表面积和孔容较小,主要靠其结构正电荷与阴离子产生静电引力,从而实现吸附作用。而Ca4Al-LDHs-1由于层间夹杂少量Ca(OH)2,其在低温水溶液中具有一定的溶解度,溶解出来的Ca2+与类水滑石层间交换出来的CO32-结合生成CaCO3(Ca4Al-LDHs-1吸附MO后的XRD已证实),这一反应便成为MO阴离子交换层间CO32-的驱动力,使得MO不断插层进入类水滑石层间,而溶液中Ca2+浓度的降低又促使Ca(OH)2继续溶解,由此实现Ca4Al-LDHs-1对MO的高吸附容量。
2.3 吸附动力学
在不同温度(293 、303 、313 K)下测量了Ca4Al-LDHs-1对100 mg/L的MO溶液的平衡吸附量随吸附时间的变化。不同温度下,Ca4Al-LDHs-1均能在吸附40 min左右达到平衡。将实验数据用准一级动力学和准二级动力学方程拟合,结果见表2。
表2 Ca4Al-LDHs-1吸附MO的动力学数据
Table 2
| T/K | C0/(mg·L-1) | qe,exp/(mg·g-1) | 准一级动力学 | 准二级动力学 | ||||
|---|---|---|---|---|---|---|---|---|
| qe,cal/(mg·g-1) | k1/min-1 | R2 | qe,cal/(mg·g-1) | k2/(g·mg-1·min-1) | R2 | |||
| 293 | 100 | 98.51 | 54.97 | 0.048 04 | 0.891 7 | 100 | 0.003 623 | 0.999 87 |
| 303 | 100 | 97.31 | 17.47 | 0.038 99 | 0.979 7 | 98.04 | 0.006 120 | 0.999 98 |
| 313 | 100 | 94.35 | 5.234 | 0.021 7 | 0.829 7 | 93.46 | 0.018 77 | 0.999 99 |
2.4 MO的初始浓度对吸附效果的影响
图6
图6
温度(a)和MO初始质量浓度(b)对MO吸附性能的影响
Fig. 6
Effect of temperature(a) and initial mass concentration(b) on MO adsorption
将实验数据代入Langmuir等温方程和Freundlich等温方程中进行拟合,相应的热力学参数及相关系数见表3。由R2可知,实验温度下,Ca4Al-LDHs-1对MO的吸附更符合Langmuir等温方程。2.5 吸附容量与其他吸附剂对比
表3 Ca4Al-LDHs-1对MO的吸附等温线参数
Table 3
| T/K | Langmuir等温模型 | Freundlich等温模型 | ||||
|---|---|---|---|---|---|---|
qm/ (mg·g-1) | KL/ (L·mg-1) | R2 | KF/ (L·mg-1) | n | R2 | |
| 293 | 526.32 | 0.196 5 | 0.993 78 | 186.05 | 4.32 | 0.988 34 |
| 303 | 645.16 | 0.064 96 | 0.997 | 89.75 | 2.28 | 0.962 19 |
| 313 | 689.66 | 0.070 32 | 0.994 92 | 95.13 | 2.17 | 0.958 71 |
表4对比了Ca4Al-LDHs-1和其他文献报道的吸附材料对MO的饱和/平衡吸附容量,从数据可以看出,Ca4Al-LDHs-1对MO的吸附容量(545 mg/g)明显大于其他类型的水滑石及改性材料,且本法操作简单,滤液可重复利用,具有较强的工业应用前景。
表4 Ca4Al-LDHs-1对MO的吸附容量与其他文献对比情况
Table 4
3 结论
(1)清洁法和共沉淀法均能制备具有层状结构的类水滑石。相同吸附条件下,清洁法制备的样品对MO的去除率(90.4%)是共沉淀法样品的5.5倍。
(2)Ca4Al-LDHs-1对MO的吸附更符合准二级动力学模型和Langmuir等温方程。
(3)比表面积分析及Ca4Al-LDHs-1吸附MO前后的IR、XRD及SEM表明,吸附作用主要是层间阴离子交换作用的结果,且吸附过程中发生的化学反应促进了MO阴离子与CO32-的层间交换作用。
(4)清洁法制备的Ca4Al-LDHs是一类低成本、高效能、环保的吸附材料,有望工业化并成为去除阴离子污染物的候选材料。
参考文献
Facile preparation of recyclable magnetic Ni@filter paper composite materials for efficient photocatalytic degradation of methyl orange
[J].
HNO3改性鱼鳞对染料废水中甲基橙吸附探究
[J].
Adsorption of methyl orange by modified fish scales with HNO3
[J].
Adsorption,kinetics and thermodynamics studies of methyl orange dye sequestration through chitosan composites films
[J].
Efficient removal of methyl orange from aqueous solution using mesoporous ZSM-5 zeolite:Synthesis,kinetics and isotherm studies
[J].
Deep eutectic solvents assisted synthesis of MgAl layered double hydroxide with enhanced adsorption toward anionic dyes
[J].
Hierarchical mesoporous ZIF-67@LDH for efficient adsorption of aqueous methyl orange and alizarine red S
[J].
Multiscale mechanistic study of the adsorption of methyl orange on the external surface of layered double hydroxide
[J].
Removal of methyl orange from aqueous solutions through adsorption by calcium aluminate hydrates
[J].
Preparation of Ca/Al-layered double hydroxide and the influence of their structure on early strength of cement
[J].
Effect of anion co⁃existence on ionic organic pollutants removal over Ca based layered double hydroxide
[J].
Systematic utilization of layered double hydroxide nanosheets for effective removal of methyl orange from an aqueous system by π-π stacking⁃induced nanoconfinement
[J].
改性稻壳生物炭对水溶液中甲基橙的吸附效果与机制
[J].
Effects and mechanisms of methyl orange removal from aqueous solutions by modified rice shell biochar
[J].
CoFe2O4/磺化石墨烯的合成及对低浓度甲基橙的吸附
[J].
Synthesis of CoFe2O4/sulfonated graphene and its adsorption for low⁃concentration methyl orange
[J].
A novel CoFe layered double hydroxides adsorbent:High adsorption amount for methyl orange dye and fast removal of Cr(Ⅵ)
[J].
活化煤矸石对水中亚甲基蓝吸附行为的研究
[J].
Adsorption of methylene blue from aqueous solution on activated coal gangue
[J].
三维花状层状双金属氢氧化物的制备及其对甲基橙的去除
[J].
Synthesis of 3D flower⁃like hierarchical layered double hydroxide microspheres and removal of methyl orange
[J].
MgAl-LDH吸附甲基橙性能研究
[J].
Studies on adsorption of methyl orange from aqueous onto Mg/Al-LDH
[J].
Zn-Al水滑石及焙烧产物对甲基橙废水的吸附研究
[J].
Adsorption research of Zn-Al hydrotalcite and calcined product to methyl orange waster water
[J].
磁性镁铝类水滑石的制备及其对甲基橙的吸附研究
[J].
Preparation of Fe3O4@hydrotalcite⁃like compound and its adsorption capacity for methyl orange
[J].
以钢渣为原料合成Ca-Mg-Al-Fe层状双金属氢氧化物及其对甲基橙的吸附
[J].
Preparation of Ca-Mg-Al-Fe layered double hydroxides using steelmaking slag as raw material and its adsorption to methyl orange
[J].










 津公网安备 12010602120337号
津公网安备 12010602120337号