随着工业4.0时代的到来,工业产品的种类和数量剧增,工业生产废水的成分越来越复杂,呈现出毒性大、色度高、难降解等特点。另外,国家层面提出绿水青山就是金山银山的环保口号,人们对环保的要求越来越高,工业废水的处理越来越受到重视。臭氧催化氧化作为一种高级氧化法,其能通过强化羟基自由基(·OH)的产生,使废水中大多数难降解有机污染物完全分解为CO2、H2O和无机离子,具有绿色、无二次污染的优势〔1-2〕。与单独的臭氧氧化技术相比,臭氧催化氧化具有更高的臭氧利用效率,可进一步提高难降解废水的可生化性,降低其毒性〔3〕。臭氧催化氧化技术包含光催化(UV/O3)、碱催化(O3/H2O2)、多相催化(O3/固体催化剂)等工艺,其中光催化臭氧氧化处理技术因具有杀菌能力强、作用快、效果好等特点而备受关注,其原理为:水中的溶解臭氧在紫外光的照射下,产生超氧负离子(O2·-)、激发基态氧分子(O2*)、H2O2以及·OH等活性物质,这些物质通过破坏有机物分子的结构,使大分子有机物分解成小分子物质,从而达到降解有机污染物的目的〔4〕。
二硝基重氮酚(DDNP)是目前国内产量最大、应用最广的起爆药,其生产过程中排出的废水主要来自还原、重氮化和洗涤工序,每生产l kg DDNP产品大约产生200~300 kg废水,废水产生量较大。废水中含带有重氮基、硝基等难生物降解基团的污染物,成分复杂、色度高、毒性大〔5〕。为控制该类废水污染,我国制订了《兵器工业水污染物排放标准 火工药剂》(GB 14470.2—2002),其规定满足排放要求的该类废水中主要特征污染物硝基酚类化合物的质量浓度≤6.0 mg/L。
本研究以DDNP生产废水为处理对象,对比研究UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ) 3种臭氧光催化氧化工艺对于难降解废水的处理效果,探究其各自的氧化作用机理,分析3种工艺的处理效率,以期为臭氧光催化氧化处理工业废水的工艺选择提供参考。
1 实验部分
1.1 废水水质
实验废水取自陕西省铜川矿务局一五三厂DDNP生产废水,废水经消爆后的水质见表1。
表1 DDNP生产废水水质
Table 1
| pH | 色度/倍 | TOC/(mg·L-1) | m(BOD5)/ m(COD) | 硝基酚/(mg·L-1) | 外观 |
|---|---|---|---|---|---|
| 7.92 | 14 200 | 405.73 | 0.06 | 101.20 | 黑褐色 |
1.2 实验装置
实验装置见图1。氧化反应在高300 mm、内径74 mm的有机玻璃反应器中进行,反应器配备25 W低压紫外灯,可发射254 nm单色光,反应器安装有水套,内置循环水可将反应器温度恒定在25 ℃。采用臭氧发生器(哈尔滨久久化学工程技术有限公司,DHX-SS-1G型),利用干燥的空气产生臭氧,空气流量控制在150 L/h。进出反应器的臭氧浓度均采用MOT500臭氧在线检测仪进行实时监测,进料气体的臭氧质量浓度保持在9.50 mg/L,尾气采用KI溶液吸收。
图1
1.3 实验方法
UV/O3工艺处理DDNP生产废水。量取1 000 mL废水,将其全部倒入反应器中,利用H2SO4和NaOH分别调节酸碱性至设定值,开启臭氧发生器和紫外灯计时反应。记录1 h内的进出臭氧质量浓度,并每隔10 min取20 mL水样用0.45 μm滤膜进行过滤后,测定水样TOC、硝基酚类化合物含量等指标。
UV/O3/H2O2或UV/O3/Fe(Ⅲ)工艺处理DDNP生产废水。量取1 000 mL废水,将其全部倒入反应器中,然后加入一定量的氧化剂H2O2或Fe(Ⅲ),待氧化剂与废水混合均匀后,利用H2SO4和NaOH分别调节酸碱性至设定值,开启臭氧发生器和紫外灯计时反应。记录1 h内的进出臭氧质量浓度,并每隔10 min取20 mL水样用0.45 μm滤膜进行过滤后,测定水样TOC、硝基酚类化合物含量等指标。
1.4 分析方法
依据《水质色度的测定 稀释倍数法》(GB 11903—1989)测定水样色度;采用德国元素液体TOC分析仪测定水样TOC;依据《化学需氧量的测定 重铬酸钾法》(GB 11914—1989)测定水样COD;依据《水质五日生化需氧量的测定 稀释与接种法》(HJ 505—2009)测定水样BOD5;依据《十六烷基三甲基溴化铵分光光度法》(GB 14470.2—2002)测定硝基酚类化合物含量。
依照文献〔8〕,定义臭氧光催化氧化效率为工艺效率,用TOC去除质量与消耗的臭氧质量之比来表示,其具体计算见
2 结果与讨论
2.1 臭氧光催化氧化工艺最佳pH的确定
图2
图2
pH对硝基酚类化合物降解率的影响
Fig. 2
Effect of pH on the degradation rate of nitrophenols
2.2 UV/O3/H2O2工艺H2O2投加量的确定
UV/O3工艺对于水中一般难降解污染物的氧化分为2个阶段,第一阶段中在紫外光的照射下水中臭氧光解生成H2O2〔
UV/O3/H2O2工艺被认为是高污染废水较为有效的处理方法之一〔10〕,该工艺向UV/O3体系中加入H2O2,H2O2会部分解离为HO2-,而HO2-能加快O3在水中分解产生·OH,使污染物被快速和完全矿化。
图3
图3
H2O2投加量对硝基酚类化合物降解率的影响
Fig. 3
Effect of H2O2 dosage on the degradation rate of nitrophenols
图4
由图3可看出,对比UV/O3工艺,当n(H2O2)∶n(硝基酚类化合物)=3∶1时,采用UV/O3/H2O2工艺对硝基酚进行降解,反应时间1 h时硝基酚降解率由87%提高到94%,而在n(H2O2)∶n(硝基酚类化合物)为6∶1和1∶1时硝基酚的降解会受到轻微抑制。推测其原因,可能是尽管H2O2投加量的增加会导致体系中·OH浓度的增加,但是硝基酚降解的主要途径是臭氧直接氧化,H2O2投加量较少或较多时臭氧的消耗影响了硝基苯类化合物的降解,但H2O2投加量为3∶1时,推测由于H2O2阻碍了
由图4可看出,当不添加H2O2时UV/O3工艺的TOC去除率明显低于UV/O3/H2O2工艺的值。当n(H2O2)∶n(硝基酚类化合物)由1∶1增加到6∶1时,氧化处理1 h废水TOC去除率由78%增加到89%。这是因为在UV辐射的条件下,H2O2投加量的增加会提高体系中自由基的生成浓度,从而提高有机物的去除率。同时考虑到H2O2投加量较多时,硝基酚类化合物降解会受到抑制,因此当n(H2O2)∶n(硝基酚类化合物)=3∶1时,UV/O3/H2O2工艺的综合处理效果较佳。
2.3 UV/O3/Fe(Ⅲ)工艺Fe(Ⅲ)投加量的确定
UV/O3/Fe(Ⅲ)工艺原理是:向UV/O3体系中加入Fe(Ⅲ),Fe(Ⅲ)在紫外光和近紫外光照射下与溶液中的水分子发生光氧化还原反应,产生Fe(Ⅱ)和·OH〔
图5
图5
Fe(Ⅲ)投加量对硝基酚类化合物降解率的影响
Fig. 5
Effect of Fe(Ⅲ) dosage on the degradation rate of nitrophenols
图6
由图5可以看出,以UV/O3工艺为基准,当n〔Fe(Ⅲ)〕∶n(硝基酚类化合物)=0.1∶1时,硝基酚降解速率基本没有变化,但当投加比例增加到1∶1和3∶1时,硝基酚的降解却被明显抑制,这一结果同样可以通过硝基酚的降解主要源于直接臭氧化作用来解释。
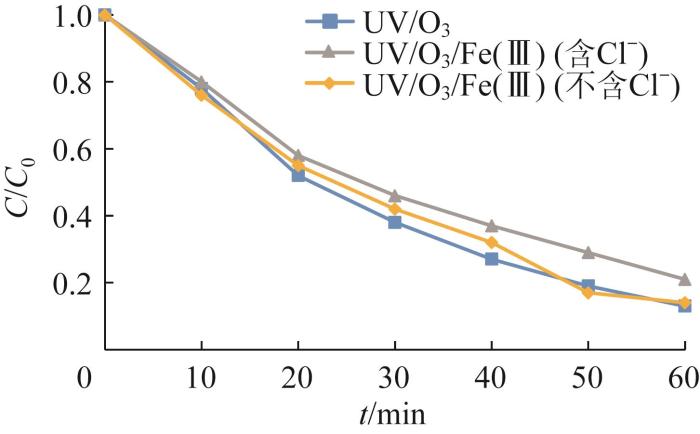
由图6可以看出,对于废水TOC的去除,UV/O3/Fe(Ⅲ)工艺的处理效果明显优于UV/O3工艺的处理效果,这是因为三价铁离子的加入促进了自由基的生成,因而增强了对废水中TOC的去除。另外,由图6还可知,少量Fe(Ⅲ)的投加即可明显提升体系对TOC的去除效果,当n〔Fe(Ⅲ)〕∶n(硝基酚类化合物)=0.1∶1时,氧化处理1 h废水TOC去除率达到96%,而投加较多的铁离子时体系对废水TOC的处理效果变差,这是因为实验中使用的铁盐是FeCl3,含有Cl-,其是一种·OH抑制剂〔11〕。因此,综合考虑图5和图6的实验结果,当n〔Fe(Ⅲ)〕∶n(硝基酚类化合物)=0.1∶1时,UV/O3/Fe(Ⅲ)工艺的处理效果较佳。
图7
图7
Cl-对硝基酚类化合物降解率的影响
Fig. 7
Effect of Cl- on the degradation rate of nitrophenols
图8
2.4 工艺对比
在废水初始pH=3,UV/O3/H2O2工艺中n(H2O2)∶n(硝基酚类化合物)=3∶1,UV/O3/Fe(Ⅲ)工艺中n〔Fe(Ⅲ)〕∶n(硝基酚类化合物)=0.1∶1的条件下,对UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ)3种工艺处理DDNP生产废水1 h的效果进行对比,结果见表2。
表2 3种工艺废水处理效果对比
Table 2
| 工艺组合 | 出水色度/倍 | 出水硝基酚/(mg·L-1) | 出水TOC/(mg·L-1) | m(BOD5)/m(COD) | 工艺效率/% |
|---|---|---|---|---|---|
| UV/O3 | 75 | 11.13 | 121.72 | 0.15 | 27 |
| UV/O3/H2O2 | 50 | 9.11 | 73.03 | 0.32 | 35 |
| UV/O3/Fe(Ⅲ) | 50 | 5.06 | 16.23 | 0.46 | 52 |
由表2可知,在UV/O3工艺基础上投加H2O2和Fe(Ⅲ)对硝基酚类化合物的降解影响不大,但对TOC的去除表现出明显的提升效果,尤其是少量铁离子的加入大大提高了TOC的去除率。UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ)3种工艺在优化条件处理DDNP生产废水1 h后出水的色度、TOC均满足GB 14470.2—2002排放标准(色度≤120倍,TOC≤150 mg/L),但只有UV/O3/Fe(Ⅲ)工艺的出水硝基酚达到了GB 14470.2—2002排放标准(≤6.0 mg/L)。
此外,UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ) 3种工艺处理后废水的可生化性由0.06分别提升到0.15、0.32、0.46,工艺效率分别为27%、35%、52%,表明各体系均能在不同程度上对DDNP废水中的难降解有机物进行降解,而UV/O3/Fe(Ⅲ)工艺相对于其他工艺则具有更优表现。
3 结论
以特征污染物硝基酚的降解率及TOC去除率为评价指标,在优化条件下对比了UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ)3种臭氧光催化氧化工艺处理DDNP生产废水的效果,得到如下结论:
(1)UV/O3工艺在pH=3时,对硝基酚类化合物的降解效果较佳,碱性条件下,该工艺对硝基酚类化合物的降解表现出轻微抑制效果。相较于UV/O3工艺,UV/O3/H2O2工艺在n(H2O2)∶n(硝基酚类化合物)=3∶1时,氧化1 h后废水TOC去除率有所提升,而UV/O3/Fe(Ⅲ)工艺在n〔Fe(Ⅲ)〕∶n(硝基酚类化合物)=0.1∶1时,氧化1 h后废水TOC去除率有大幅度的提升,但这2种工艺都没有明显提升特征污染物硝基酚类化合物的降解率。
(2)针对DDNP废水的水质特点,少量Fe(Ⅲ)的加入会提升废水综合处理效果,但需要注意的是,Fe(Ⅲ)投加时Cl-的引入或者过量铁离子会抑制·OH的产生,从而降低废水的TOC去除率。
(3)经检测,UV/O3、UV/O3/H2O2、UV/O3/Fe(Ⅲ)3种工艺在考察的最佳实验条件下氧化DDNP废水1 h后出水的色度、TOC均达到GB 14470.2—2002排放标准,其中UV/O3/Fe(Ⅲ)工艺表现出最优的处理效果,其出水硝基苯类化合物达到GB 14470.2—2002排放标准,废水m(BOD5)/m(COD)可由0.06提升到0.46,工艺效率可达52%。
参考文献
Identification of new oxidation products of bezafibrate for better understanding of its toxicity evolution and oxidation mechanisms during ozonation
[J].
臭氧催化氧化在工业废水处理中的应用进展
[J].
Application progress of catalytic ozonation in industrial effluents treatment
[J].
臭氧催化氧化工艺处理工业废水的研究进展
[J].
Review on research of catalytic ozonation industrial wastewater
[J].
臭氧高级氧化法处理化工废水的进展研究
[J].
Research on chemical wastewater treatment with advanced oxidation processes
[J].
DDNP废水处理方法浅析
[J].
Discussion on the DDNP waste-water treatment methods
[J].
混凝-吸附处理DDNP废水的研究
[D].
Study on treatment of wastewater produced by DDNP production with coagulation and adsorption
[D].
化学需氧量测定中H2O2干扰消除方法
[J].
Elimination method of H2O2 interference in determination of CODCr
[J].
Oxidation of nitrobenzene by O3/UV:The influence of H2O2 and Fe(Ⅱ). Experiences in a pilot plant
[J].
催化臭氧氧化处理DDNP废水的研究
[D].
Catalytic oxidation of DDNP wastewater
[D].
基于过硫酸盐和过氧化氢高级氧化体系处理DDNP工业废水的研究
[D].
Treatment of DDNP industrial wastewater by advanced oxidation system based on persulfate and hydrogen peroxide
[D].
Paraben degradation using catalytic ozonation over volcanic rocks
[J].












 津公网安备 12010602120337号
津公网安备 12010602120337号