目前,寻找环境友好、廉价的高效吸附剂仍是吸附技术关注的焦点。经文献调研发现,有关环境友好型四氧化三铁/镁铁类水滑石复合物的制备及其吸附行为的研究尚未报道。因此,笔者采用两步法制备了一系列四氧化三铁/镁铁类水滑石复合物(Fe3O4@Mg-Fe-LDH,简写为FLDH),并以甲基橙为模拟污染物,研究了FLDH吸附偶氮染料类有机污染物的行为。
1 试验材料与方法
1.1 仪器与试剂
752型紫外可见分光光度计,中国彩虹公司;pHS-3C型pH计,上海雷磁仪器有限公司;BS110S型电子天平,德国Sartorius公司;ZHWY-2012C振荡器;X-射线粉末衍射仪,辽宁丹东。所用试剂均为市售分析纯,所有溶液均采用去离子水配制。
1.2 四氧化三铁的制备
四氧化三铁采用溶剂热法〔17〕制备:称取10.66 g六水合氯化铁和17.28 g六水合醋酸钠,加入120 mL的乙二醇,室温下磁力搅拌至固体药品溶解,形成分散均匀的棕黄色溶液;将上述溶液转移至高压反应釜中,置于干燥箱中,于180 ℃下恒温反应24 h,抽滤,洗涤,干燥即可得到四氧化三铁产品。
1.3 Fe3O4@Mg-Fe-LDH的制备
(1)称取1 g制备的四氧化三铁产品于250 mL的烧杯中,加入体积比1:1的去离子水-甲醇的混合溶液100 mL,用玻璃棒搅拌均匀后,超声分散20 min。(2)将分散均匀的四氧化三铁悬浊液转入250 mL的圆底烧瓶中,室温下磁力搅拌。(3)将一定量的六水合氯化镁与九水合硝酸铁(二者物质的量比为3:1)的混合溶液转入酸式滴定管中待用。(4)将6.4 g的氢氧化钠和21.2 g的无水碳酸钠用150 mL的去离子水溶解,形成所需要的碱液。(5)将步骤(3)的混合盐溶液和步骤(4)的混合碱溶液同时滴入持续磁力搅拌的步骤(2)的四氧化三铁悬浊液中,控制二者的滴加速度,使反应悬浊液的pH稳定在8.5左右,滴定结束后,于75 ℃油浴搅拌10 h,之后将最终反应的悬浊液抽滤、洗涤、干燥,即可得FLDH。根据Mg-Fe-LDH在FLDH中质量分数(0%、39%、55%、66%、80%)的不同,将FLDH分别命名为FLDH0、FLDH39、FLDH55、FLDH66、FLDH 80。Mg-Fe-LDH含量的计算见式(1)。
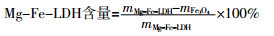
1.4 批量吸附实验
1.4.1 pH对吸附的影响
分别称取0.03 g FLDH55于盛有30 mL MO溶液(30 mg/L)的50 mL离心管中,用0.5 mol/L的HCl或NaOH溶液调节吸附体系至不同的pH。置于恒温(35 ℃)振荡器中,以300 r/min的振荡速度振荡12 h至吸附平衡,然后用磁铁分离,取上层清液,分别分析其浓度变化。并根据溶液中MO的初始质量浓度和吸附平衡时的浓度差计算FLDH对MO的吸附去除率。
1.4.2 Mg-Fe-LDH含量的影响
分别称取Mg-Fe-LDH不同含量的FLDH于盛有30 mL MO溶液(30 mg/L或80 mg/L)的50 mL离心管中,用0.2 mol/L的HCl溶液调节吸附体系的pH至4.5。其他步骤同1.4.1。
1.4.3 吸附等温线
分别移取不同体积的MO贮备液于盛有0.03 g Fe3O4@Mg-Fe-LDH的50 mL离心管中,在35 ℃和pH=7.0的条件下振荡12 h至吸附平衡,然后快速离心分离,分别测定其平衡浓度,并计算Fe3O4@Mg-Fe-LDH吸附MO的平衡吸附量。
1.4.4 分析方法
利用MO与其最大吸收波长(465 nm)有很好的线性相关性这一特点,采用紫外-可见分光光度法测定溶液中MO的浓度。
2 结果与讨论
2.1 材料表征
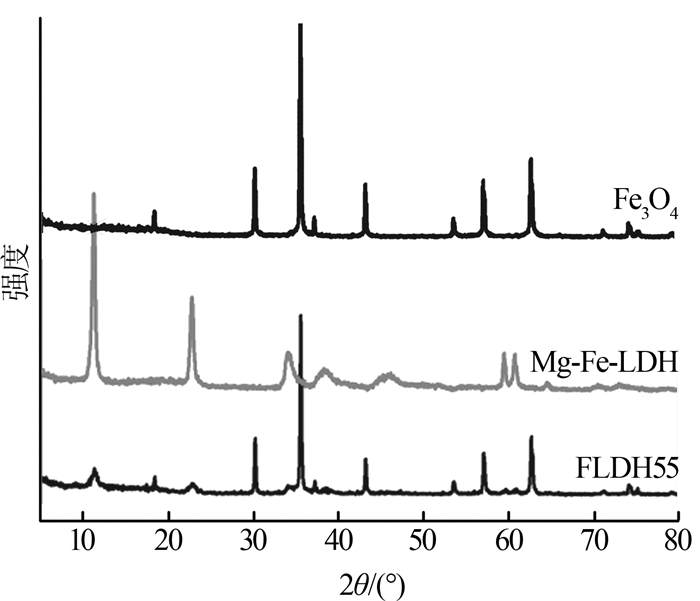
图1是四氧化三铁(Fe3O4)、镁铁类水滑石(Mg-Fe-LDH)、FLDH55的XRD图谱。
图1
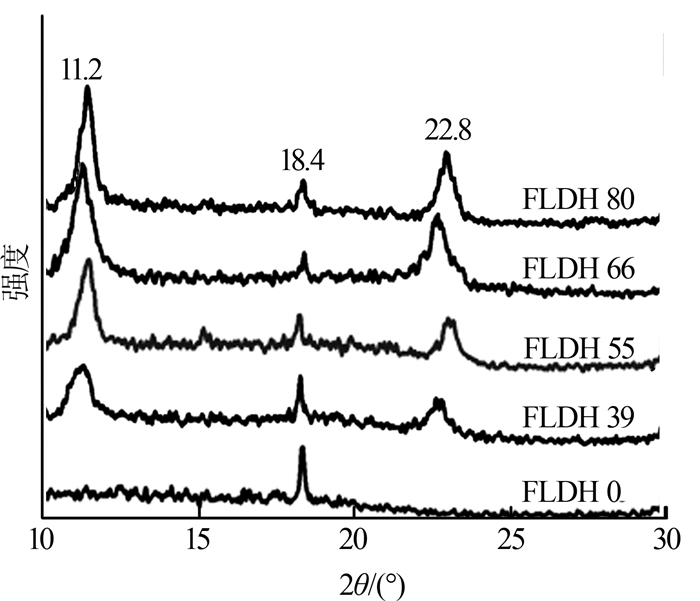
可以看出,图1中的Fe3O4与标准图库的Fe3O4(JCPDF番号为97- 015-9969)相对应。Mg-Fe-LDH在2θ在11.2°、22.8°、34.2°、38.3°、45.9°、59.5°、60.7°出现层状六角形晶体结构的特征衍射峰〔18-19〕,它们分别归属于(003)、(006)、(012)、(015)、(018)、(110)、(113)等7个晶面。该物种的结构式为Mg6Fe2(OH)16(CO3)(H2O)4.5,属于P63/m空间群,对应于JCPDF番号为97- 002-7321。FLDH55的XRD图上同时出现了Mg-Fe-LDH层状结构的特征衍射峰(2θ为11.2°、22.8°、34.2°、38.3°、59.5°、60.7°等)和Fe3O4的主要特征衍射峰(2θ为18.4°、30.0°、35.5°、62.7°等),标志着Fe3O4@Mg-Fe-LDH磁性复合结构的形成。
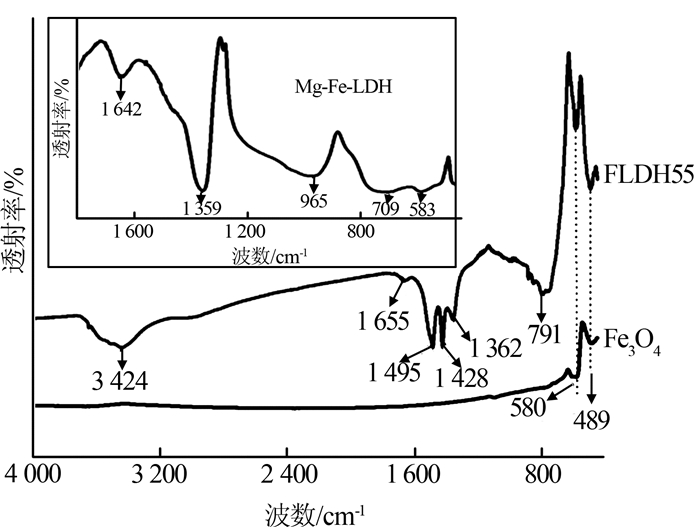
图2是Fe3O4和FLDH55的FT-IR图谱。
图2
由图2可以看出,Fe3O4在580、489 cm-1出现Fe—O键的特征吸收峰,无其他铁氧化物的特征吸收峰出现,表明样品是纯相Fe3O4。与Fe3O4相比,FLDH55不仅有Fe3O4的两个特征吸收峰,在3 424、1 655、1 450~996、791 cm-1等处出现了新的吸收峰。其中,3 424 cm-1处强而宽的吸收带由羟基伸缩振动和层间水分子伸缩振动重叠而成。1 655 cm-1处的吸收峰对应于水分子的弯曲振动〔20-21〕。1 495、1 428、791、1 362、996 cm-1处的吸收峰分别对应于CO32-的反对称伸缩振动、对称伸缩振动、面外弯曲振动等〔20〕。与纯Mg-Fe-LDH相比,FLDH55中Mg-Fe-LDH结构的相应峰向高波数方向移动,同时,碳酸根分裂峰明显增多,这是由于Mg-Fe-LDH与Fe3O4发生静电相互作用,导致Mg-Fe-LDH结构对称性下降影响引起的。结合XRD表征结果,说明该体系生成了Fe3O4@Mg-Fe-LDH复合物。
图3
表1 系列FLDH XRD参数
| LDH含量/% | d(003)/nm | D(006)/nm | 晶粒尺寸/nm | 分散度/% |
| 0 | - | - | - | - |
| 33 | 7.83 | 3.90 | 11.5 | 8.3 |
| 55 | 7.69 | 3.84 | 15.6 | 6.15 |
| 66 | 7.70 | 3.87 | 16.4 | 5.80 |
| 80 | 7.69 | 3.84 | 16.7 | 5.74 |
注:晶粒尺寸对应于2θ=11.2°(003)晶面,利用谢乐公式计算;分散度参考文献〔
2.2 吸附研究
2.2.1 Mg-Fe-LDH含量对Fe3O4@ Mg-Fe-LDH吸附MO的影响
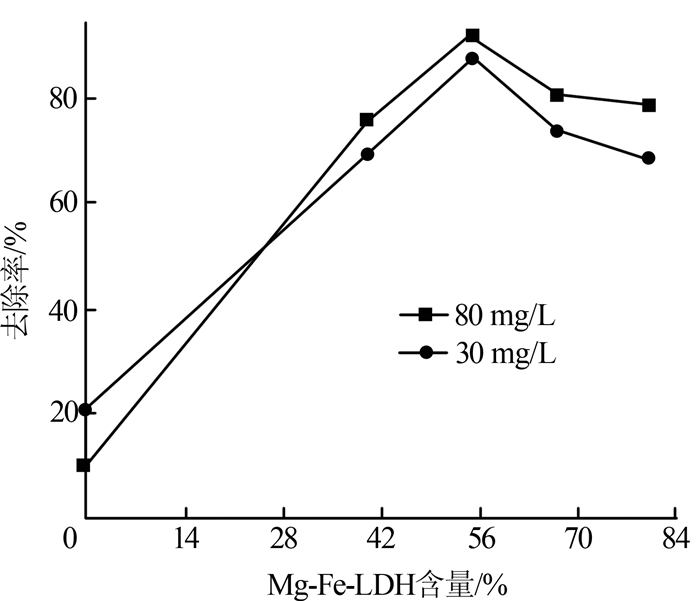
在36 ℃、pH=7.0条件下,以甲基橙初始质量浓度分别为30、80 mg/L为例研究了Mg-Fe-LDH包覆量对Fe3O4@ Mg-Fe-LDH吸附MO的影响,结果见图4。
图4
由图4可知,Fe3O4对MO的吸附率很低,MO两种初始浓度时的去除率分别为21.1%、15.5%;随着四氧化三铁表面包覆Mg-Fe-LDH量的增加,Mg-Fe-LDH在Fe3O4表面分散程度逐渐下降,晶化程度提高,磁性复合物对甲基橙的吸附量呈现出先增加后降低的趋势。当四氧化三铁表面包覆Mg-Fe-LDH的质量分数为55%(FLDH55)时,吸附效果最佳。MO两种初始质量浓度(30、80 mg/L)时的去除率分别为88%、92.5%。因此,这里对FLDH55做了进一步研究。
2.2.2 吸附溶液pH的影响
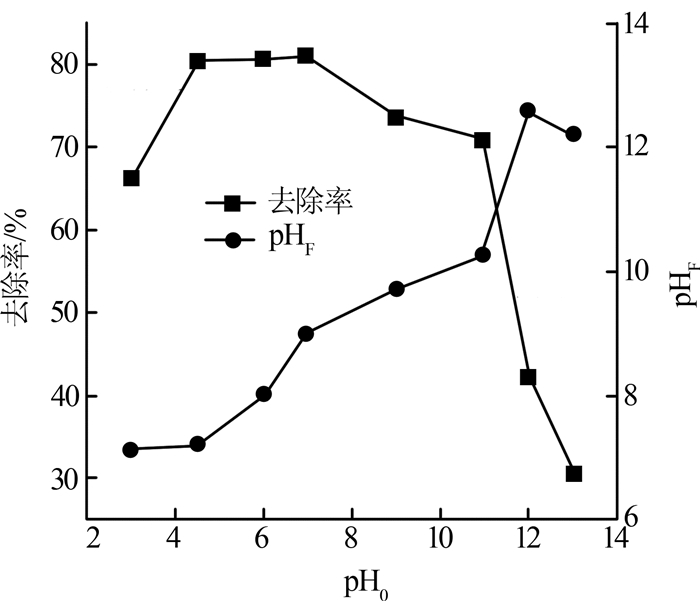
图5反映了FLDH55对MO的去除率随溶液初始pH(pH0)的变化及吸附反应结束后溶液的pH(pHF),其中温度36 ℃、MO初始质量浓度80 mg/L。
图5
由图5可以看出,当吸附溶液的pH超过11~12或者pH≤4.5时FLDH55对MO的去除率急剧下降。这可以从以下两方面进行解释。Mg-LDH的表面零电荷pH(pHpzc)约为12〔24-25〕。当溶液pH>pHpzc时,FLDH55表面带负电荷,MO是含磺酸根的水溶性阴离子型染料,故二者之间产生静电斥力,导致FLDH55对MO的吸附率骤然下降。当吸附溶液的pH为12~13时,吸附率分别下降至40%、25%。pH越高,吸附率越低。利用高pH吸附率低的特点可以实现Fe3O4@Mg-Fe-LDH的回收、再利用。当溶液pH≤4.5时,MO的磺酸根部分质子化,使得带正电荷的FLDH55与MO间的静电吸引作用减弱,吸附量下降。
吸附反应结束后溶液的pH明显高于相应的pH0。这是由于甲基橙与吸附剂FLDH55中含有的氢氧根和碳酸根发生离子交换的原因。其中,当pH0介于4.5~7.0时,pHF位于7~9,对吸附设备的腐蚀较小。因此,FLDH55对MO的最佳吸附在pH0 4.5~7.0。
2.2.3 甲基橙初始浓度的影响及吸附等温线
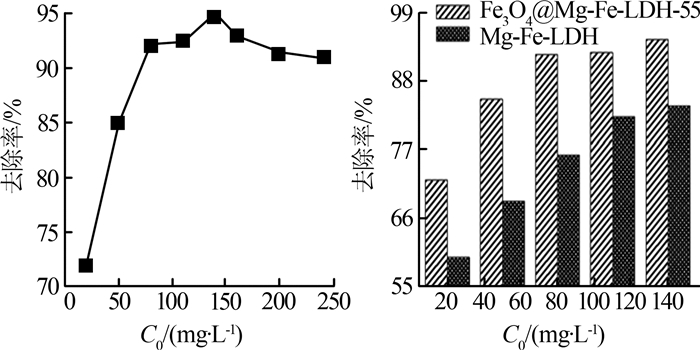
图6反映了FLDH55对甲基橙的去除率随甲基橙初始浓度(C0)变化的过程。
图6
随着C0的增加,MO的吸附率呈现先增加后降低趋势。这是因为C0在一定范围内增加可以提高染料分子与FLDH55之间静电吸引的推动力。但是,当FLDH55表面吸附MO达到饱和后,C0进一步增加会导致其吸附率下降。当C0=140 mg/L时,FLDH55对MO吸附率达到最大(94.5%)。
同时比较了FLDH55和Mg-Fe-LDH两种材料在C0为20~140 mg/L时对MO的去除率比较。结果表明,同样条件下FLDH55对MO的去除率明显高于Mg-Fe-LDH。这是由于Mg-Fe-LDH在Fe3O4表面生长过程中有效地抑制了其本身的团聚和晶化,提高了Mg-Fe-LDH的分散度(具体数据见表1),增加了Mg-Fe-LDH接触溶液中MO分子的机会。
将图6中的数据进一步处理得到FLDH55对MO的吸附等温线,再分别用Langmuir模型和Freundlich模型对吸附等温线中的数据处理,得到相关吸附参数,其中Langmuir和Freundlich模型拟合所得R2值分别为0.994、0.985。由此可知,FLDH55对MO的吸附规律更符合Langmuir模型,说明MO在Fe3O4@Mg-Fe-LDH上的吸附为单分子层吸附,且拟合结果表明,吸附温度为36 ℃时,FLDH55对MO饱和吸附量为3 242.5 mg/g,明显高于相同温度下传统吸附剂如活性炭(11.2 mg/g)和金属有机骨架材料(MOF235)(447 mg/g)对MO的饱和吸附量〔26〕。
3 结论
采用两步法制备的FLDH因Fe3O4表面包覆Mg-Fe-LDH质量的不同使其吸附MO性能具有明显差异。当Fe3O4表面包覆Mg-Fe-LDH的质量分数为55%、吸附溶液的pH控制在4.5~7.0,FLDH对MO的吸附效果最佳。FLDH55对不同初始浓度的MO吸附率明显高于Mg-Fe-LDH本身。吸附温度为36 ℃时,FLDH55对MO饱和吸附量为3 242.5mg/g,明显高于传统吸附剂对MO的去除效果。因此,Fe3O4@Mg-Fe-LDH磁性复合物作为水中有机污染物的吸附剂具有重要的研究意义和潜在应用前景。
参考文献
The challenge of micropollutants in aquatic systems
[J].DOI:10.1126/science.1127291 [本文引用: 1]
Ferrihydrite preparation and its application for removal of anionic dyes
[J].
Removal of methylene blue by two zeolites prepared from naturally occurring Egyptian kaolin as cost effective technique
[J].DOI:10.1016/j.solidstatesciences.2011.07.016
Templated preparation of porous magnetic microspheres and their application in removal of cationic dyes from wastewater
[J].
Electrochemical degradation of remazol red BR and novacron blue C-D dyes using diamond electrode
[J].
Removal of natural organic matter from drinking water by advanced oxidation processes
[J].DOI:10.1016/j.chemosphere.2010.04.067 [本文引用: 1]
Low-field magnetic separation of monodisperse Fe3O4 nanocrystals
[J].DOI:10.1126/science.1131475 [本文引用: 1]
The effect of nanocrystalline magnetite size on arsenic removal
[J].
Removal and recovery of Cr(Ⅵ) from wastewater by maghemite nanoparticles
[J].DOI:10.1016/j.watres.2005.05.051 [本文引用: 1]
Magnetic permanently confined micelle arrays for treating hydrophobic organic compound contamination
[J].DOI:10.1021/ja806556a [本文引用: 1]
A facile method to fabricate carbon-encapsulated Fe3O4 core/shell composites
[J].DOI:10.1088/0957-4484/18/3/035602 [本文引用: 1]
Facile method to synthesize magnetic iron oxides/TiO2 hybrid nanoparticles and their photodegradation application of methylene blue
[J].
General and controllable synthesis of novel mesoporous magnetic iron Oxide@Carbon encapsulates for efficient arsenic removal
[J].
Study on formation mechanism by monitoring the morphology and structure evolution of nearly monodispersed Fe3O4 Submicroparticles with controlled particle sizes
[J].
纳米Fe3O4/膨润土的制备、表征及光催化降解焦化废水
[J].DOI:10.3969/j.issn.1003-6504.2013.04.031 [本文引用: 1]
Magnetic mesoporous clay adsorbent:Preparation, characterization and adsorption capacity for atrazine
[J].DOI:10.1016/j.micromeso.2014.03.038 [本文引用: 2]
Structural aspects of layered double hydroxides
[J].
Incorporation of Fe3+ into Mg/Al layered double hydroxide framework:effects on textural properties and photocatalytic activity for H2 generation
[J].DOI:10.1039/c2jm15658j [本文引用: 2]
Catalytic performance of a three-dimensionally ordered macroporous Co/ZrO2 catalyst in Fischer-Tropsch synthesis
[J].DOI:10.1016/j.molcata.2012.03.024 [本文引用: 2]
Cobalt supported on Zr-modified SiO2 as an efficient catalyst for Fischer-Tropsch synthesis
[J].DOI:10.1039/C7RA01756A [本文引用: 1]
Nearly monodispersed core-shell structural Fe3O4@DFUR-LDH submicro particles for magnetically controlled drug delivery and release
[J].
Removal of fluoride ions from aqueous solution by the calcination product of Mg-Al-Fe hydrotalcitelike compound
[J].
Adsorptive removal of methyl orange and methylene blue from aqueous solution with a metal-organic framework Material, iron terephthalate(MOF-235)
[J].DOI:10.1016/j.jhazmat.2010.09.035 [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号