苯酚废水毒性大、难以处理,排放到自然环境中会对自然环境和人类健康安全造成巨大危害〔1〕。针对难降解有机物,高级氧化技术(AOPs)通过反应体系持续产生具有强氧化性的·OH、SO4·-,进而达到氧化降解有机物的目的〔2-4〕。单独加入臭氧、过硫酸盐等氧化剂不能取得较好的降解效果,需加入催化剂促进反应进行〔5-6〕。在AOPs技术中,主要采用过渡金属作为催化剂,分为均相催化剂和非均相催化剂。均相催化剂主要应用钴、铁、锰离子等,虽然处理效果好,但残存离子会造成水体二次污染;非均相催化剂对单一金属氧化物研究较多,而对多元复合氧化物的报道相对较少〔7-8〕。铁锰复合氧化物,由于铁锰之间能够产生协同效应,进而有效活化过硫酸氢钾(PMS)生成自由基,提高对水中有机物的降解〔9-10〕。笔者使用溶胶凝胶法制备了铁锰复合氧化物粉体,之后将复合氧化物粉体负载至无定型硅铝载体上,得到成型的铁锰催化剂,并研究了该催化剂活化PMS去除水中苯酚的效果。
1 实验部分
1.1 原料和试剂
氯化铁、高锰酸钾、硝酸(65%~68%)、苯酚、氢氧化钠、乙酸、乙酸钠、稀硫酸,均为分析纯,天津光复精细化工研究所;葡萄糖,分析纯,国药集团化学试剂有限公司;纳米二氧化硅粉(平均粒径20 nm),上海超威纳米科技有限公司;拟薄水铝石(固含量60%),山东英朗化工有限公司;PMS(2KHSO5·KHSO4·K2SO4),西格玛奥德里奇(上海)贸易有限公司;去离子水为实验室自制。
1.2 催化剂的制备
按照n(KMnO4):n(C6H12O6):n(FeCl3)=1:2:1,称取药品溶解于去离子水中,并持续搅拌4 h;将溶液放入带有聚四氟乙烯内衬的高压反应釜,在150 ℃的条件下水热反应12 h,之后分离、水洗、干燥得到复合氧化物前驱物;将前驱体放入马弗炉,以10 ℃/min的速率升至500 ℃,并保持该温度煅烧2 h,得到铁锰氧化物粉体;按照n(KMnO4):n(C6H12O6)=1:1,n(FeCl3):n(C6H12O6)=1:1,应用上述方法制备三氧化二锰(Mn2O3)、四氧化三铁(Fe3O4)粉体。将铁锰氧化物粉体、纳米二氧化硅粉和拟薄水铝石按照质量比6:1:1进行混合,加入适量硝酸和氢氧化钠使之变为可塑形态,之后挤条、干燥,然后以10 ℃/min的速率升至500 ℃,并保持该温度煅烧2 h,得到成型的铁锰催化剂产品,催化剂直径为2.5 mm,平均长度为10 mm。文中催化剂活性评价实验所用催化剂均为粉体催化剂,其余实验均采用成型的铁锰催化剂产品。
1.3 催化剂的表征
所制备的催化剂使用X射线衍射分析仪(D/max-250,日本理学株式会社)表征其晶相结构和结晶度;使用扫描电子显微镜(SEM,S-4800,Hitachi)来观测其表面形貌;使用物理吸附仪(ASAP2405,Micromeritics)采用BET法进行催化剂比表面积和孔体积的计算。
1.4 催化剂的活性评价实验方法
向带温控搅拌的反应釜中加入一定量的去离子水、苯酚、PMS和催化剂,考察苯酚浓度、PMS浓度和催化剂投加量对苯酚降解效果的影响。反应液中苯酚浓度的测量,按照4-氨基安替比林直接光度法,使用分光光度计(UV5,梅特勒)测量,根据反应前后苯酚浓度的变化计算苯酚去除率。
2 结果与分析
2.1 催化剂的表征
所制备的铁锰催化剂的SEM照片如图 1所示。
图1
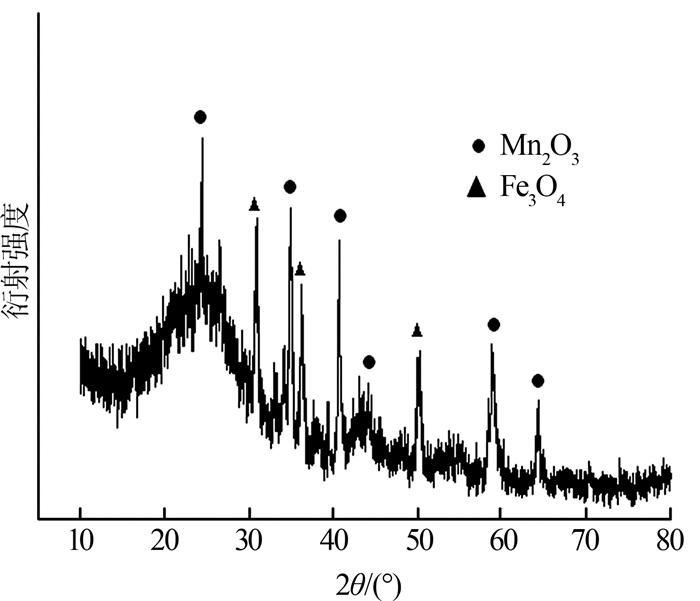
图2
从图 2可以看出,铁锰催化剂的XRD图上有明显的Fe3O4、Mn2O3特征峰。在水热反应的过程中,KMnO4和FeCl3先与葡萄糖发生氧化还原反应,生成MnCO3和FeCO3的前驱体,之后进行煅烧生成纳米Mn2O3和Fe3O4。XRD图在20°~30°间出现明显的弥散峰型,这是因为在催化剂成型过程中加入了硅铝氧化物作为黏结剂,出现了无定型结构。BET数据显示,按1.2中方法制备的成型铁锰催化剂、铁锰氧化物粉体的比表面积分别为187.3、91.9 m2/g,孔体积0.753、0.257 cm3/g。可以看出,成型之后的催化剂比表面积和孔体积都相应增大,这是因为成型催化剂中含有比表面积和孔容较大的无定形硅铝氧化物。
2.2 催化剂活性评价
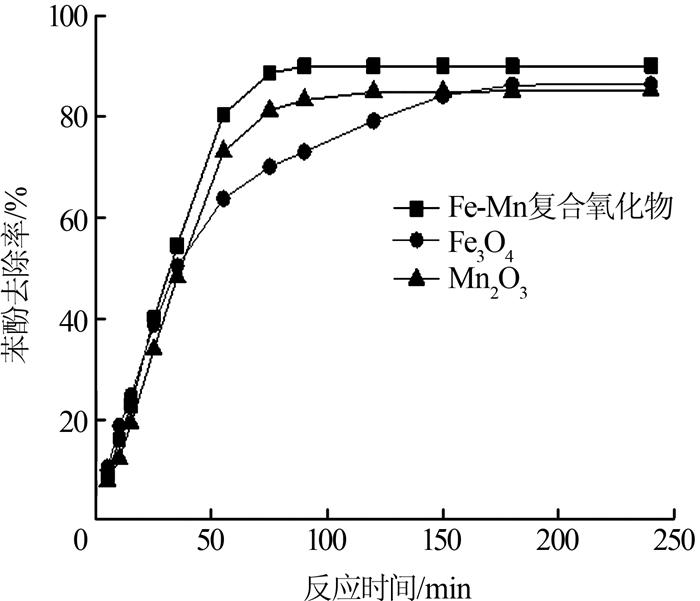
控制苯酚废水水温为25 ℃,初始pH为5,苯酚质量浓度30 mg/L,PMS质量浓度为2.0 g/L,铁锰催化剂、Fe3O4、Mn2O3的投加质量浓度分别为0.5 g/L,考察三种金属氧化物活化PMS降解苯酚的效果,结果见图 3。
图3
由图 3可知,制备的铁锰催化剂在反应时间为90 min时,体系中苯酚的去除率为90.06%,继续延长反应时间至240 min,苯酚去除率没有明显上升;而Fe3O4粉体在反应时间为90 min时,苯酚去除率为73.12%,随着反应时间延长,苯酚去除率逐渐上升,最终在240 min时去除率达到86.49%。Fe3O4活化PMS降解苯酚的速率较慢,这是因为Fe2+/Fe3+循环较慢,导致活化过硫酸盐的效率降低;而铁锰复合氧化物中,由于Mn3+的存在,不仅可以活化PMS,而且可以将Fe3+还原成Fe2+,促进了Fe2+/Fe3+循环;另一方面,Fe2+的存在,又可以将Mn3+还原成Mn2+,促进了Mn2+/Mn3+循环,Fe和Mn之间的协同效应增强了活化PMS的效率,使苯酚的降解速率和降解效果得到了提升。
控制苯酚废水水温25 ℃,初始pH为5,苯酚质量浓度30 mg/L,反应时间90 min,考察单独使用PMS、铁锰催化剂以及铁锰催化剂和PMS联合使用对苯酚的降解效果。结果表明,使用铁锰催化剂对PMS进行活化,对苯酚的去除率达到了90.59%;单独使用PMS的苯酚去除率为5.41%,降解效果不明显;单独使用催化剂的前5 min,苯酚去除率为5.67%;而反应结束后苯酚去除率仅为6.58%,无明显上升,这可能是因为催化剂具有较大的比表面积,吸附了一部分溶液中的苯酚,而催化剂本身对苯酚没有明显的降解作用。
2.3 铁锰催化剂投加量对降解效果的影响
控制苯酚废水水温25 ℃,初始pH为5,苯酚质量浓度30 mg/L,PMS质量浓度2.0 g/L,反应时间90 min,考察铁锰催化剂投加量对苯酚降解效果的影响,结果见图 4。
图4
由图 4可知,随着铁锰催化剂投加质量浓度从0.1 g/L上升至0.5 g/L,反应时间为90 min时,苯酚去除率由57.41%上升至90.59%,降解速率明显增加,这是由于增加催化剂投加量提升了其对PMS的活化速率;而投加质量浓度继续上升到1.0 g/L,反应时间为90 min时,苯酚去除率仅上升至91.67%,没有明显提高,这是因为体系中PMS的浓度和苯酚浓度是固定的,增大催化剂的投加量虽然能提高降解速率,但固定反应时间内降解苯酚的总量却不能提高。所以,针对上述体系,铁锰催化剂投加质量浓度以0.5 g/L为宜。
2.4 PMS浓度对降解效果的影响
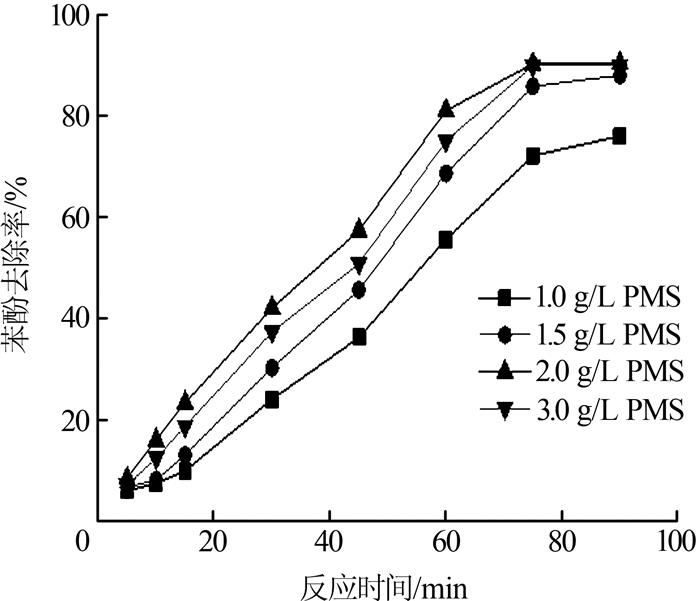
控制苯酚废水水温25 ℃,初始pH为5,苯酚质量浓度30 mg/L,铁锰催化剂投加质量浓度0.5 g/L,反应时间90 min,考察PMS浓度对苯酚降解效果的影响,结果见图 5。
图5
2.5 苯酚初始浓度对降解效果的影响
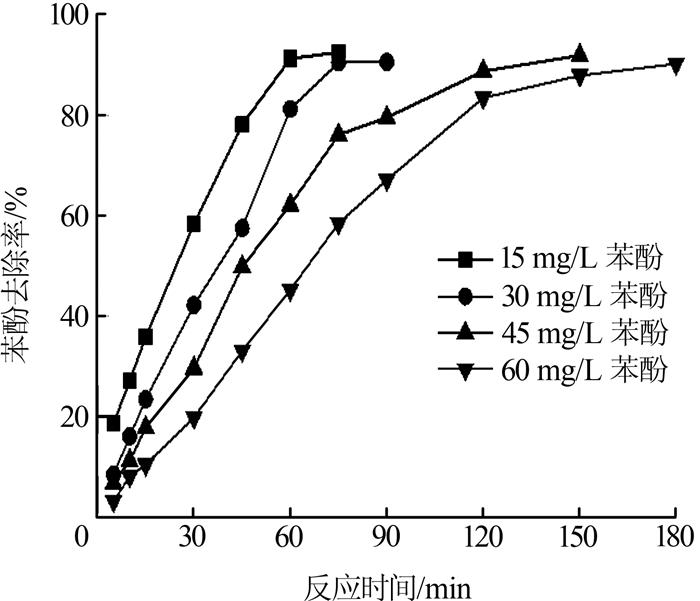
控制苯酚废水水温25 ℃,初始pH为5,铁锰催化剂投加质量浓度0.5 g/L,PMS质量浓度2.0 g/L,反应时间90 min,考察苯酚初始浓度对苯酚降解效果的影响,结果见图 6。
图6
由图 6可知,随着苯酚初始质量浓度从15 mg/L上升至60 mg/L,苯酚去除率达到90%以上需要的反应时间逐渐增大。这是因为PMS的浓度和催化剂投加量是固定的,产生的SO4·-浓度也是固定的,所以相同的反应时间,只能降解溶液中固定量的苯酚。
2.6 初始pH对降解效果的影响
控制苯酚废水水温25 ℃,苯酚质量浓度30 mg/L,PMS质量浓度2.0 g/L,铁锰催化剂投加质量浓度0.5 g/L,反应时间90 min,考察初始pH对苯酚降解效果的影响。结果表明,当初始pH由3上升至5,苯酚去除率从90.13%升至90.59%,提升并不明显;但当初始pH大于5时,随着pH的升高苯酚去除率会相应降低,这是由于制备的铁锰催化剂表面的等电点经过检测为5.23,当溶液中pH大于该值时,会使催化剂表面带负电荷,使其与HSO5-产生排斥,进而使催化剂活化PMS的效果下降〔12〕。考虑到当pH分别为3和5的条件下,苯酚降解效果变化不大,所以选择pH=5为该过程的最佳初始pH。
2.7 铁锰催化剂的重复使用性能
控制苯酚废水水温25 ℃,初始pH为5,苯酚质量浓度30 mg/L,PMS质量浓度2.0 g/L,铁锰催化剂投加质量浓度0.5 g/L,反应时间90 min,考察该催化剂重复使用对苯酚降解效果的影响。催化剂使用后,使用去离子水进行清洗,直至洗液为中性,再将催化剂加入反应体系中进行重复性试验。结果表明,经过5次循环实验,苯酚去除率仍保持在80%以上,表明所制备铁锰催化剂均有优异的稳定性和重复使用性。
3 结论
(1)使用溶胶凝胶法制备了纳米铁锰复合金属氧化物,通过将复合氧化物粉末、黏结剂及其他助剂按一定比例混合成可塑形态,通过挤条、干燥、煅烧得到成型催化剂。催化剂主要成分为Fe3O4和Mn2O3,金属氧化物平均粒径为100 nm左右,分散均匀,无明显团聚现象。且由于硅铝作为黏结剂的加入,使其出现无定形结构,使成型催化剂具有较高的比表面积和孔容。
(2)在25 ℃,PMS质量浓度为2.0 g/L,铁锰催化剂投加质量浓度为0.5 g/L,苯酚质量浓度为30 mg/L,反应时间为90 min的条件下,苯酚的去除率达到90.59%,显示出对苯酚良好的处理效果;催化剂经过5次循环,苯酚去除率仍保持在80%以上,表明该催化剂具有优异的稳定性和重复使用性。
参考文献
高级氧化技术处理染料废水的研究进展
[J].DOI:10.3969/j.issn.1005-829X.2006.06.001 [本文引用: 1]
Oxidation of Orange G by persulfate activated by Fe(Ⅱ), Fe(Ⅲ) and zero valent iron(ZVI)
[J].DOI:10.1016/j.chemosphere.2013.12.037 [本文引用: 1]
Facile synthesis of CoFe2O4 magnetic nanomaterial by natural cellulose template and catalytic performance in heterogeneous activation of peroxymonosulfate
[J].DOI:10.1007/s10971-019-05118-9 [本文引用: 1]
Oxidation of bisphenol A by persulfate via Fe3O4-α-MnO2 nanoflower-like catalyst:Mechanism and efficiency
[J].DOI:10.1016/j.cej.2018.09.179 [本文引用: 1]
Degradation of acetaminophen with ferrous/copperoxide activate persulfate:Synergism of iron and copper
[J].
Co-SBA-15 for heterogeneous oxidation of phenol with sulfate radical for wastewater treatment
[J].DOI:10.1016/j.cattod.2011.03.005 [本文引用: 1]







 津公网安备 12010602120337号
津公网安备 12010602120337号