本研究以有机砷(ROX)及其降解产物无机砷〔As(Ⅲ)/As(Ⅴ)〕为一体的复合污染废水为研究对象,运用高铁酸钾作为多功能氧化处理剂处理ROX和As(Ⅲ)/As(Ⅴ)复合污染废水,考察反应时间、pH、温度、高铁酸钾投加量以及不同碱性物质对复合污染废水治理效果的影响,并初步探讨了氧化机理。以期为有机物与重金属复合污染废水的治理技术与机理的探索提供先导性作用。
1 材料与方法
1.1 仪器与试剂
主要仪器:Primaide型高效液相色谱仪(日本日立);AFS-2202E型双道原子荧光光度计(北京海光仪器公司)。
主要试剂:高铁酸钾(上海麦克林)、洛克沙胂、砷酸钠、亚砷酸钠(东京化成工业株式会社)均为分析纯。
1.2 实验方法
配制100 mg/L ROX+10 mg/L As(Ⅲ)+10 mg/LAs(Ⅴ)的砷复合污染混合溶液,其中2种无机砷浓度为单一元素浓度。取250 mL复合污染物质加入到500 mL锥形瓶中,调节pH至4左右,加入一定量的高铁酸钾,迅速震摇,充分混合后,再次调节pH至4左右,放入摇床,在室温下匀速震荡。
2 结果与讨论
2.1 处理砷复合污染废水前后高铁酸钾的XRD
处理废水前后处理剂高铁酸钾的XRD见图 1。
图1
由图 1可知,通过MDI jade 6软件对比,发现Fe2O3(33-0664)的特征峰与高铁酸钾中的尖峰完全一致,说明高铁酸钾直接水解后有结晶度良好的Fe2O3形成,同时馒头峰的出现也说明有结晶度不好的沉淀物FeOOH(18-0639)形成,高铁酸钾处理废水后,Fe2O3(33-0664)的特征峰消失,说明高铁酸钾加入含砷复合污染废水后,其水解所生成的Fe2O3与砷发生了化学反应,形成了结晶度比较差的铁砷化合物,通过MDI jade 6软件与参考文献对比,发现FeAsO4特征峰与图中的馒头峰相吻合,这个馒头峰的位置与高铁酸钾直接水解后所形成的结晶度不好的沉淀物FeOOH(18-0639)有重合,但通过仔细分析,在FeAsO4特征峰的位置,处理废水后高铁酸钾的峰强度高于处理前,所以可以推测高铁酸钾用于处理砷复合污染废水后新生成了结晶度不好的FeAsO4。
2.2 反应时间对砷复合污染废水处理效果的影响
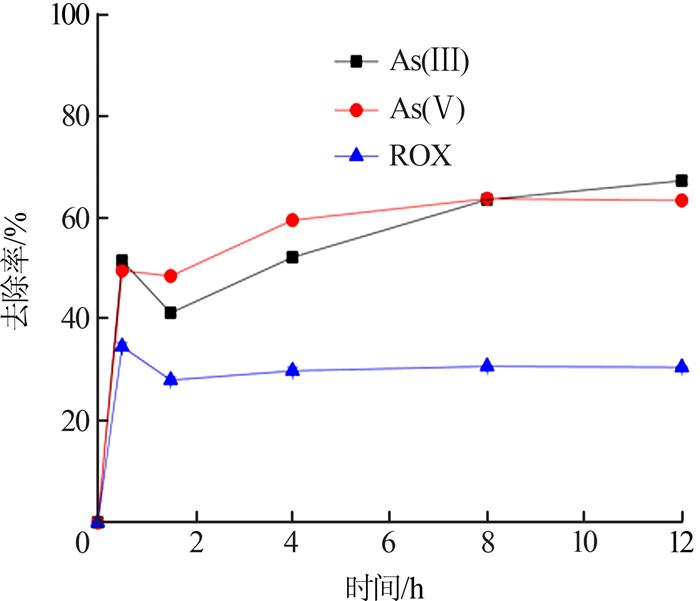
在锥形瓶中加入铁砷质量比为10:1的高铁酸钾迅速摇匀后,调节pH为4,在30 ℃下进行恒温震摇,分别在0.5、1.5、4、8、12 h这5个不同时间段取样,考察反应时间对复合污染废水处理效果的影响,结果见图 2。
图2
由图 2可知,3种污染物的去除过程可以分为氧化阶段和吸附阶段〔11〕,且反应时间对氧化吸附反应影响较大。0~0.5 h内3种污染物质的去除率随反应时间增加而快速提高;而在0.5~1.5 h时,3种污染物质的去除率随反应时间增加而略有降低,这是由于0.5 h内污染物与高铁酸钾试剂发生氧化反应,在该阶段主要是有机砷ROX和无机砷As(Ⅲ)分别被高铁酸钾氧化,导致其去除率明显增加,与此同时高铁酸钾被还原成多羟基氧化铁。0.5~1.5 h范围内,污染物质的去除率均有所下降,这可能是因为高铁酸钾在初始阶段快速发生氧化反应和自分解反应产生的FeOOH和Fe2O3包裹和封闭了部分污染物。这部分污染物随着Fe2O3与体系中无机砷逐步反应生成砷酸铁而逐渐被释放出来。在该过程中FeOOH去除的砷量少于由于消除包裹效应所放出砷的量,由此污染物质的去除率小幅下降;而在1.5 h后,随着反应时间的增加,去除率逐渐增加,体系中的Fe3+与污染物质发生化学反应所生成的铁砷共沉淀协同FeOOH吸附共同去除污染物。8 h后,3种污染物的去除率趋近于平衡且达到最大值,因此,确定反应时间为8 h。
2.3 pH对砷复合污染废水处理效果的影响
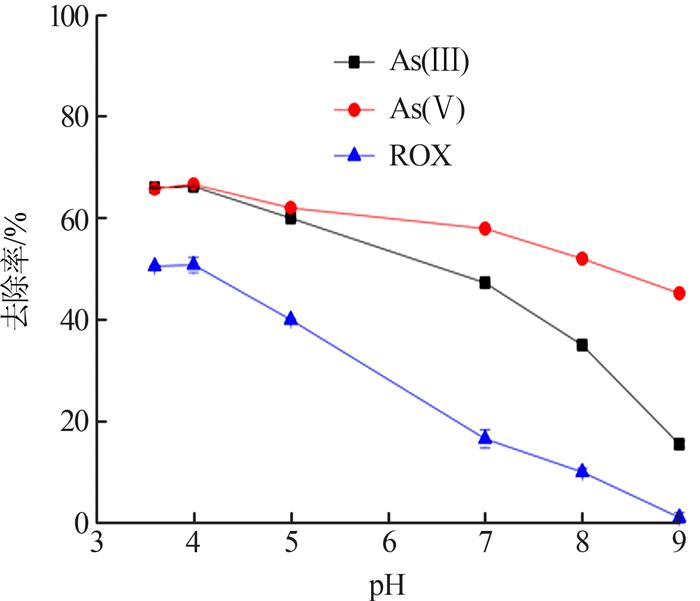
30 ℃下,铁砷质量比为10:1,在锥形瓶中加入高铁酸钾迅速摇晃均匀后,再次将pH分别调节为3、4、5、7、9,震摇8 h后取样,考察pH对复合污染废水处理效果的影响,结果见图 3。
图3
2.4 温度对砷复合污染废水处理效果的影响
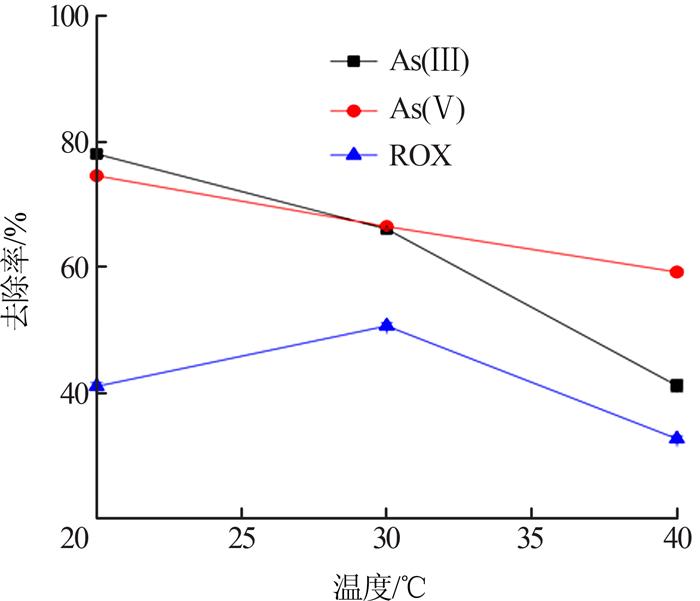
铁砷质量比为10:1,取样时间为8 h,在锥形瓶中加入高铁酸钾迅速摇匀后,调节pH为4,分别在20、30、40 ℃下进行恒温震摇,考察温度对复合污染废水处理效果的影响,结果见图 4。
图4
由图 4可知,随着温度的升高,2种无机砷的去除率均呈下降的趋势,而ROX的去除率则先升高再降低,在30 ℃时达到最大值,对无机砷而言,在一定温度范围内较低的温度更有利于促进其吸附去除。而对ROX,30 ℃时去除效果更好。这可能是由于温度升高,促进了高铁酸钾与ROX的反应,因此其去除率升高,而由于反应生成了较多的As(Ⅴ),故As(Ⅴ)的去除反而降低。同时,在40 ℃时,较之30 ℃时高铁酸钾对ROX的去除率降低,是由于高铁酸钾本身温度越高越不稳定,导致体系中Fe6+有效含量降低,吸附起的作用更大,因此40 ℃时符合温度对吸附的影响,该吸附过程应属于放热反应,温度越低,吸附效果越好。由理论上计算可知,若完全降解,100 mg/LROX大约会产生28.48 mg/L As(Ⅴ)。由图 4可知,ROX的去除率在30 ℃时比20 ℃增加了9.66%,约会产生2.75 mg/L的As(Ⅴ),无机总砷的去除率在30 ℃时比20 ℃降低了10%,约2 mg/L的无机砷。也就是说,无机砷的来源有两处:一处是初始添加的,另一处是ROX降解所产生的。30 ℃时相较于20 ℃时多降解的ROX理应生成了2.75 mg/L无机砷,但无机总砷只少了2 mg/L,虽然无机总砷在20 ℃时测得的去除率更高,但由此可知无机总砷在30 ℃时比20 ℃去除得更多,因此,将温度设为30 ℃较为合理。
2.5 高铁酸钾投加量对砷复合污染废水处理效果的影响
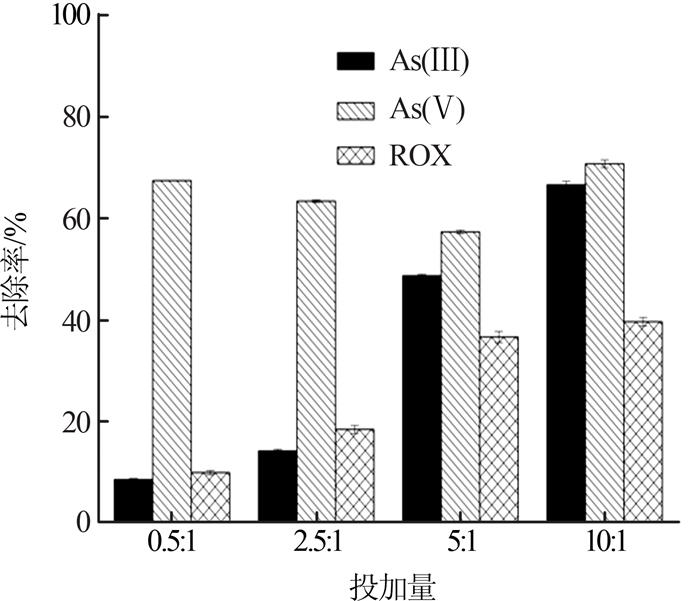
加入铁砷质量比分别为0.5:1,2.5:1,5:1,10:1的高铁酸钾迅速摇匀后,调节pH为4,在30 ℃下进行恒温震摇,8 h后取样,考察高铁酸钾投加量对复合污染废水处理效果的影响,结果见图 5。
图5
由图 5可知,随着铁砷质量比的增大,砷复合污染废水中无机砷的去除率明显升高。在铁砷质量比为5:1之前,As(Ⅴ)的去除率在逐渐下降,而As(Ⅲ)的去除率在迅速升高。众所周知,高铁酸盐去除As(Ⅲ)的机理就是将As(Ⅲ)氧化为As(Ⅴ)后,进行化学吸附或者物理吸附来去除。体系中的As(Ⅴ)可能有3个来源,即母液原有的As(Ⅴ)、As(Ⅲ)及洛克沙砷被高铁酸钾氧化后的生成物。由此可知,在某段时间内,溶液中会出现较多As(Ⅴ),却无法被及时地吸附去除,此时便会出现污染物质增多的现象。在铁砷质量比为10:1时,As(Ⅴ)去除率增大,残留液中As(Ⅴ)减少,说明污染物质浓度不变的情况下,此时的氧化剂投加量能够在有效氧化As(Ⅲ)同时吸附过多的As(Ⅴ)。铁砷质量比为5:1与10:1时,残留砷的浓度相差不大,说明了铁砷质量比为10:1时,ROX的被氧化量已经接近于饱和。当高铁酸钾增多,被还原生成的Fe3+越多,产生的FeOOH越多,被去除的无机砷污染物也就越多,总砷去除效果越好,结合经济与实际反应用量等因素,实验选用投加铁砷质量比为10:1的高铁酸钾。
2.6 不同碱对砷复合污染废水处理效果的影响
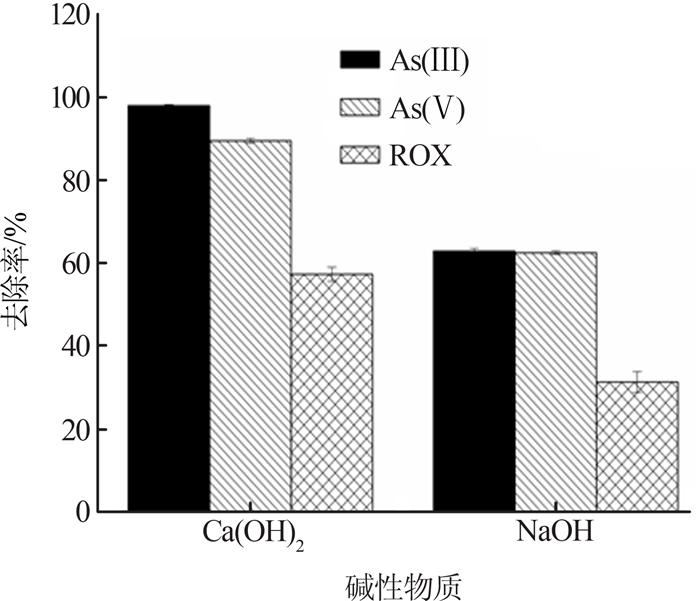
加入铁砷质量比为10:1的高铁酸钾迅速摇匀后,分别以NaOH-HCl和Ca(OH)2-HCl将复合污染废水的pH调节为4,在30 ℃下进行恒温震摇,8 h后取样。考察了不同碱性物质调节pH对复合污染废水去除效果的影响,结果见图 6。
图6
在最优条件下,即pH为4左右,温度为20~30 ℃,铁砷质量比达到10:1时,调节pH的碱性物质为Ca(OH)2,无机总砷和ROX综合去除效果最好。
2.7 氧化动力学
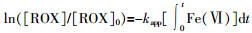
式中,kapp表示高铁酸钾与ROX反应的表观二级反应动力学速率常数。由于高铁酸钾在水溶液中不稳定,故采用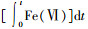
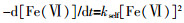
拟合结果表明,pH为4时高铁酸钾氧化降解ROX的表观二级反应动力学速率常数为0.000 18,其相关系数为0.906 03。由于高铁酸钾这种物质本身稳定性很差,因此,相关系数为0.9以上将视作拟合效果良好。
由上述影响条件实验结果、XRD以及氧化动力学综合分析表明,高铁酸钾加入含砷复合污染废水后,其极强的氧化性使得ROX与As(Ⅲ)氧化,将ROX降解生成无机砷;另一方面,高铁酸钾水解生成了FeOOH与Fe2O3,这些固体在液体中起到絮凝的作用,并且Fe2O3与砷发生了化学反应,形成了铁砷化合物FeAsO4。
3 结论
以质量浓度为100 mg/L ROX+10 mg/L As(Ⅲ)+10 mg/L As(Ⅴ)的砷复合污染废水为研究对象,探讨了不同条件对高铁酸钾氧化和吸附砷复合污染废水的影响。结果表明:在pH为4,温度为30 ℃,铁砷质量比达到10:1时,调节pH的碱性物质为Ca(OH)2,无机总砷和ROX综合去除效果最好,由影响条件、XRD以及氧化动力学协同阐释了高铁酸钾同时去除有机砷与无机砷复合污染废水的机理:高铁酸钾加入含砷复合污染废水后,其极强的氧化性使得ROX与As(Ⅲ)氧化,将ROX降解生成无机砷;另一方面,高铁酸钾水解生成了FeOOH与Fe2O3,这些固体在液体中起到絮凝的作用,并且Fe2O3与砷发生了化学反应,形成了铁砷化合物FeAsO4。
参考文献
Simultaneous redox conversion and sequestration of chromate(Ⅵ) and arsenite(Ⅲ) by iron(Ⅲ)-alginate based photocatalysis
[J].
Fast transformation of roxarsone into toxic arsenic species with ferrous iron and tetrapolyphosphate
[J].DOI:10.1007/s10311-018-00831-3
Sorption mechanisms of arsenate on Mg-Fe layered double hydroxides:A combination of adsorption modeling and solid state analysis
[J].DOI:10.1016/j.chemosphere.2016.11.031 [本文引用: 1]
Fate of roxarsone during biological nitrogen removal process in wastewater treatment systems
[J].DOI:10.1016/j.cej.2014.06.030 [本文引用: 1]
高铁酸钾处理含砷废水
[J].DOI:10.3321/j.issn:1009-606X.2009.06.013 [本文引用: 1]
高铁酸钾去除饮用水中2, 6-二氯-1, 4-苯醌的研究
[J].DOI:10.3969/j.issn.1006-4303.2018.03.018 [本文引用: 1]
Effect of roxarsone metabolites in chicken manure on soil biological property
[J].DOI:10.1016/j.ecoenv.2019.01.017
Highly effective oxidation of roxarsone by ferrate and simultaneous arsenic removal with the in situ formed ferric nanoparticles
[J].DOI:10.1016/j.watres.2018.10.012 [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号