近年来,研究人员针对砷的稳定化、无害化目标研究了多种处理工艺,包括化学沉淀法、物化法等。工业上常用的化学沉淀法可分为中和沉淀法〔4〕、硫化沉淀法〔5〕、混凝沉淀法〔6〕,但上述方法分别存在沉淀不稳定、易产生H2S有毒气体及投加量大、渣中砷品味低等缺点。物化法主要包括离子交换法〔7〕、萃取法〔8〕、膜分离法〔9〕及吸附法等〔10〕,其中离子交换法的处理效果好、设备简单,但不适合处理成分复杂、离子浓度高的水体;萃取法及膜分离法则存在处理量小、成本高等缺点,不适于直接处理大量高砷高酸废水;吸附法主要利用天然吸附材料(如沸石、活性炭等)和人工合成材料(如二氧化锰、活性氧化铝等)吸附水中的砷,但该方法对As(Ⅲ)的选择性较差。上述方法均以分离并形成稳定的砷化合物为目标,很少直接将溶液体系中的砷转化为低毒的单质砷。
笔者研究了水溶液中砷的还原热力学,考察直接将溶液体系中的砷还原为单质砷的可行性,在此基础上用纳米零价铁(nZVI)对铜冶炼废酸中的砷进行直接还原处理,以期得到一种高效、廉价的处理方法。
1 砷的还原热力学
计算As-H2O的热力学,分析水溶液中As的存在形式与组分,计算As-H2O的半电池反应,并绘制相应φ-pH图,为nZVI处理含砷废酸、分离废酸中的砷提供理论指导。
1.1 水溶液中砷的存在形态
As(Ⅲ)的形态主要包括H3AsO3、H2AsO3-、HAsO32-和AsO33-,As(Ⅴ)主要包括H3AsO4、H2AsO4-、HAsO42-和AsO43-。溶液体系中砷的总浓度为As(Ⅲ)与As(Ⅴ)之和,即[As]=[H3AsO3]+[H2AsO3-]+[HAsO32-]+[AsO33-]+[H3AsO4]+[H2AsO4-]+[HAsO42-]+[AsO43-]。
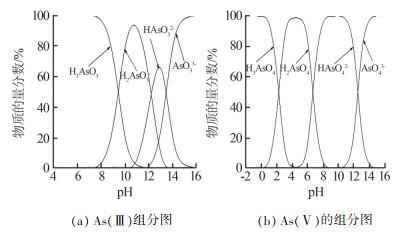
根据As(Ⅲ)、As(Ⅴ)在溶液体系中的解离平衡方程及平衡常数,可得到不同pH下As(Ⅲ)及As(Ⅴ)的组分比例,如图 1所示。
图1
由图 1(a)可知,As(Ⅲ)在溶液体系中主要存在形式为H3AsO3(pH<12)、H2AsO3-(pH在7.1~13.5)、HAsO32-(pH在10.5~16)、AsO33-(pH>11.7)。酸性溶液中,As(Ⅲ)主要以H3AsO3形式存在,存在比例趋于100%;溶液为弱碱性时,H3AsO3解离出H+生成H2AsO3-,H3AsO3的比例随pH的增加而减小;pH约为10.7时H2AsO3-的比例达到最大值93.1%;此后溶液体系中解离出HAsO32-,H3AsO3占比减小,pH接近12时完全消失;pH为12.9时HAsO32-占比最大,为65.9%,随着H3AsO3的消失,AsO33-被解离出来;pH继续增加,HAsO32-不断减少,比例接近0,溶液中最后只剩下AsO33-。
由图 1(b)可知,As(Ⅴ)在溶液体系中主要存在形式为H3AsO4(pH<4)、H2AsO4-(pH在0~8.5)、HAsO42-(pH在4.5~14.6)、AsO43-(pH>10)。H3AsO4的比例随pH的增大而不断减小,pH为4.5时趋于0,此时HAsO42-开始解离出来,比例随pH增大呈现先增大后减小的变化,pH为4.5时达到最大值98.4%;pH为9时,H2AsO4-趋于零,此时HAsO42-达到最大值99.9%,直到pH为10时HAsO42-的比例逐渐减小,AsO43-被解离出来;pH越大,AsO43-的比例越大,最终趋于100%。这也是利用石灰乳中和沉淀法处理含砷废水的原理。
综上,当溶液体系呈强酸性时,As主要以H3AsO3和H3AsO4存在,随着pH的升高砷的存在形态变得更加复杂,强碱性时溶液体系中只存在AsO33-和AsO43-。
1.2 φ-pH图
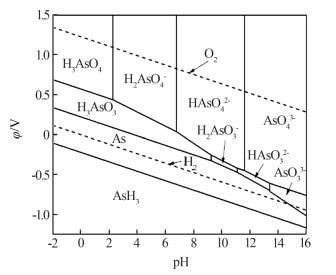
根据砷在溶液体系中可能发生的半电池反应、φ与pH的关系式,绘制出相应的φ-pH图,如图 2所示。
图2
由图 2可知,在As-H2O体系中,随着pH的增大,砷的还原电位减小,说明砷在酸性条件下比碱性条件下更易被还原。在水的稳定区域内,当pH<14.73时,若保持较低的氧化还原电势,单质砷稳定存在的区域较大;若电势升高,稳定物质由单质砷转为三价的含氧酸分子或离子,随pH增大分别为H3AsO3、H2AsO3-、HAsO32-和AsO33-。在较高的氧化还原电势条件下,砷以五价存在,并随pH的增大分别以H3AsO4、H2AsO4-、HAsO42-和AsO43-存在。当溶液pH较小时,体系中的砷以H3AsO3与H3AsO4的形式稳定存在,随着pH的不断增大,H3AsO3与H3AsO4发生不同程度的水解,溶液体系呈碱性时,As(Ⅲ)稳定存在的区域非常小,易被氧化生成As(Ⅴ)。
1.3 热力学参数计算
酸性溶液体系中的砷还原可能存在如表 1所示的化学反应,根据热力学数据可计算出标准状态下反应的ΔrGmΘ、ΔrHmΘ、ΔrSmΘ。
表1 溶液体系中砷还原的标准平衡常数渊298.15 K冤
| 反应式 | ΔrGmΘ/(kJ·mol-1) | ΔrHmΘ/(kJ·mol-1) | ΔrSmΘ/(kJ·mol-1) |
| H3AsO4(aq)+2e+2H+=H3AsO3(aq)+H2O(l) | -110.796 | -125.578 | -0.050 |
| H2AsO4-(aq)+2e+3H+=H3AsO3(aq)+H2O(l) | -123.588 | -118.462 | 0.017 |
| HAsO42-(aq)+2e+4H+=H3AsO3(aq)+H2O(l) | -162.383 | -121.811 | 0.136 |
| HAsO42-(aq)+2e+3H+=H2AsO3-(aq)+H2O(l) | -110.030 | -94.605 | 0.052 |
| HAsO42-(aq)+2e+2H+=HAsO32-(aq)+H2O(l) | -46.638 | -68.650 | -0.074 |
| AsO43-(aq)+2e+3H+=HAsO32-(aq)+H2O(l) | -112.683 | -86.650 | 0.087 |
| AsO43-(aq)+2e+2H+=AsO33-(aq)+H2O(l) | -36.190 | -61.325 | -0.084 |
| H3AsO3(aq)+3e+3H+=As(s)+3H2O(l) | -72.025 | -115.115 | -0.145 |
| H2AsO3-(aq)+3e+4H+=As(s)+3H2O(l) | -124.378 | -142.324 | -0.060 |
| HAsO32-(aq)+3e+5H+=As(s)+3H2O(l) | -187.774 | -168.276 | 0.065 |
| AsO33-(aq)+3e+6H+=As(s)+3H2O(l) | -264.267 | -193.601 | 0.237 |
由表 1可知,砷还原的相关化学反应ΔrGmΘ均<0,表明标准状态下能将砷元素以单质砷的化学形态还原;标准反应焓变ΔrHmΘ<0,说明各反应为放热反应,在低温下可自发进行。
由ΔrGmΘ计算出化学反应的平衡常数KΘ,如表 2所示。
表2 溶液体系中砷还原的标准平衡常数渊298.15 K冤
| 反应式 | lgKΘ | KΘ |
| H3AsO4(aq)+2e+2H+=H3AsO3(aq)+H2O(l) | 20.29 | 1.95×1020 |
| H2AsO4-(aq)+2e+3H+=H3AsO3(aq)+H2O(l) | 22.63 | 4.27×1022 |
| HAsO42-(aq)+2e+4H+=H3AsO3(aq)+H2O(l) | 29.74 | 5.50×1029 |
| HAsO42-(aq)+2e+3H+=H2AsO3-(aq)+H2O(l) | 20.15 | 1.41×1020 |
| HAsO42-(aq)+2e+2H+=HAsO32-(aq)+H2O(l) | 8.54 | 3.47×108 |
| AsO43-(aq)+2e+3H+=HAsO32-(aq)+H2O(l) | 20.65 | 4.47×1020 |
| AsO43-(aq)+2e+2H+=AsO33-(aq)+H2O(l) | 6.63 | 4.27×106 |
| H3AsO3(aq)+3e+3H+=As(s)+3H2O(l) | 13.19 | 1.55×1013 |
| H3AsO3(aq)+3e+3H+=As(s)+3H2O(l) | 22.78 | 6.03×1022 |
| HAsO32-(aq)+3e+5H+=As(s)+3H2O(l) | 34.39 | 2.45×1034 |
| AsO33-(aq)+3e+6H+=As(s)+3H2O(l) | 48.39 | 2.45×1048 |
2 纳米零价铁除砷初步研究
零价铁在湿法冶金领域中应用广泛,可有效还原工业废水中金属活动性低的金属阳离子。将零价铁纳米化后电位更低,反应活性更强〔11〕。考察了普通微米零价铁(mZVI)与纳米零价铁直接处理原始铜冶炼废酸的除砷效果,对比了粒径对零价铁除砷的影响,探究各实验条件对除砷效果的影响,并分析nZVI直接去除铜冶炼废酸中砷的机理。
2.1 实验方案及表征方法
实验所用含砷废酸来自国内某厂铜冶炼制酸车间集水池,废酸含砷11.235 g/L,为As(Ⅲ),H+为1.545 mol/L;采用氢还原法〔12〕制备稳定的nZVI。其他试剂及mZVI均为分析纯,购自国药集团。
将一定量铁粉倒入三口烧瓶中,加入适量含砷废酸,密封,水浴锅恒温加热,机械搅拌2 h后用0.45 μm滤纸过滤,滤渣于105 ℃真空干燥4 h,冷却至常温后收集。
用溴酸钾化学滴定法测定溶液中的As(Ⅲ)、As(Ⅴ);用LE438 pH计(梅特勒-托利多)测定溶液pH;用扫描电镜(SEM-EDS)对反应前后固体的形貌进行表征;用X射线荧光光谱(XRF)测定固体粉末中元素的种类及含量;用X射线衍射光谱(XRD)对反应前后固体的晶相结构进行分析;用傅里叶红外光谱(FTIR)分析固体中的化学键;用X射线光电子能谱(XPS)测定固体表面的化学组成及元素化学态。
2.2 结果与讨论
2.2.1 反应时间对零价铁除砷效果的影响
在反应温度为70 ℃、n(Fe)∶n(As)为5∶1的条件下,分别将mZVI与nZVI加至废酸中,每隔一段时间取样测定As。As去除效果随反应时间的变化如表 3所示。
表3 As去除率随反应时间的变化
| 时间/min | 5 | 15 | 30 | 60 | 90 | 120 | 150 | 180 | 210 | 240 |
| mZVI对As去除率/% | 15.85 | 18.24 | 19.46 | 28.42 | 32.01 | 33.70 | 33.81 | 33.04 | — | — |
| nZVI对As去除率/% | 54.86 | 58.49 | 58.88 | 59.55 | 60.69 | 60.50 | 63.85 | 65.57 | 64.81 | 66.43 |
由表 3可知,nZVI的除砷效果明显优于mZVI。反应15 min后nZVI对砷的去除率达到60%左右,反应趋于稳定,150 min后砷去除率有所上升,并稳定在65%左右,残余砷降至4 g/L左右;mZVI对砷的去除效果在90 min后趋于稳定,废酸中的残余砷降至7.5 g/L左右。后续实验中,nZVI与废酸反应150 min,mZVI与废酸反应90 min后进行固液分离。
2.2.2 铁砷比对零价铁除砷效果的影响
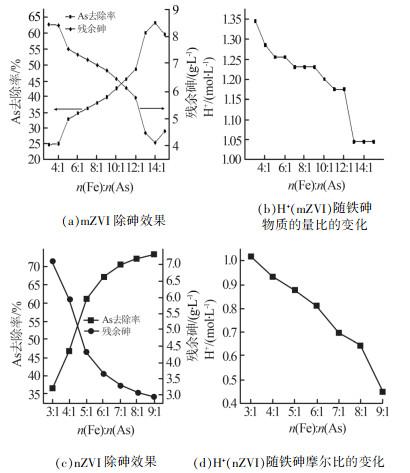
调节铁砷的物质的量比,其他实验条件保持不变,mZVI、nZVI除砷效果及H+的变化情况如图 3所示。
图3
2.2.3 反应温度对零价铁除砷效果的影响
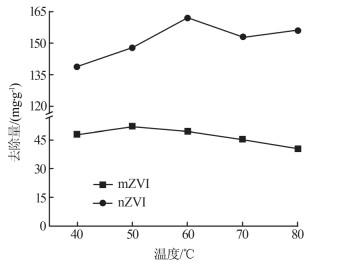
n(Fe)∶n(As)为13∶1时,零价铁除砷效果随温度的变化情况如图 4所示。
由图 4可知,mZVI对砷的去除能力随温度的升高先增加后降低,但总体影响不大,50 ℃时1 g Fe可去除52 mg As;nZVI对砷的去除能力随温度的升高先增加后有所降低,60 ℃时去除能力最高,1 g Fe可去除162 mg As。工业上含砷废酸温度一般在40~60 ℃,温度过高不适于实际应用,后续实验温度设置为50 ℃。
图4
2.2.4 机理分析
对最优条件下反应前后的零价铁进行SEM扫描,如图 5所示。
图5
由图 5(a)、(b)可见,mZVI与废酸反应后表面产生球状小颗粒,该球状颗粒粒径<100 nm,附着在光滑的铁颗粒表面,伴有团聚现象,同时存在片状物质,说明mZVI与废酸反应后发生腐蚀,表面氧化薄层脱落,露出的Fe(0)与废酸反应生成活性极高的结构态亚铁,进而去除废酸中的亚砷酸分子;由于mZVI颗粒大、比表面积小,沉积的含砷物质、铁氧化物及[H+]降低会抑制mZVI继续腐蚀,总的除砷效果不理想。由图 5(c)、(d)可见,nZVI颗粒呈不规则粗树枝状,粒径在200 nm以下,与废酸反应后呈球状,粒径<100 nm,并生成50 nm以下颗粒。nZVI的粒径小、比表面积大,废酸腐蚀后nZVI粒径有所减小,新生成的小颗粒可能为吸附的含砷物质。
对最优条件下反应的滤渣进行XRF分析,如表 4所示。
表4 零价铁除砷滤渣成分
| mZVI滤渣 | Fe | As | Mg | S | Bi | 失重率 |
| 质量分数/% | 58.79 | 8.81 | 1.43 | 0.292 | 0.343 | 3.563 |
| nZVI滤渣 | Fe | As | S | Si | Bi | 失重率 |
| 质量分数/% | 53.03 | 16.97 | 0.616 | 0.154 | 0.256 | 30.471 |
由表 4可知,mZVI与废酸反应后的滤渣中存在58.79%的Fe、8.81%的As,失重率达3.563%,说明mZVI反应活性低,在强还原条件下大部分铁没有被废酸消耗,只有少部分铁起到除砷作用;nZVI与废酸反应后的滤渣中存在53.03%Fe、16.97%As,失重率达到30.471%,说明nZVI反应活性高,在除砷的同时,有很大一部分铁与废酸中的H+发生反应而被消耗。
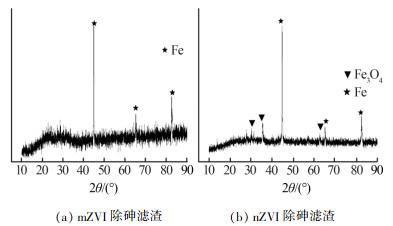
对最优条件下零价铁除砷滤渣进行XRD分析,如图 6所示。
图6
由图 6可知,mZVI和nZVI与废酸反应后的滤渣中均出现3个主要峰,分别位于44.67°、65.02°、82.34°,峰尖锐而明显,表明其结晶良好,图中未观察到As物相。mZVI反应后的滤渣出现峰宽较大的峰,判断为铁氧化物与砷氧化物结合形成的非晶态物质。nZVI反应后的滤渣在35.72°处出现的小峰为Fe3O4,进一步说明nZVI的反应活性更高。
对最优条件下nZVI与废酸反应前后的滤渣进行红外光谱分析。红外谱图中出现6个明显的特征峰〔13〕,3 428、1 630 cm-1为H2O的伸缩和弯曲振动峰,1 021 cm-1为Fe—OH的摇摆振动峰,两者均由空气中的水蒸气或废酸中的水分子形成;475、681 cm-1为nZVI氧化形成的Fe—O伸缩振动峰;802 cm-1为nZVI与废酸反应后吸附沉积的As—O伸缩振动峰。分析认为废酸的酸性大,As(Ⅲ)以H3AsO3绝对优势存在,H3AsO3脱氢与—OH进行离子交换,使As(Ⅲ)络合于铁氧化物表面,同时交换下来的—OH与H+发生反应。
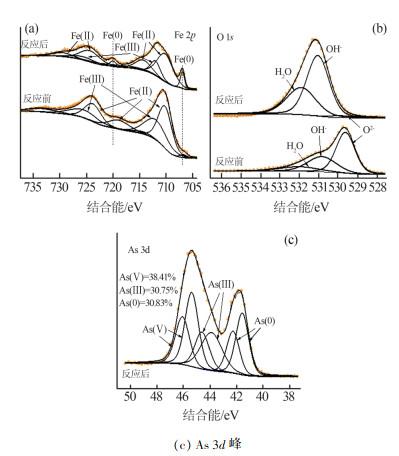
对最优条件下nZVI与废酸反应前后的滤渣进行XPS分析,如图 7所示。
图7
由图 7(a)可知,Fe(0)、Fe(Ⅱ)和Fe(Ⅲ)的Fe 2p3/2峰分别位于结合能707.1、710.2、712.0 eV处,Fe(0)、Fe(Ⅱ)和Fe(Ⅲ)的Fe 2p1/2峰分别位于结合能719.7、723.8、725.6 eV处,Fe(Ⅱ)和Fe(Ⅲ)的卫星峰分别位于714.6、729.5 eV,718.9、733.4 eV处。图 7(b)中O 1s则存在3处特征峰,位于结合能529.9、531.0、532.0 eV处,分别对应样品中的O2-、OH-以及物理吸附或化学结合的H2O〔14〕。表明nZVI与废酸反应前表面存在少量Fe(0),由于空气氧化作用,表面形成大部分Fe(Ⅱ)和Fe(Ⅲ),导致Fe的峰较小。同时,其表面存在占比较大的O2-、OH-和少量H2O。nZVI与废酸反应后表面Fe(0)和OH-比例升高,是由于废酸可使nZVI不断腐蚀、溶解,暴露于废酸溶液中,并产生大量铁氢氧化物。
由图 7(c)可知,As 3d存在3组特征峰,As(0)、As(Ⅲ)和As(Ⅴ)的As 3d5/2峰分别位于结合能41.6、44.03、45.03 eV处,As(Ⅲ)和As(Ⅴ)的As 3d3/2峰分别位于结合能42.3、44.6、45.68 eV处〔15-16〕,说明nZVI与废酸反应后表面存在3种砷的价态,而废酸中仅存在As(Ⅲ),并以H3AsO3形式存在。As(Ⅲ)不仅被还原至As(0),还被氧化至As(Ⅴ)。实验溶液为强酸性体系,nZVI不断被腐蚀暴露出新鲜的、强反应活性的零价铁核,部分As(Ⅲ)被还原为As(0);nZVI具有高反应活性,与空气中的氧气发生反应,见式(1)~式(4)。
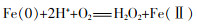
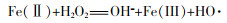
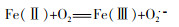
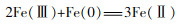
HO·和O2· ̄均有较强的氧化性,结合空气中的O2,滤渣表面部分As(Ⅲ)被氧化为As(Ⅴ)。
3 结论
(1)溶液体系中的砷在不同pH下以不同形式存在。酸性条件下主要以H3AsO3、H3AsO4、H2AsO4-和HAsO42-形式存在,强酸性条件下只存在H3AsO3和H3AsO4;碱性条件下主要存在H2AsO3-、HAsO32-、AsO33-、H2AsO4-、HAsO42-、AsO43-,强碱性条件下只存在AsO33-和AsO43-。
(2)As-H2O体系中的φ-pH图表明单质砷稳定存在的区域较大,酸性条件下更容易还原出单质砷,标准吉布斯自由能与标准平衡常数的计算结果表明亚砷酸与砷酸各类离子在标准状态下能够被还原为单质砷。
(3)nZVI直接处理铜冶炼废酸时可将其中的As(Ⅲ)还原为As(0),除砷机理包括络合吸附As(Ⅲ)、还原As(Ⅲ)至As(0)、氧化As(Ⅲ)至As(Ⅴ)并将其吸附。
(4)强酸性体系可提供砷还原的优异条件,但废酸中较高的H+会消耗加入的nZVI,导致除砷效果不理想。因此需考虑降低含砷废酸的酸度,使nZVI更好地与废酸中的砷发生反应。
参考文献
Arsenic speciation in environmental waters by a new specific phosphine modified polymer microsphere preconcentration and HPLC-ICP-MS determination
[J].DOI:10.1016/j.talanta.2016.07.050 [本文引用: 1]
Arsenic scenario in Gangetic delta of west Bengal: risk and management
[J].
Neutralization and co-precipitation of heavy metals by lime addition to effluent from acid plant in a copper smelter
[J].DOI:10.1016/j.mineng.2018.03.028 [本文引用: 1]
硫化氢净化强酸性高砷废液
[J].DOI:10.7524/j.issn.0254-6108.2015.12.2015091502 [本文引用: 1]
Arsenic removal from alkaline leaching solution using Fe(Ⅲ) precipitation
[J].DOI:10.1080/09593330.2018.1429495 [本文引用: 1]
Arsenic removal from water by hybrid electro-regenerated anion exchange resin/electrodialysis process
[J].
Quaternized hydroxyethyl cellulose ethoxylate and membrane separation techniques for arsenic removal
[J].
Synthesis of mesoporous bismuth-impregnated aluminum oxide for arsenic removal: adsorption mechanism study and application to a lab-scale column
[J].
Sequestration of metal cations with zerovalent iron nanoparticles-a study with high resolution X-ray photoelectron spectroscopy(HR-XPS)
[J].DOI:10.1021/jp0702189 [本文引用: 1]
Nitrate reduction over nanoscale zero-valent iron prepared by hydrogen reduction of goethite
[J].
Effects of geochemical conditions, surface modification, and arsenic(As) loadings on As release from As-loaded nano zero-valent iron in simulated groundwater
[J].
Solution and surface chemistry of the Se(Ⅳ)-Fe(0) reactions: effect of initial solution pH
[J].DOI:10.1016/j.chemosphere.2016.11.150 [本文引用: 1]
Simultaneous oxidation and reduction of arsenic by zero-valent iron nanoparticles: understanding the significance of the core-shell structure
[J].DOI:10.1021/jp9051837 [本文引用: 1]
Multi-tiered distributions of arsenic in iron nanoparticles: observation of dual redox functionality enabled by a core-shell structure
[J].DOI:10.1039/c0cc02311f [本文引用: 1]






 津公网安备 12010602120337号
津公网安备 12010602120337号