NiSiO@NiAlFe对不同抗生素的吸附特性研究
胡玉瑛 1 , 潘成 1 , 郑晓环 1 , 刘苏苏 1 , 彭小明 , 1 , 胡锋平 1 , 许莉 2 , 3 , 许高平 2 , 3
Study on the adsorption properties of NiSiO@NiAlFe to different antibiotics
Hu Yuying 1 , Pan Cheng 1 , Zheng Xiaohuan 1 , Liu Susu 1 , Peng Xiaoming , 1 , Hu Fengping 1 , Xu Li 2 , 3 , Xu Gaoping 2 , 3
通讯作者: 彭小明, 副教授。E-mail: pengxiaoming70@126.com
收稿日期: 2021-03-9
基金资助:
国家自然科学青年基金 . 51908214 国家自然科学青年基金 . 51908213 江西省科技厅重点研发计划项目 . 20192BBH80009 江西省重点实验室项目 . 20192BCD40013
Abstract
Layered double hydroxides(LDHs) coated NiAlFe-nickel silicate hollow spheres(NiSiO@NiAlFe) were prepared by hydrothermal method for the removal of different types of antibiotics in water. Results indicated that NiSiO@NiAlFe had a good adsorption efficiency on tetracycline(TC) and ciprofloxacin(CIP) in the pH range of 4-8. The adsorption process of TC and CIP was more consistent with the Freundlich model. At 15℃, the maximum adsorption capacities of NiSiO@NiAlFe for TC and CIP were 35.7 and 35.3 mg/g, respectively. Adsorption thermodynamics showed that the adsorption process was spontaneous and endothermic. The adsorption mechanisms of NiSiO@NiAlFe on TC and CIP were electrostatic attraction and complexation. The results showed that this material had great potential to remove antibiotics from water.
Keywords:
nickel silicate antibiotics tetracycline ciprofloxacin adsorption
本文引用格式
胡玉瑛, 潘成, 郑晓环, 刘苏苏, 彭小明, 胡锋平, 许莉, 许高平. NiSiO@NiAlFe对不同抗生素的吸附特性研究 . 工业水处理 [J], 2021, 41(4): 56-61 doi:10.11894/iwt.2020-0687
Hu Yuying. Study on the adsorption properties of NiSiO@NiAlFe to different antibiotics . Industrial Water Treatment
抗生素在人类和动物体内难以被完全代谢和吸收,50%~80%以原药物或不完全代谢的产物被排出体外〔1 〕 并进入环境,导致生态风险和人类健康问题〔2 〕 。高级氧化、吸附、萃取和生物降解等技术可用于水中抗生素的去除〔3 〕 ,但这些方法大多存在pH适用范围窄、对高盐浓度耐受能力有限等局限性。吸附法因成本低、操作方便、通用性强等优点,成为去除抗生素类污染物最有效的方法之一〔4 〕 。
硅酸盐在自然环境中十分丰富,其中具有典型层状结构的硅酸镍可作为吸附功能性材料而备受关注〔5 〕 。层状双氢氧化物(LDHs)是一种新型无机吸附材料,表面积大、阴离子交换性能好〔6 〕 ,但易聚集,导致吸附性能差〔7 〕 。合理构建硅酸镍与LDHs的复合材料,提高吸附剂表面官能团数目,有望提高材料的吸附性能。
笔者课题组前期研发并制备了NiAlFe LDHs包裹的硅酸镍空心球NiSiO@NiAlFe纳米材料〔8 〕 ,并用于放射性元素铯的吸附。该材料具有制备成本低、避免LDHs聚集、吸附速率较快等优点。基于此,笔者采用NiSiO@NiAlFe作为吸附剂,选取四环素(TC)和环丙沙星(CIP)作为常见四环素类和沙星类抗生素的典型代表,考察吸附剂投加量、pH、离子强度等对TC和CIP吸附性能的影响,并开展NiSiO@NiAlFe对TC和CIP的吸附等温线和吸附热力学研究,揭示其吸附机理。
1 实验部分
1.1 实验材料
试剂:四环素、环丙沙星,上海麦克林生化科技有限公司;正硅酸乙酯、六水硝酸镍、九水硝酸铝、九水硝酸铁,国药集团化学试剂有限公司;氨水、尿素、无水乙醇,西陇化工股份有限公司。以上试剂均为分析纯。
仪器:HH-S2恒温水浴锅,郑州予华仪器制造有限公司;HJ-6磁力搅拌器,金坛市江南仪器厂;DHG-9203A鼓风干燥箱,上海一恒科学仪器有限公司;pHS-25 pH计,上海仪电科学仪器股份有限公司;ME204E电子天平,METTLER TOLEDO;UV-1801紫外可见分光光度计,北京瑞利分析仪器公司;S-4800扫描电子显微镜,日本日立;JEOL JEM 2100透射电子显微镜,日本电子株式会社。
1.2 吸附剂制备
1.2.1 模板SiO2 制备
采用Stober方法制备SiO2 〔9 〕 。在100 mL无水乙醇中依次加入9 mL正硅酸乙酯、4 mL去离子水、100 mL氨水,随后在室温下搅拌5 h。混合液离心5 min,得到的固体用超纯水洗涤3次、60 ℃下干燥12 h,研磨后过0.075 mm筛(200目),得到白色二氧化硅粉体(球状)。
1.2.2 NiSiO空心球制备
将0.4 g SiO2 分散于80 mL水中并超声10 min,形成悬浮液A。取5.4 mmol Ni(NO3 )2 ·6H2 O、20 mmol NH4 Cl溶于80 mL蒸馏水中,搅拌约15 min,然后缓慢加入4 mL NH3 ·H2 O形成溶液B。将溶液B滴加到悬浮液A中,形成混合溶液。剧烈搅拌混合液10 min后,送入100 mL高压釜中,120 ℃下保持24 h。沉淀物分别用乙醇和超纯水冲洗3次,于60 ℃下干燥12 h。
1.2.3 NiSiO@NiAlFe LDHs制备
采用水热法制备NiSiO@NiAlFe LDHs。分别将1 g NiSiO空心球、2 mmol Mg(NO3 )2 ·6H2 O、2 mmol Al(NO3 )3 ·9H2 O、2 mmol Fe(NO3 )3 ·9H2 O、40 mmol尿素分散于60 mL水中。随后将混合悬液移至高压釜中,在120 ℃下反应12 h。沉积物分别用乙醇和超纯水冲洗3次,随后在60 ℃下干燥约12 h。
1.3 吸附实验
将一定量的NiSiO@NiAlFe、50 mL 20 mg/L的TC(CIP)溶液移入100 mL锥形瓶内,用0.1 mol/L硝酸和氢氧化钠溶液调节pH;将锥形瓶置于气浴恒温振荡器中,振动速率180 r/min,保持24 h;离心分离,用紫外-可见分光光度计在356(277)nm处对TC(CIP)溶液进行测定。所有实验均重复3次。
2 结果与讨论
2.1 NiSiO和NiSiO@NiAlFe形貌
用扫描电镜(SEM)及透射电镜(TEM)对材料表面形貌进行表征,如图 1 所示〔8 〕 。
图1
图1
NiSiO(a)与NiSiO@NiAlFe(b)的SEM照片(插图为TEM)
图 1 中,NiSiO为空心球结构,球体直径约400 nm,具有较好的分散性,其表面被垂直排列的片状团簇覆盖。由TEM可以看出NiSiO表面的片状结构高度约为40 nm。NiSiO空心球表面负载LDHs后,其空心球形态保持良好。NiSiO@NiAlFe被泡沫状团簇包裹,由TEM可见其表面团簇厚度增加,表明LDHs成功负载到NiSiO空心球上。
2.2 初始pH的影响
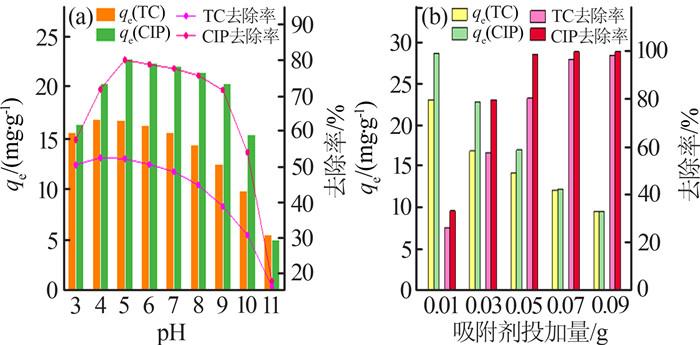
在吸附剂投加量为0.05 g(50 mL)、温度为25 ℃的条件下,考察pH对吸附剂吸附TC和CIP性能的影响,如图 2(a) 所示。
图2
图2
pH(a)和NiSiO@NiAlFe投加量(b)对吸附容量的影响
图 2(a) 中,随着溶液初始pH的增加,吸附剂对TC和CIP的吸附容量均出现先增大后减小的趋势,即pH<4的酸性条件及pH>10的碱性条件下NiSiO@ NiAlFe对TC和CIP的吸附容量较低,pH为4~10条件下吸附容量较高。碱性条件下吸附容量较低的原因可能为TC和CIP在碱性环境下表面带负电荷〔10 〕 ,会与LDHs表面的负电荷形成静电斥力,从而导致吸附量降低。当pH<4时,吸附体系中H+ 浓度较高,LDHs存在溶解效应,材料的吸附点位减少〔11 〕 ,吸附容量降低。由于TC、CIP分别在pH为4、5条件下吸附效果最好,后续研究均在此pH条件下进行。
2.3 吸附剂投加量的影响
吸附剂投加量对NiSiO@NiAlFe吸附TC和CIP效果的影响如图 2(b) 所示。当吸附剂投加量为0.07 g(溶液体积50 mL)时,NiSiO@NiAlFe对TC和CIP的去除率均接近100%。吸附剂投加量较低时(<0.05 g),NiSiO@NiAlFe对CIP的吸附容量和去除率均高于TC,表明低投加量条件下该材料对CIP的去除效果优于TC。此外,随着投加量的增加,NiSiO@ NiAlFe对TC和CIP的去除率均呈上升趋势,吸附容量逐渐下降。这可能是因为增加NiSiO@NiAlFe投加量可导致活性位点数量增加、总有效比表面积增大,因此去除率增大;而在恒定浓度溶液中,暴露的吸附位点随投加量的增加而增加,以至于未达到饱和的吸附位点随着投加量的增加而增多,使得吸附容量下降。考虑到NiSiO@NiAlFe投加量在0.03 g时对TC和CIP的吸附容量和去除率均较高,后续研究在此投加量下进行。
2.4 离子强度的影响
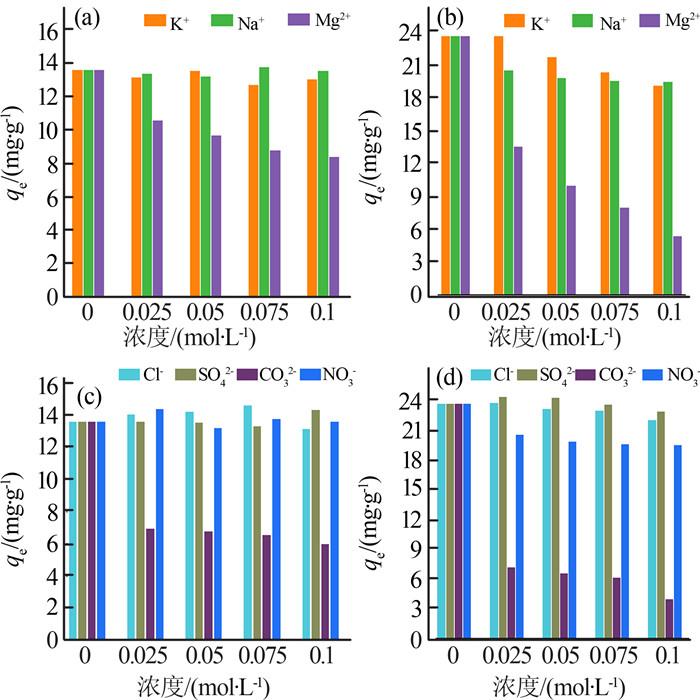
实际含抗生素的废水可能含有其他盐离子。研究了不同阳离子(K+ 、Na+ 、Mg2+ )和阴离子(Cl- 、SO4 2- 、CO3 2- 、NO3 - )存在下TC和CIP的吸附效果,如图 3 所示。
图3
图3
离子强度对吸附TC(a、c)、CIP(b、d)效果的影响
由图 3 可见,K+ 、Na+ 、Cl- 、SO4 2- 、NO3 - 对TC和CIP的吸附效果均无显著影响,而溶液中的Mg2+ 及CO3 2- 对二者的吸附效果均有抑制作用。图 3(a) 中,随着Mg2+ 的增加,NiSiO@NiAlFe对TC和CIP的吸附容量逐渐下降,可能是由于Mg2+ 占据了NiSiO@ NiAlFe表面的活性位点。当溶液中存在CO3 2- 时,NiSiO@NiAlFe吸附容量降低更为显著,可能是CO3 2- 水解导致溶液pH增加,而前述实验已证明pH升高会降低NiSiO@NiAlFe对TC和CIP的吸附效果。
2.5 吸附动力学
考察了不同接触时间及温度下NiSiO@NiAlFe对TC和CIP的吸附能力。实验结果表明,NiSiO@ NiAlFe对TC和CIP的吸附具有时间依赖性,随着接触时间的延长,NiSiO@NiAlFe对TC和CIP的吸附量逐渐增大。吸附过程在实验前期进行较快,吸附120 min时对TC、CIP的吸附量分别为10、14 mg/g左右;240 min后吸附过程逐渐变慢,960 min左右达到近似平衡状态。原因在于,吸附开始阶段TC和CIP分子与NiSiO@NiAlFe表面活性位点的接触时间有限,吸附能力较低;随着接触时间的增加,NiSiO@ NiAlFe表面的活性位点逐渐被占据并达到饱和,吸附速率逐渐降低。
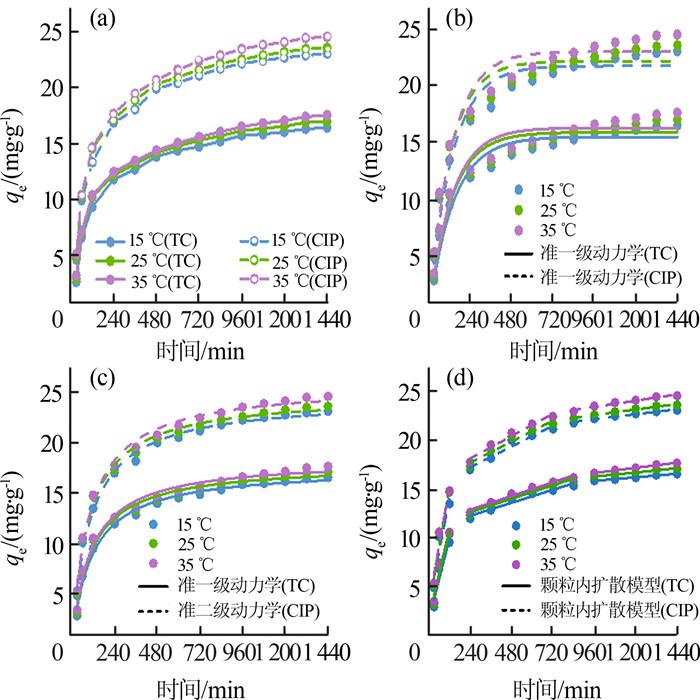
采用准一级、准二级动力学模型对NiSiO@ NiAlFe吸附TC、CIP过程进行拟合(pH分别为4、5,TC和CIP初始质量浓度为20 mg/L,吸附剂投加量0.03 g)。同时,为探讨TC和CIP在NiSiO@NiAlFe上吸附多过程控制的各阶段情况,用Weber-Morris颗粒内扩散模型进行拟合。拟合结果如图 4 、表 1 所示。
图4
图4
TC(CIP)吸附量随吸附时间的变化(a)、准一级拟合曲线(b)、准二级拟合曲线(c)、内扩散拟合曲线
由图 4 可知,NiSiO@NiAlFe对TC、CIP的吸附分为3个阶段,拟合直线未过原点,说明颗粒内扩散并不是该吸附过程唯一的速率控制步骤。吸附初期,TC和CIP分子在溶液驱动力下迅速附着在NiSiO@ NiAlFe外表面,随后在分子传质力作用下缓慢扩散到NiSiO@NiAlFe内部并逐渐占据内部活性位点,达到吸附平衡,最大吸附量分别为16.3、23.0 mg/g。由表 1 可见,NiSiO@NiAlFe吸附TC和CIP的准二级动力学模型拟合曲线的R 2 高于准一级动力学拟合曲线的R 2 ,说明化学吸附在整个吸附过程起主导作用。
2.6 吸附等温线
温度在15~45 ℃时,NiSiO@NiAlFe对TC和CIP的吸附量随初始质量浓度的增加而显著增加。CIP溶液初始质量浓度为120 mg/L时,其在NiSiO@NiAlFe的吸附逐渐饱和,45 ℃时最大吸附量为40.2 mg/g;TC初始质量浓度为80 mg/L时,吸附开始趋于平衡,45 ℃时最大吸附量为35.4 mg/g。原因可能在于溶液质量浓度较低时,NiSiO@NiAlFe表面大量活性位点没有达到饱和,此时NiSiO@NiAlFe对CIP和TC的吸附容量较大;随着二者初始质量浓度逐渐升高,固液界面的传质驱动力增强,吸附容量变大。初始质量浓度过高时,NiSiO@NiAlFe表面活性位点饱和,吸附量不再显著增加。
采用Langmuir、Freundlich和Temkin等温模型对NiSiO@NiAlFe吸附TC和CIP进行拟合。Langmuir等温线模型假设吸附过程在均质表面进行,不存在分子间的相互作用,所有吸附位点均相等〔12 〕 。Freundlich模型假定吸附过程为多相表面的多层吸附,并提出分子结合于表面位点会影响相邻位点的假设〔13 〕 。Temkin等温线模型是基于强静电作用的正负电荷间的化学吸附模型〔14 〕 。拟合结果如表 2 所示。
由表 2 可知,Freundlich模型对TC和CIP的拟合度均高于Langmuir模型,NiSiO@NiAlFe对TC和CIP的吸附过程更符合Freundlich模型,NiSiO@ NiAlFe对二者吸附是表面不均匀的多分子层吸附。1/n 均<0.5,表明NiSiO@NiAlFe对TC和CIP的吸附较易进行。此外,CIP的Temkin模型拟合曲线的R 2 高于TC,表明NiSiO@NiAlFe与CIP分子之间的静电作用比TC分子更强。
2.7 吸附热力学
温度对吸附过程中分子运动有促进作用,考察了温度为15、30、45 ℃时,NiSiO@NiAlFe对TC和CIP的吸附量。结果表明在15~45 ℃范围内,随着温度的升高,NiSiO@NiAlFe对TC和CIP的吸附量均增加,说明高温更有利于吸附过程进行。
通过范霍夫方程〔15 〕 对NiSiO@NiAlFe吸附TC和CIP过程进行热力学研究。范霍夫方程由式(1)~式(3)描述。
(1)
(2)
(3)
式中:R ——通用气体常数,8.314 J/(mol·K);
由表 3 可知,3个环境温度下的ΔG 均为负值,说明TC和CIP在NiSiO@NiAlFe处的吸附是自发进行的。ΔG 的绝对值随温度升高而增大,表明自发程度随温度的升高而加剧。ΔH 为正,表明该吸附过程为吸热反应,这与等温吸附过程中NiSiO@NiAlFe对TC和CIP的吸附量随温度升高而增大的结论一致。
2.8 NiSiO@NiAlFe对TC和CIP的吸附机理
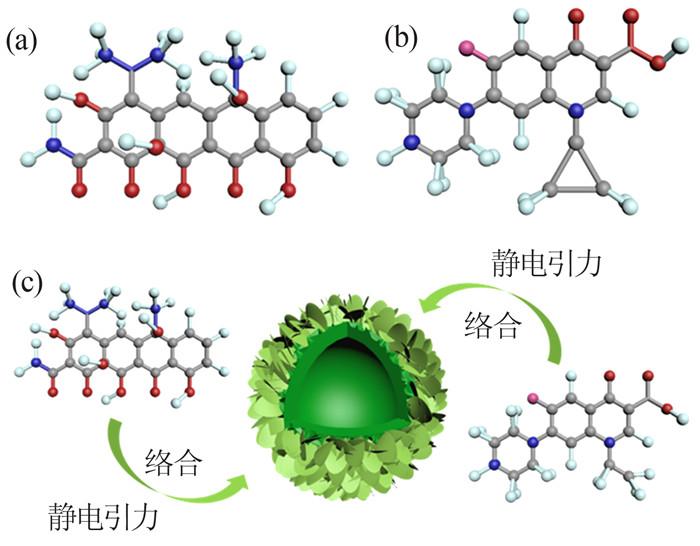
研究发现,NiSiO@NiAlFe吸附CIP的Temkin模型的R 2 较高,表明NiSiO@NiAlFe与CIP存在较强的静电吸附作用。这可能是由于CIP在酸性环境中以阳离子形式存在〔10 〕 ,而LDHs具有大量层间阴离子,可与CIP形成静电引力,使CIP快速聚集在吸附剂表面。此外,NiSiO@NiAlFe表面存在Ni2+ 、Al3+ 、Fe3+ 等金属离子,而TC与CIP分子均存在—COOH,金属离子可与—COOH形成—CO—M—CO—形式的络合物(M代表金属离子),将TC与CIP固定在NiSiO@ NiAlFe,完成吸附过程。综上认为,NiSiO@NiAlFe对TC和CIP的吸附主要依靠NiSiO@NiAlFe的静电引力和络合效应,如图 5 所示。
图5
图5
TC(a)、CIP(b)分子结构及吸附机理(c)
2.9 再生性能评价
为评价NiSiO@NiAlFe的可重复使用性,用0.5 mol/L的NaOH溶液进行脱附实验:将吸附平衡后的吸附剂按6 g/L的固液比分散于0.5 mol/L NaOH溶液中,震荡3 h后5 000 r/min离心5 min进行固液分离,用超纯水清洗3次,在60 ℃下干燥12 h,得到再生NiSiO@NiAlFe并用于下一次吸附实验。循环上述操作5次以测试其可再生能力,结果表明:连续5次循环实验后,NiSiO@NiAlFe对TC和CIP的吸附能力略有下降,但仍保持在良好范围内。再生5次后,NiSiO@NiAlFe对TC和CIP的吸附率分别为82.7%、83.1%,为再生前的90.2%、89.3%。
3 结论
(1)研究表明NiSiO@NiAlFe对CIP和TC均有较好的吸附性能,与其他吸附剂相比具有一定优势〔16 -17 〕 。NiSiO@NiAlFe对CIP的吸附效果优于TC,可能是由于NiSiO@NiAlFe与CIP的静电作用强于TC。
(2)NiSiO@NiAlFe吸附CIP和TC的最佳pH分别为5、4。水溶液中的Mg2+ 及CO3 2- 对吸附效果有抑制作用。
(3)吸附等温线表明NiSiO@NiAlFe对CIP和TC的吸附为多层吸附,吸附过程更符合Freundlich模型,15 ℃下最大吸附量分别为35.7、35.3 mg/g。吸附热力学表明随着温度的升高,NiSiO@NiAlFe对CIP和TC的吸附量均增大,且吸附过程自发进行,为吸热过程。
(4)NiSiO@NiAlFe表面的金属离子可与—COOH形成—CO—M—CO—形式的络合物,将TC与CIP固定在NiSiO@NiAlFe上完成吸附过程。
参考文献
View Option
[1]
Halling-Sorensen B , Sengelov G , Tjornelund J . Toxicity of tetracyc lines and tetracycline degradation products to environmentally rele vant bacteria, including selected tetracycline-resistant bacteria
[J]. Archives of Environmental Contamination and Toxicology , 2002 , 42 , 263 - 271 .
DOI:10.1007/s00244-001-0017-2
[本文引用: 1]
[2]
安博宇 , 袁园园 , 黄玲利 , 等 . 头孢菌素类药物在环境中的行为及残留研究进展
[J]. 中国抗生素杂志 , 2020 , (6 ): 551 - 559 .
URL
[本文引用: 1]
[3]
Wang Qiang , Li Xunan , Yang Qingxiang , et al . Evolution of microbial community and drug resistance during enrichment of tetracycline-de grading bacteria
[J]. Ecotoxicology and Environmental Safety , 2019 , 171 , 746 - 752 .
DOI:10.1016/j.ecoenv.2019.01.047
[本文引用: 1]
[5]
Liu Jiangyong , Chen Tingting , Jian Panming , et al . Hierarchical ho llow nickel silicate microflowers for selective oxidation of styrene
[J]. Journal of Colloid and Interface Science , 2019 , 553 , 606 - 612 .
DOI:10.1016/j.jcis.2019.06.042
[本文引用: 1]
[6]
谢丹丹 , 曲晓飞 , 杜芳林 . 形貌和尺寸可控的二氧化硅/硅酸镍锰空心微球的制备
[J]. 材料导报 , 2014 , 28 (10 ): 86 - 88 .
URL
[本文引用: 1]
[7]
Zhang Xiangling , Xue Yu , Gao Jingtian , et al . Comparison of adsorp tion mechanisms for cadmium removal by modified zeolites and sands coated with Zn-layered double hydroxides
[J]. Chemical Engineer ing Journal , 2020 , 380 , 122578 .
DOI:10.1016/j.cej.2019.122578
[本文引用: 1]
[8]
Hu Yuying , Pan Cheng , Zheng Xiaohuan , et al . Prediction and opti mization of adsorption properties for Cs+ on NiSiO@NiAlFe LDHs hollow spheres from aqueous solution: kinetics, isotherms, and BBD model
[J]. Journal of Hazardous Materials , 2021 , 401 , 123374 .
DOI:10.1016/j.jhazmat.2020.123374
[本文引用: 2]
[9]
Stober W , Fink A , Bohn E . Controlled growth of monodisperse silica spheres in the micron size range
[J]. Journal of Colloid and Inter face Science , 1968 , 26 (1 ): 62 - 69 .
DOI:10.1016/0021-9797(68)90272-5
[本文引用: 1]
[10]
El-Shafey E S I , Al-Lawati H , Al-Sumri A S . Ciprofloxacin adsorp tion from aqueous solution onto chemically prepared carbon from date palm leaflets
[J]. Journal of Environmental Sciences , 2012 , 24 (9 ): 1579 - 1586 .
DOI:10.1016/S1001-0742(11)60949-2
[本文引用: 2]
[11]
Hu Yuying , Pan Cheng , Zheng Xiaohuan , et al . Removal of ciproflo xacin with aluminum-pillared kaolin sodium alginate beads(CA Al-KABs): kinetics, isotherms, and BBD model
[J]. Water , 2020 , 12 (3 ): 905 .
DOI:10.3390/w12030905
[本文引用: 1]
[12]
Wang Min , Peng Jing , Zhai Maolin , et al . Adsorption and desorption of Sr(Ⅱ) ions in the gels based on polysaccharide derivates
[J]. Jo urnal of Hazardous Materials , 2009 , 171 (1/2/3 ): 820 - 826 .
URL
[本文引用: 1]
[13]
Mohan D , Sarswat A , Ok Y S , et al . Organic and inorganic contami nants removal from water with biochar, a renewable, low cost and sustainable adsorbent-a critical review
[J]. Bioresource Technolo gy , 2014 , 160 , 191 - 202 .
DOI:10.1016/j.biortech.2014.01.120
[本文引用: 1]
[14]
Lian Lili , Guo Liping , Guo Chunjing . Adsorption of Congo red from aqueous solutions onto Ca-bentonite
[J]. Journal of Hazardous Ma terials , 2009 , 161 (1 ): 126 - 131 .
DOI:10.1016/j.jhazmat.2008.03.063
[本文引用: 1]
[15]
Yousef R I , El-Eswed B , Al-Muhtaseb A H . Adsorption characteri stics of natural zeolites as solid adsorbents for phenol removal from aqueous solutions: kinetics, mechanism, and thermodynamics stud ies
[J]. Chemical Engineering Journal , 2011 , 171 (3 ): 1143 - 1149 .
DOI:10.1016/j.cej.2011.05.012
[本文引用: 1]
[16]
范世锁 , 刘文浦 , 王锦涛 , 等 . 茶渣生物炭制备及其对溶液中四环素的去除特性
[J]. 环境科学 , 2020 , 41 (3 ): 1308 - 1318 .
URL
[本文引用: 1]
[17]
薛向东 , 王星源 , 梅雨晨 , 等 . 微塑料对水中铜离子和四环素的吸附行为
[J]. 环境科学 , 2020 , 41 (8 ): 3675 - 3683 .
URL
[本文引用: 1]
Toxicity of tetracyc lines and tetracycline degradation products to environmentally rele vant bacteria, including selected tetracycline-resistant bacteria
1
2002
... 抗生素在人类和动物体内难以被完全代谢和吸收,50%~80%以原药物或不完全代谢的产物被排出体外〔1 〕 并进入环境,导致生态风险和人类健康问题〔2 〕 .高级氧化、吸附、萃取和生物降解等技术可用于水中抗生素的去除〔3 〕 ,但这些方法大多存在pH适用范围窄、对高盐浓度耐受能力有限等局限性.吸附法因成本低、操作方便、通用性强等优点,成为去除抗生素类污染物最有效的方法之一〔4 〕 . ...
头孢菌素类药物在环境中的行为及残留研究进展
1
2020
... 抗生素在人类和动物体内难以被完全代谢和吸收,50%~80%以原药物或不完全代谢的产物被排出体外〔1 〕 并进入环境,导致生态风险和人类健康问题〔2 〕 .高级氧化、吸附、萃取和生物降解等技术可用于水中抗生素的去除〔3 〕 ,但这些方法大多存在pH适用范围窄、对高盐浓度耐受能力有限等局限性.吸附法因成本低、操作方便、通用性强等优点,成为去除抗生素类污染物最有效的方法之一〔4 〕 . ...
Evolution of microbial community and drug resistance during enrichment of tetracycline-de grading bacteria
1
2019
... 抗生素在人类和动物体内难以被完全代谢和吸收,50%~80%以原药物或不完全代谢的产物被排出体外〔1 〕 并进入环境,导致生态风险和人类健康问题〔2 〕 .高级氧化、吸附、萃取和生物降解等技术可用于水中抗生素的去除〔3 〕 ,但这些方法大多存在pH适用范围窄、对高盐浓度耐受能力有限等局限性.吸附法因成本低、操作方便、通用性强等优点,成为去除抗生素类污染物最有效的方法之一〔4 〕 . ...
原料和制炭方式对生物炭吸附抗生素的影响
1
2020
... 抗生素在人类和动物体内难以被完全代谢和吸收,50%~80%以原药物或不完全代谢的产物被排出体外〔1 〕 并进入环境,导致生态风险和人类健康问题〔2 〕 .高级氧化、吸附、萃取和生物降解等技术可用于水中抗生素的去除〔3 〕 ,但这些方法大多存在pH适用范围窄、对高盐浓度耐受能力有限等局限性.吸附法因成本低、操作方便、通用性强等优点,成为去除抗生素类污染物最有效的方法之一〔4 〕 . ...
Hierarchical ho llow nickel silicate microflowers for selective oxidation of styrene
1
2019
... 硅酸盐在自然环境中十分丰富,其中具有典型层状结构的硅酸镍可作为吸附功能性材料而备受关注〔5 〕 .层状双氢氧化物(LDHs)是一种新型无机吸附材料,表面积大、阴离子交换性能好〔6 〕 ,但易聚集,导致吸附性能差〔7 〕 .合理构建硅酸镍与LDHs的复合材料,提高吸附剂表面官能团数目,有望提高材料的吸附性能. ...
形貌和尺寸可控的二氧化硅/硅酸镍锰空心微球的制备
1
2014
... 硅酸盐在自然环境中十分丰富,其中具有典型层状结构的硅酸镍可作为吸附功能性材料而备受关注〔5 〕 .层状双氢氧化物(LDHs)是一种新型无机吸附材料,表面积大、阴离子交换性能好〔6 〕 ,但易聚集,导致吸附性能差〔7 〕 .合理构建硅酸镍与LDHs的复合材料,提高吸附剂表面官能团数目,有望提高材料的吸附性能. ...
Comparison of adsorp tion mechanisms for cadmium removal by modified zeolites and sands coated with Zn-layered double hydroxides
1
2020
... 硅酸盐在自然环境中十分丰富,其中具有典型层状结构的硅酸镍可作为吸附功能性材料而备受关注〔5 〕 .层状双氢氧化物(LDHs)是一种新型无机吸附材料,表面积大、阴离子交换性能好〔6 〕 ,但易聚集,导致吸附性能差〔7 〕 .合理构建硅酸镍与LDHs的复合材料,提高吸附剂表面官能团数目,有望提高材料的吸附性能. ...
Prediction and opti mization of adsorption properties for Cs+ on NiSiO@NiAlFe LDHs hollow spheres from aqueous solution: kinetics, isotherms, and BBD model
2
2021
... 笔者课题组前期研发并制备了NiAlFe LDHs包裹的硅酸镍空心球NiSiO@NiAlFe纳米材料〔8 〕 ,并用于放射性元素铯的吸附.该材料具有制备成本低、避免LDHs聚集、吸附速率较快等优点.基于此,笔者采用NiSiO@NiAlFe作为吸附剂,选取四环素(TC)和环丙沙星(CIP)作为常见四环素类和沙星类抗生素的典型代表,考察吸附剂投加量、pH、离子强度等对TC和CIP吸附性能的影响,并开展NiSiO@NiAlFe对TC和CIP的吸附等温线和吸附热力学研究,揭示其吸附机理. ...
... 用扫描电镜(SEM)及透射电镜(TEM)对材料表面形貌进行表征,如图 1 所示〔8 〕 . ...
Controlled growth of monodisperse silica spheres in the micron size range
1
1968
... 采用Stober方法制备SiO2 〔9 〕 .在100 mL无水乙醇中依次加入9 mL正硅酸乙酯、4 mL去离子水、100 mL氨水,随后在室温下搅拌5 h.混合液离心5 min,得到的固体用超纯水洗涤3次、60 ℃下干燥12 h,研磨后过0.075 mm筛(200目),得到白色二氧化硅粉体(球状). ...
Ciprofloxacin adsorp tion from aqueous solution onto chemically prepared carbon from date palm leaflets
2
2012
... 图 2(a) 中,随着溶液初始pH的增加,吸附剂对TC和CIP的吸附容量均出现先增大后减小的趋势,即pH<4的酸性条件及pH>10的碱性条件下NiSiO@ NiAlFe对TC和CIP的吸附容量较低,pH为4~10条件下吸附容量较高.碱性条件下吸附容量较低的原因可能为TC和CIP在碱性环境下表面带负电荷〔10 〕 ,会与LDHs表面的负电荷形成静电斥力,从而导致吸附量降低.当pH<4时,吸附体系中H+ 浓度较高,LDHs存在溶解效应,材料的吸附点位减少〔11 〕 ,吸附容量降低.由于TC、CIP分别在pH为4、5条件下吸附效果最好,后续研究均在此pH条件下进行. ...
... 研究发现,NiSiO@NiAlFe吸附CIP的Temkin模型的R 2 较高,表明NiSiO@NiAlFe与CIP存在较强的静电吸附作用.这可能是由于CIP在酸性环境中以阳离子形式存在〔10 〕 ,而LDHs具有大量层间阴离子,可与CIP形成静电引力,使CIP快速聚集在吸附剂表面.此外,NiSiO@NiAlFe表面存在Ni2+ 、Al3+ 、Fe3+ 等金属离子,而TC与CIP分子均存在—COOH,金属离子可与—COOH形成—CO—M—CO—形式的络合物(M代表金属离子),将TC与CIP固定在NiSiO@ NiAlFe,完成吸附过程.综上认为,NiSiO@NiAlFe对TC和CIP的吸附主要依靠NiSiO@NiAlFe的静电引力和络合效应,如图 5 所示. ...
Removal of ciproflo xacin with aluminum-pillared kaolin sodium alginate beads(CA Al-KABs): kinetics, isotherms, and BBD model
1
2020
... 图 2(a) 中,随着溶液初始pH的增加,吸附剂对TC和CIP的吸附容量均出现先增大后减小的趋势,即pH<4的酸性条件及pH>10的碱性条件下NiSiO@ NiAlFe对TC和CIP的吸附容量较低,pH为4~10条件下吸附容量较高.碱性条件下吸附容量较低的原因可能为TC和CIP在碱性环境下表面带负电荷〔10 〕 ,会与LDHs表面的负电荷形成静电斥力,从而导致吸附量降低.当pH<4时,吸附体系中H+ 浓度较高,LDHs存在溶解效应,材料的吸附点位减少〔11 〕 ,吸附容量降低.由于TC、CIP分别在pH为4、5条件下吸附效果最好,后续研究均在此pH条件下进行. ...
Adsorption and desorption of Sr(Ⅱ) ions in the gels based on polysaccharide derivates
1
2009
... 采用Langmuir、Freundlich和Temkin等温模型对NiSiO@NiAlFe吸附TC和CIP进行拟合.Langmuir等温线模型假设吸附过程在均质表面进行,不存在分子间的相互作用,所有吸附位点均相等〔12 〕 .Freundlich模型假定吸附过程为多相表面的多层吸附,并提出分子结合于表面位点会影响相邻位点的假设〔13 〕 .Temkin等温线模型是基于强静电作用的正负电荷间的化学吸附模型〔14 〕 .拟合结果如表 2 所示. ...
Organic and inorganic contami nants removal from water with biochar, a renewable, low cost and sustainable adsorbent-a critical review
1
2014
... 采用Langmuir、Freundlich和Temkin等温模型对NiSiO@NiAlFe吸附TC和CIP进行拟合.Langmuir等温线模型假设吸附过程在均质表面进行,不存在分子间的相互作用,所有吸附位点均相等〔12 〕 .Freundlich模型假定吸附过程为多相表面的多层吸附,并提出分子结合于表面位点会影响相邻位点的假设〔13 〕 .Temkin等温线模型是基于强静电作用的正负电荷间的化学吸附模型〔14 〕 .拟合结果如表 2 所示. ...
Adsorption of Congo red from aqueous solutions onto Ca-bentonite
1
2009
... 采用Langmuir、Freundlich和Temkin等温模型对NiSiO@NiAlFe吸附TC和CIP进行拟合.Langmuir等温线模型假设吸附过程在均质表面进行,不存在分子间的相互作用,所有吸附位点均相等〔12 〕 .Freundlich模型假定吸附过程为多相表面的多层吸附,并提出分子结合于表面位点会影响相邻位点的假设〔13 〕 .Temkin等温线模型是基于强静电作用的正负电荷间的化学吸附模型〔14 〕 .拟合结果如表 2 所示. ...
Adsorption characteri stics of natural zeolites as solid adsorbents for phenol removal from aqueous solutions: kinetics, mechanism, and thermodynamics stud ies
1
2011
... 通过范霍夫方程〔15 〕 对NiSiO@NiAlFe吸附TC和CIP过程进行热力学研究.范霍夫方程由式(1)~式(3)描述. ...
茶渣生物炭制备及其对溶液中四环素的去除特性
1
2020
... (1)研究表明NiSiO@NiAlFe对CIP和TC均有较好的吸附性能,与其他吸附剂相比具有一定优势〔16 -17 〕 .NiSiO@NiAlFe对CIP的吸附效果优于TC,可能是由于NiSiO@NiAlFe与CIP的静电作用强于TC. ...
微塑料对水中铜离子和四环素的吸附行为
1
2020
... (1)研究表明NiSiO@NiAlFe对CIP和TC均有较好的吸附性能,与其他吸附剂相比具有一定优势〔16 -17 〕 .NiSiO@NiAlFe对CIP的吸附效果优于TC,可能是由于NiSiO@NiAlFe与CIP的静电作用强于TC. ...
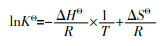
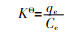
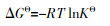






 津公网安备 12010602120337号
津公网安备 12010602120337号