阿特拉津(ATZ)是一种人工合成的除草剂,半衰期较长(41~231 d),进入环境中难以降解,对动植物和人类可产生不同程度的危害。我国《地表水环境质量标准》(GB 3838—2002)中规定,地表水中的ATZ最高为3.0 μg/L〔1〕。《生活饮用水卫生标准》(GB 5746—2006)明确规定,ATZ的质量浓度不得超过2 μg/L的限值。
目前,采用BDD阳极电活化硫酸盐降解去除ATZ的研究很少,且在特定条件下SO4·-对ATZ的降解贡献程度尚不清楚。因此,笔者研究了BDD电极的电催化性能,并与Pt电极进行对比;利用自制的循环阳极电极装置,比较电活化硫酸盐去除ATZ与直接电解去除ATZ的降解效果,对降解反应进行动力学规律拟合;采用自由基竞争捕获法,分析电活化硫酸盐过程中SO4·-氧化降解ATZ的贡献率。
1 材料与方法
1.1 实验试剂
高氯酸钠、碳酸氢钠、碳酸钠,天津市恒兴化学试剂制造有限公司。ATZ购自MACKLIN。PDS购自Aladdin。硫酸钠、碘化钾,天津大茂化学试剂有限公司。甲醇(MeOH)、叔丁醇(TBA),色谱纯,天津科密欧化学试剂有限公司。以上试剂均直接使用。溶液均用超纯水(20 ℃时电阻率为18.2 MΩ·cm)制备。
1.2 实验装置
电解化学实验装置由3部分组成:(1)定制的H型阴阳极分槽反应器,阳极、阴极室的有效容积均为100 mL,由阳离子交换膜隔开。阳极为BDD电极(25 mm×50 mm×1 mm),阴极为Pt电极(25 mm×50 mm×1 mm),两电极板竖直平行放置,浸没高度为40 mm,间距为27 mm,阴阳极均设有电解液输入与输出通道。(2)电解液循环装置,阳极室通过恒流泵与储液罐相连,电解质以30 mL/min的恒定流量循环电解。储液罐有效容积为250 mL,置于恒温磁力搅拌器上,保证电解质温度恒定为(25±2)℃、反应浓度均匀,阴极循环部分与阳极循环部分对称布置。(3)直流稳压电源通过电极夹具与电极板连接,实验过程中以恒电流供电。
1.3 实验方法
1.3.1 循环伏安曲线(CV)扫描
CV曲线测试体系为经典三电极体系,工作电极为BDD电极,对电极为Pt电极,参比电极为饱和甘汞电极(SCE)。实验在20 ℃室温下关闭循环装置进行,扫描开始前通入高纯氮气15 min去除溶解氧,Na2SO4电解质浓度为0.2 mol/L,扫描速率为100 mV/s。
1.3.2 自由基竞争捕获实验
实验选用ATZ作为自由基探针,甲醇和叔丁醇分别为自由基猝灭剂,在ATZ初始浓度为10 μmol/L、电流密度为30 mA/cm2、Na2SO4电解质浓度为0.1 mol/L的条件下,测定BDD阳极电解ATZ的降解程度。在ATZ直接电解的空白对照实验中,用NaClO4配制背景电解质溶液,NaClO4在阳极电解过程中具有很好的稳定性,不易被氧化〔5〕。实验至少重复2次。
1.3.3 电活化硫酸盐降解实验
在分槽循环阳极电解模式下,当电流密度为30 mA/cm2、Na2SO4电解质浓度为0.1 mol/L,对初始浓度为10 μmol/L的ATZ进行电解去除,同时检测该过程中PDS的生成情况。实验至少重复2次。
1.4 分析方法
ATZ浓度用高效液相色谱(HPLC)测定。将样品迅速加入事先盛有纯甲醇的样品瓶中(甲醇需过量)进行猝灭。由于样品液可能含有不溶性沉淀,为防止色谱柱堵塞,进样前需经0.22 μm有机滤膜过滤。检测器为紫外检测器,色谱柱为C18柱,流动相为甲醇与水的混合物,体积比80∶20,检测波长为222 nm,设置流速1 mL/min,检测温度30 ℃,进样量20 μL。
2 结果与讨论
2.1 BDD和Pt阳极在硫酸盐溶液中的CV曲线
Pt电极具有良好的电催化活性,但析氧副反应较为剧烈,以致产生的·OH更易生成O2析出,降低了电流效率。图 1对比了Pt电极与BDD电极在0.2 mol/L Na2SO4电解质中的CV曲线。
图1
2.2 BDD阳极电活化硫酸盐去除ATZ
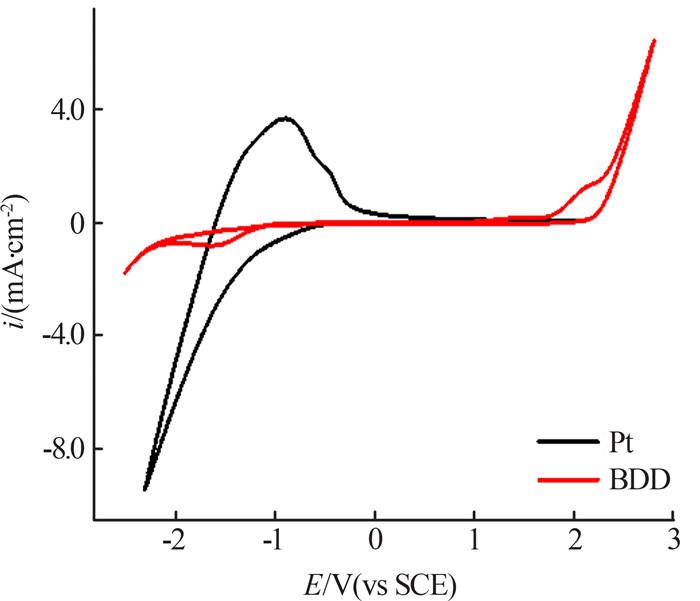
比较了直接投加PDS(2 mmol/L)、BDD阳极直接电解和BDD阳极活化硫酸盐实验条件下ATZ的降解效果,结果见图 2。
图2
表1 ATZ降解一级动力学反应速率常数
| 反应条件 | ATZ降解一级反应速率常数/min-1 | R2 |
| BDD阳极电活化硫酸盐 | 0.134 2 | 0.968 4 |
| BDD直接电解 | 0.009 4 | 0.982 9 |
| 直接投加PDS | 0.001 2 | 0.945 5 |
由表 1可见,不同反应条件下,ATZ的降解速率由大到小依次为BDD阳极电活化硫酸盐 > 直接电解 > 直接投加PDS。
2.3 SO4·-降解ATZ的相对贡献率
表2 竞争捕获实验的猝灭反应速率常数
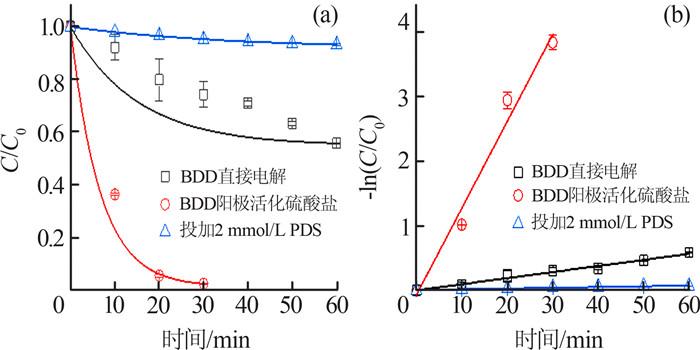
图3
在直接电解过程中,ATZ的降解速率主要由电极表面的直接电子转移和·OH氧化反应决定,其降解率为70.52%(120 min)。在自由基竞争捕获实验中,加入过量MeOH几乎能同时猝灭·OH和SO4·-,使ATZ的降解受到明显抑制,降解率减至29.84%(120 min)。而加入过量TBA后ATZ的降解率为56.25%(120 min),与加入MeOH相比,降解率有所增加。这是因为在相同条件下TBA不能有效猝灭SO4·-,证明BDD阳极电解硫酸盐过程中产生强氧化活性的SO4·-降解ATZ。在硫酸钠电解质中,30 min内ATZ降解了97.83%,可能是由于BDD阳极电活化硫酸盐产生SO4·-和·OH,协同作用于ATZ。
从化学动力学角度分析,ATZ的降解反应符合一级动力学,其拟合公式见表 3。
表3 不同实验条件下ATZ降解一级反应动力学模型
| 反应条件 | 拟合曲线 | R2 |
| 1 mol/L MeOH | y=0.002 8x+0.005 3 | 0.940 0 |
| 1 mol/L TBA | y=0.007 2x-0.028 1 | 0.994 6 |
| 无醇类/硫酸盐 | y=0.009 9x-0.005 2 | 0.991 4 |
| 硫酸钠 | y=0.134 2x-0.081 7 | 0.968 4 |
自由基猝灭剂对ATZ降解的抑制作用与其一级反应速率常数正相关,置信水平在95%附近,相关性良好。
用ATZ作为自由基探针,根据其在不同反应条件下的降解速率常数比值,计算氧化物种对ATZ降解的相对贡献率,结果如表 4所示。
表4 氧化物种对ATZ降解的相对贡献率
| 反应条件 | 氧化物种 | ATZ一级反应速率常数/min-1 | 相对贡献率/% |
| 硫酸钠 | DET+SO4·-+·OH | 0.134 2 | 100 |
| 无醇类/硫酸盐 | DET+·OH | 0.009 9 | 7.38 |
| 1 mol/L MeOH | DET | 0.002 8 | 2.09 |
| ·OH | 0.007 1 | 5.19 | |
| SO4·- | 0.124 3 | 92.62 |
2.4 SO4·-产生机理分析
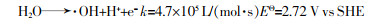
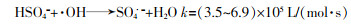
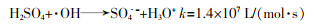
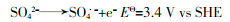
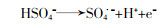
3 结论
硫酸盐溶液在电化学氧化降解有机污染物的过程中常被认为呈惰性。本研究在循环阳极电极模式下,对BDD阳极电活化硫酸盐去除ATZ与直接电解去除ATZ的效果进行比较,并用自由基竞争捕获法研究了BDD阳极电活化硫酸盐降解ATZ的自由基相对贡献率及可能机理。
(1)在循环阳极电解模式下,与传统直接电解相比,BDD阳极电活化硫酸盐可在更短时间内将ATZ降解完全。该过程无需额外投加PDS,且不会引起水体中原有硫酸盐浓度的升高,具有环境修复和节约药剂的双重效益。此外,PDS可在电解过程中生成,经分离纯化后可能具备一定的工业价值。
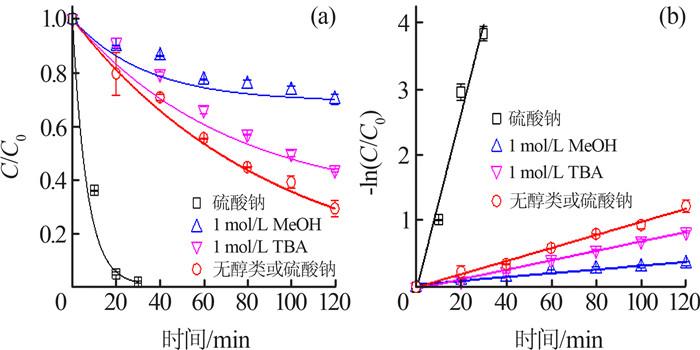
(2)由于BDD电极对反应活性物质具有弱吸附性,其表面会产生大量强氧化性的·OH,质子化的HSO4-和H2SO4被·OH氧化成SO4·-;此外,SO4·-可通过SO42-和HSO4-在电极表面的直接氧化而产生。
参考文献
Toward a green generation of oxidant on demand: practical electrosynthesis of ammonium persulfate
[J].
Electrochemical gene ration of persulfate and its performance on 4-bromophenol treatme nt
[J].DOI:10.1016/j.seppur.2018.06.071 [本文引用: 1]
Understanding electro chemically activated persulfate and its application to ciprofloxacin abatement
[J].
Detection of hydrate forms of lithium and sodium perchlorates in aqueous solutions using near infrared spectroscopy
[J].DOI:10.1255/jnirs.1107 [本文引用: 1]
Electrochemical activation of sulfate by BDD anode in basic medium for efficient re moval of organic pollutants
[J].DOI:10.1016/j.chemosphere.2018.07.043 [本文引用: 2]
Removal of 2-MIB and geos min using UV/persulfate: contributions of hydroxyl and sulfate radi cals
[J].DOI:10.1016/j.watres.2014.11.029 [本文引用: 4]
Rate constants for hydrogen abstraction rea ctions of the sulfate radical, SO4·-. Alcohols
[J].DOI:10.1002/kin.550210807 [本文引用: 2]
Production of sulfate radical and hydroxyl radical by reaction of ozone with peroxymonosulfate: a novel advanced oxidation process
[J].
Design and synthesis of cop per-cobalt catalysts for the selective conversion of synthesis gas to ethanol and higher alcohols
[J].DOI:10.1002/anie.201402680 [本文引用: 1]
Electrochemical oxidation of or ganics in sulfate solutions on boron-doped diamond electrode: Mul tiple pathways for sulfate radical generation
[J].DOI:10.1016/j.apcatb.2019.04.060 [本文引用: 1]
Understanding persulfate produc tion at boron doped diamond film anodes
[J].DOI:10.1016/j.electacta.2014.10.104 [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号