本研究以城市污泥为原料制备出污泥生物炭(BC),并通过Fe浸渍制备出磁性污泥生物炭(MBC)。考察溶液初始pH、吸附时间、共存离子、吸附温度以及Cd(Ⅱ)初始浓度等因素对BC和MBC去除Cd(Ⅱ)效果的影响,并通过FTIR分析MBC的去除机理。
1 材料与方法
1.1 生物炭及改性生物炭的制备
脱水的城市污泥取自石家庄某污水处理厂,取一定量的污泥在90 ℃的恒温烘箱中烘干至恒重。将烘干的干污泥通过研钵破碎后,过80目(0.177 mm)筛并收集过筛污泥粉末。称取一定量的污泥粉末置于坩埚中压实并盖紧坩埚盖,将坩埚在500 ℃的恒温马弗炉中热解3 h,取出坩埚得到的黑色固体为生物炭,记为BC。
磁性污泥生物炭的制备〔5〕:称取一定量的BC与FeCl3·6H2O固体按质量比1∶1加入到200 mL的溶液中,并采用0.1 mol/L NaOH溶液调节pH至11.0,再在80 ℃的恒温水浴锅中以150 r/min的转速搅拌2 h后,过滤并收集所得固体,在90 ℃的烘箱中干燥12 h后,所得固体记为MBC。
1.2 批量吸附试验
影响因素试验:考察溶液初始pH(2.0~8.0)和不同浓度(0~50 mg/L)阳离子(Ca2+、Zn2+、Cu2+和Pb2+)对生物炭去除Cd(Ⅱ)效果的影响。将10 mg的生物炭和25 mL 10 mg/L的Cd(Ⅱ)溶液加入到50 mL的锥形瓶中,并采用0.1 mol/L HNO3和NaOH溶液调节pH,并将调节pH后的锥形瓶在20 ℃、150 r/min的恒温摇床中吸附360 min。
动力学试验:称取10 mg生物炭和25 mL 10 mg/L的Cd(Ⅱ)溶液加入到50 mL锥形瓶中。将其置于20 ℃、150 r/min的恒温摇床中,分别于5、10、20、30、60、90、120、180、240、300、360、480 min后取出锥形瓶,考察吸附时间对生物炭去除Cd(Ⅱ)效果的影响。
等温吸附试验:称取10 mg的生物炭和量取25 mL不同质量浓度(10~150 mg/L)的Cd(Ⅱ)溶液加入到50 mL的锥形瓶中,并将锥形瓶置于不同温度(15、25、35 ℃)转速为150 r/min的恒温摇床中吸附360 min,考察不同吸附温度和Cd(Ⅱ)初始质量浓度对生物炭去除Cd(Ⅱ)的影响。
上述每组试验重复3次,以平均值为测定值并计算标准差。吸附达到平衡后的溶液采用0.22 μm进行过滤,收集滤液采用原子吸收分光光度法(AA-6300型,日本岛津)测定过滤液中Cd(Ⅱ)的浓度,并计算去除率和吸附量。
1.3 表征分析
通过V-Sorb 2800TP型比表面积及孔径分析仪(北京金埃谱科技有限公司),利用N2吸附-脱附等温线法分析BC和MBC表面积、孔体积和孔径;利用D8X型X衍射分析仪(德国布鲁克)分析污泥和生物炭晶型结构及物象组成;利用SUPRA40型扫描电子显微镜(德国蔡司)观察BC和MBC的表面结构;利用Zetasizer3000HS型Zate电位仪(英国马尔文公司)分析BC和MBC的零电势点;吸附前后的MBC通过Nicolet-460型傅里叶红外光谱分析仪(美国赛默飞公司)分析官能团特征变化。Cd(Ⅱ)在水溶液pH为2.0~8.5的物种分布通过软件visual MINTEQ3.1进行模拟。
1.4 吸附解吸试验
在25 ℃、溶液pH为6.0以及生物炭投加量为10 mg的条件下,对25 mL 10 mg/L的Cd(Ⅱ)溶液吸附360 min后,离心、过滤,收集生物炭,并将其加入到0.1 mol/L的HCl中振荡脱附2 h。之后将其过滤,用蒸馏水洗至中性,60 ℃恒温干燥后重复上述过程,计算每次吸附试验后的Cd(Ⅱ)去除率。
1.5 释放金属离子的测定
取25 ℃条件下,不同浓度的Cd(Ⅱ)被MBC吸附后的过滤溶液10 mL,利用原子吸收分光光度法测定溶液中Ca2+、Mg2+、Na+和K+的释放量,同时设置空白组以消除MBC表面金属离子的影响。
2 结果与讨论
2.1 生物炭的特征分析
生物炭的比表面积、孔体积和孔径变化见表 1。
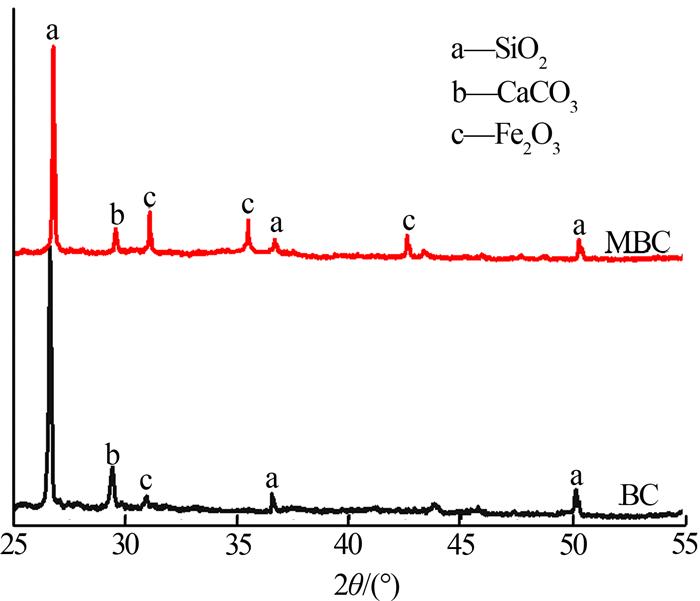
BC和MBC的SEM见图 1。
图1
由图 1可知,BC的表面光滑,存在大量的孔道;在MBC的表面出现很多颗粒物质,这些颗粒物质不仅占据了生物炭的表面,而且还占据了孔道,导致MBC的比表面积、孔体积及孔径减少。
BC和MBC的XRD见图 2。
图2
2.1 溶液初始pH对生物炭去除Cd(Ⅱ)效果的影响
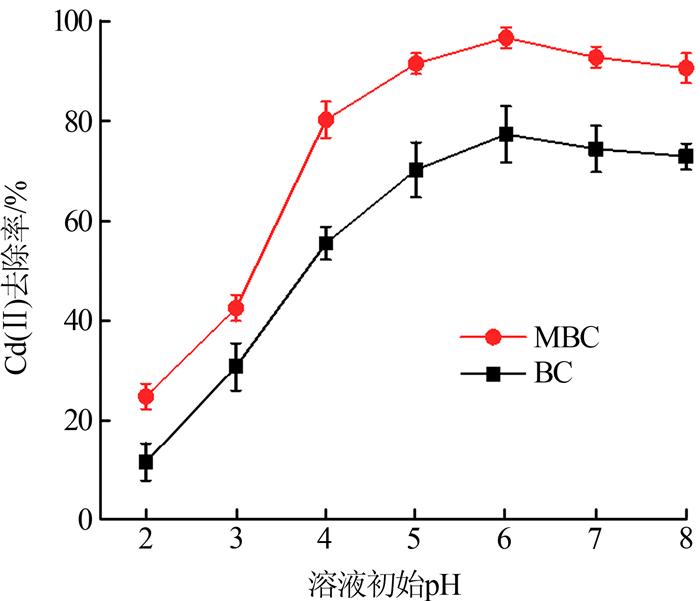
在温度为25 ℃,生物炭投加量为10 mg,25 mL 10 mg/L的Cd(Ⅱ)溶液,吸附时间为360 min的条件下,考察溶液初始pH对生物炭去除Cd(Ⅱ)效果的影响,结果见图 2。
图2
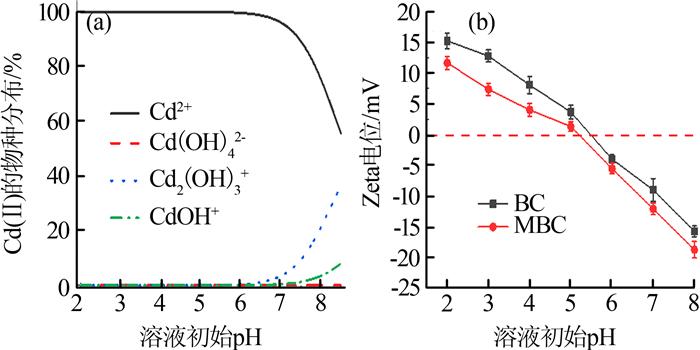
由图 2可知,pH为2.0时,BC和MBC对Cd(Ⅱ)的去除率分别为11.64%和24.80%;pH增加到6.0时,BC和MBC对Cd(Ⅱ)的去除率达到最大值,分别为77.44%和96.79%,pH增加到8.0时,BC和MBC对Cd(Ⅱ)的去除率分别下降到72.99%和90.73%。pH较低时,2种生物炭对Cd(Ⅱ)的去除率均较低,这是因为大量的H+占据吸附剂表面,并使其质子化带正电。
不同pH下Cd(Ⅱ)的物种分布和Zeta电位分析见图 3。
图3
2.2 吸附时间对BC和MBC去除Cd(Ⅱ)的影响
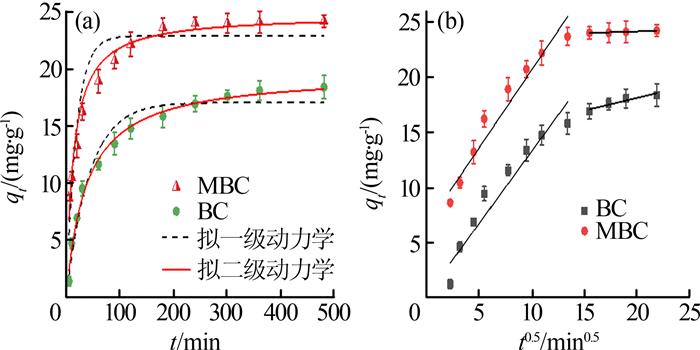
在温度为25 ℃,生物炭投加量为10 mg,Cd(Ⅱ)初始质量浓度为10 mg/L的溶液25 mL,溶液初始pH为6.0的条件下,考察吸附时间对生物炭去除Cd(Ⅱ)效果的影响,结果见图 4。
图4
由图 4可知,在BC和MBC去除Cd(Ⅱ)的过程中,大致可以分为三个阶段:第一阶段为快速吸附阶段,在5~120 min内,BC和MBC对Cd(Ⅱ)的吸附量分别从1.34、8.66 mg/g快速增加到14.76、22.17 mg/g;第二阶段为缓慢吸附阶段,在120~300 min内,BC和MBC对Cd(Ⅱ)的吸附量分别从14.76、22.17 mg/g缓慢增加到17.59、24.00 mg/g;第三阶段为吸附平衡阶段,在吸附240 min之后,吸附基本上达到吸附平衡。在吸附初始阶段吸附较快,是由于吸附剂表面存在大量的吸附位点,随着吸附时间的增加表面吸附位点减少导致吸附量增加变缓最后达到平衡〔9〕。此外MBC对Cd(Ⅱ)的吸附量一直高于BC,推测是因为引入了铁氧化物的原因。
为了进一步了解BC和MBC去除Cd(Ⅱ)的吸附过程,采用了拟一级动力学方程、拟二级动力学方程和颗粒内扩散模型进行拟合分析,结果见表 2。
表2 动力学拟合参数
| 吸附剂 | 拟一级动力学模型 | 拟二级动力学模型 | 颗粒内扩散模型 | |||||||||||
| qe/(mg·g-1) | k1/min-1 | R2 | qe/(mg·g-1) | k2/(g·mg-1·min-1) | R2 | kd1/(mg·m-1·min-0.5) | C1 | R2 | kd2/(mg·m-1·min-0.5) | C2 | R2 | |||
| BC | 17.05 | 0.023 | 0.912 | 19.65 | 0.001 | 0.993 | 1.301 | 0.30 | 0.934 | 0.228 | 13.57 | 0.903 | ||
| MBC | 22.90 | 0.054 | 0.895 | 24.76 | 0.003 | 0.974 | 1.406 | 6.60 | 0.952 | 0.031 | 23.51 | 0.948 | ||
2.3 吸附等温线
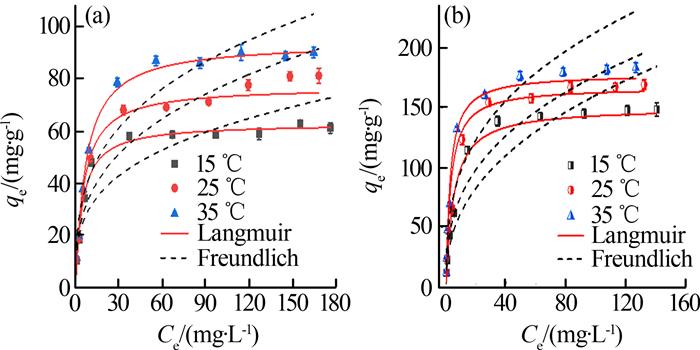
在初始溶液pH为6.0,生物炭投加量为10 mg及吸附时间为360 min的条件下,研究Cd(Ⅱ)的初始质量浓度及吸附温度对BC和MBC去除的影响,结果见图 5。
图5
通过Langmuir和Freundlich吸附等温线模型进行拟合,结果见表 3。
表3 BC和MBC对Cd(Ⅱ)的吸附等温模型拟合参数
| 吸附剂 | T/℃ | Langmuir | Freundlich | |||||
| qmax/(mg·g-1) | KL | R2 | KF | n | R2 | |||
| BC | 15 | 62.84 | 0.222 | 0.993 | 15.64 | 2.364 | 0.897 | |
| 25 | 76.93 | 0.187 | 0.988 | 16.44 | 2.985 | 0.946 | ||
| 35 | 93.92 | 0.148 | 0.971 | 21.06 | 3.181 | 0.924 | ||
| MBC | 15 | 150.35 | 0.202 | 0.967 | 24.36 | 2.440 | 0.934 | |
| 25 | 167.42 | 0.337 | 0.981 | 33.23 | 2.751 | 0.942 | ||
| 35 | 178.40 | 0.339 | 0.953 | 44.70 | 2.945 | 0.920 | ||
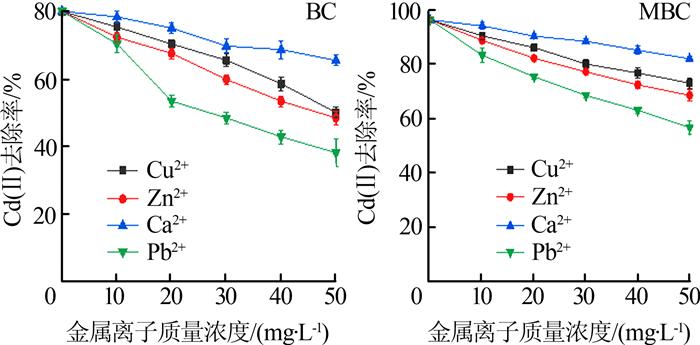
2.4 金属离子对去除Cd(Ⅱ)效果的影响
在溶液初始pH为6.0,生物炭投加量为10 mg,Cd(Ⅱ)质量浓度为10 mg/L,吸附时间为360 min,温度为25 ℃的条件下,考察金属离子质量浓度对不同种类金属离子去除Cd(Ⅱ)效果的影响,结果见图 6。
图6
2.5 MBC去除Cd(Ⅱ)的机理分析
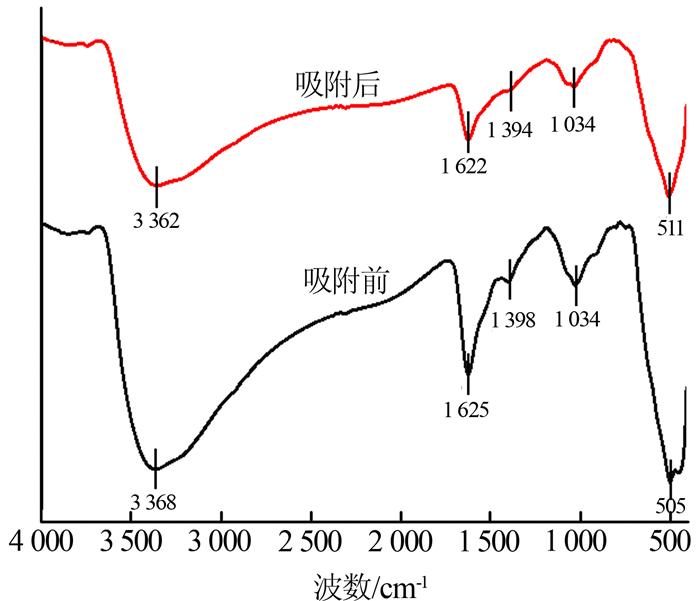
为了进一步证实MBC去除Cd(Ⅱ)的机理,采用FTIR技术对MBC吸附Cd(Ⅱ)前后进行官能团分析,结果见图 7。
图7
由图 7可知,吸附前,波长为3 368 cm-1处的吸收峰被认为是—OH峰〔1〕,在吸附后—OH偏移至3 362 cm-1处并出现了减弱,说明MBC中的—OH官能团参与吸附Cd(Ⅱ)的过程。在吸附前的FTIR光谱中,1 625 cm-1和1 398 cm-1处振动峰被分别认为是C=O和C—O的振动峰〔3〕;吸附后C=O和C—O振动峰都出现了减弱和偏移,分别偏移至1 622 cm-1和1 394 cm-1。在MBC中波长为1 034 cm-1处的振动峰为Si—O峰〔12〕,吸附前后Si—O振动峰也出现了减弱。在振动峰为505 cm-1处被认定为Fe—O基团,说明MBC中成功引入了大量的Fe—O基团,推测这也就是造成了MBC对Cd(Ⅱ)吸附量增加的原因;在吸附后Fe—O基团偏移至511 cm-1处并出现了减弱〔5, 9〕。通过上述FTIR分析表明,MBC中的—OH、C=O、C—O、Si—O以及Fe—O基团都参与了Cd(Ⅱ)的吸附。
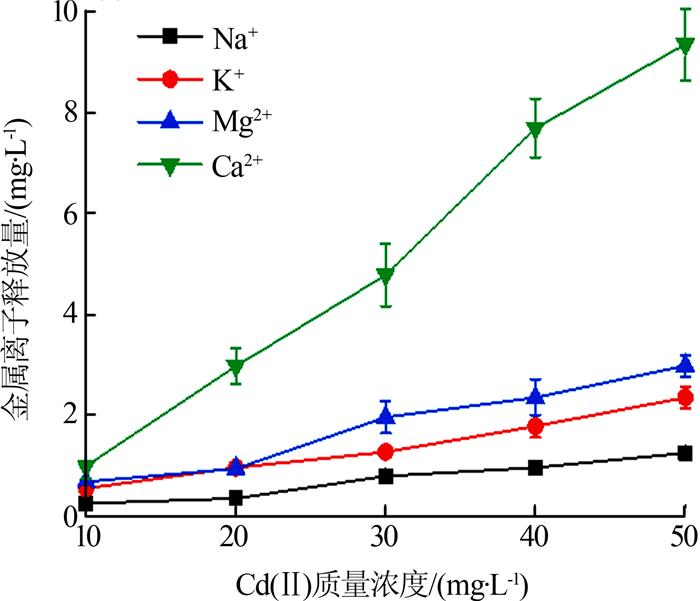
图8
由图 8可知,随着Cd(Ⅱ)初始质量浓度的增加,Na+、K+、Ca2+及Mg2+4种离子释放的浓度也随着增加,说明MBC在吸附过程中这些离子通过离子交换为Cd(Ⅱ)的去除提供吸附位点;其中Ca2+浓度的释放量最多,这也可能是由于MBC中本身的Ca2+含量较高造成的。
2.6 吸附解吸试验
在溶液初始pH为6.0,生物炭投加量为10 mg,Cd(Ⅱ)质量浓度为10 mg/L,吸附时间为360 min,温度为25 ℃的条件下,考察BC和MBC经过5次吸附解吸试验结果,经过5次吸附解吸试验结果表明,BC对Cd(Ⅱ)的去除率从80%左右下降到55.68%,而MBC对Cd(Ⅱ)的去除率保持在90%以上。说明Fe浸渍后的生物炭具有更好的去除率和再生能力,MBC具有更好地应用于去除水溶液中Cd(Ⅱ)的潜力。
3 结论
(1)经过Fe浸渍后,比表面积、孔径和孔体积都出现了减小,此外在MBC的表面出现很多颗粒状物质。
(2)BC和MBC对Cd(Ⅱ)的吸附过程复合拟二级动力学模型,属于化学吸附;Langmuir吸附等温模型能够更好地描述其吸附过程,属于单层吸附。在溶液初始pH为6.0,生物炭投加量为10 mg,Cd(Ⅱ)质量浓度为10 mg/L的溶液25 mL,吸附时间为360 min,温度为25 ℃的最佳条件下,BC和MBC对Cd(Ⅱ)的最大吸附量分别为76.93 mg/g和167.42 mg/g,说明Fe浸渍BC有效地提高了吸附量。此外,Cu2+、Zn2+、Ca2+及Pb2+等金属离子对去除起到了抑制作用。
(3)MBC对Cd(Ⅱ)的去除机理,包括Cd(Ⅱ)与MBC中的—OH、C=O、C—O、Si—O以及Fe—O等基团的络合,MBC中的Na+、K+、Ca2+及Mg2+等离子通过离子交换为去除Cd(Ⅱ)提供吸附位点及Cd(Ⅱ)与MBC之间的静电吸引等。
(4)经过5次吸附解吸试验表明:BC对Cd(Ⅱ)的去除率下降到55%左右,而MBC保持在90%以上,因此MBC具有更好应用于去除水溶液中Cd(Ⅱ)的潜力。
参考文献
不同温度桉树叶生物炭对Cd2+的吸附特性及机制
[J].DOI:10.3969/j.issn.1000-6923.2018.03.025 [本文引用: 2]
不同热解温度污泥生物炭对Pb2+, Cd2+的吸附特性
[J].DOI:10.12030/j.cjee.201507083 [本文引用: 3]
磁性生物炭复合材料研究进展
[J].DOI:10.3969/j.issn.1001-9731.2016.07.006 [本文引用: 3]
磁性生物质炭的制备方法研究进展
[J].DOI:10.3969/j.issn.1008-021X.2019.16.052 [本文引用: 2]
Preparation of rice straw-derived biochar for efficient cadmium removal by modification of oxygen-containing functional groups
[J].DOI:10.1016/j.scitotenv.2018.03.071 [本文引用: 1]
Adsorption of cadmium by biochar derived from municipal sewage sludge: Impact factors and adsorption mechanism
[J].DOI:10.1016/j.chemosphere.2015.04.052 [本文引用: 2]
磁性玉米秸秆生物炭对水体中Cd的去除作用及回收利用
[J].DOI:10.11975/j.issn.1002-6819.2018.19.027 [本文引用: 1]
Influence of pyrolysis temperature on characteristics and heavy metal adsorptive performance of biochar derived from municipal sewage sludge
[J].DOI:10.1016/j.biortech.2014.04.048 [本文引用: 1]






 津公网安备 12010602120337号
津公网安备 12010602120337号