Diverse and abundant antibiotic resistance genes in Chinese swine farms
1
2013
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
Occurrence and fate of eleven classes of antibiotics in two typical wastewater treatment plants in South China
1
2013
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
Residues of veterinary antibiotics in manures from feedlot livestock in eight provinces of China
2
2010
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
Comprehensive evaluation of antibiotics emission and fate in the river basins of China: Source analysis, multimedia modeling, and linkage to bacterial resistance
3
2015
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
Occurrence of antibiotics and antibiotic resistance genes in hospital and urban wastewaters and their impact on the receiving river
0
2015
Effluent from drug manufactures contains extremely high levels of pharmaceuticals
2
2007
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
Antibiotics in aquatic environments of China: A review and meta-analysis
3
2020
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 从表 2可以看出,ERY、AZI、CLA和ROX这四种抗生素在我国的许多江河湖泊中高频检出,可见我国的水环境普遍存在MA污染.地表水中这四类MA的平均质量浓度大多在3 ng/L以上,其中平均浓度最高的水域是洞庭湖.ROX在洞庭湖的平均质量浓度达到了惊人的1 250 ng/L,ERY和CLA也均高于100 ng/L,分别是107 ng/L和496 ng/L〔25〕.同时,最大浓度方面,多项检测远远高于200 ng/L,尤其是洞庭湖水体中的ROX达到了惊人的4 870 ng/L.此外,MA在地表水中的浓度分布存在区域差异和季节性差异,不同的湖泊其MA浓度存在较大差异〔7, 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
2
... 抗生素作为一种可以有效抑制或者杀灭病原体的药物,在医疗、水产及畜禽养殖等方面得到了广泛的应用〔1-6〕.当前中国已经成为了抗生素药品的主要生产国与使用国〔7〕.数据显示,我国每年抗生素的使用量达到了惊人的15~20万t,由此产生了大量的抗生素废水〔7〕.根据结构的不同,抗生素可分为磺胺类、大环内酯类、四环素类等〔3-4〕.其中,大环内酯类的使用量占所有抗生素使用量的26%,居于首位〔8〕. ...
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
Pharmaceuticals of emerging concern in aquatic systems: Chemistry, occurrence, effects, and removal methods
4
2019
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 抗生素被服用后,只有部分可以得到有效地利用,大量的大环内酯类抗生素未被利用就通过代谢排入到环境中〔9, 24〕.现有污水处理厂的污水处理工艺对MA的处理效果有限,近年来在地表环境和污水处理厂二级出水中大环内酯类抗生素被高频检出〔11, 13, 15〕.表 2列出了我国地表水中四种常见MA的浓度水平. ...
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
... 〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
Occurrence, removal, and risk assessment of antibiotics in 12 wastewater treatment plants from Dalian, China
6
2017
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
10〕
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
10〕
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
Occurrence and behavior of macrolide antibiotics in municipal wastewater treatment: Possible importance of metabolites, synthesis byproducts, and transformation products
4
2019
... 抗生素被服用后,只有部分可以得到有效地利用,大量的大环内酯类抗生素未被利用就通过代谢排入到环境中〔9, 24〕.现有污水处理厂的污水处理工艺对MA的处理效果有限,近年来在地表环境和污水处理厂二级出水中大环内酯类抗生素被高频检出〔11, 13, 15〕.表 2列出了我国地表水中四种常见MA的浓度水平. ...
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
11〕
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
11〕
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
A new method for macrolide antibiotics determination in wastewater from three different wastewater treatment plants
4
2017
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
12〕
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
12〕
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
12〕
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
Occurrence and fate of antibiotics in a wastewater treatment plant and their biological effects on receiving waters in Guizhou
5
2018
... 抗生素被服用后,只有部分可以得到有效地利用,大量的大环内酯类抗生素未被利用就通过代谢排入到环境中〔9, 24〕.现有污水处理厂的污水处理工艺对MA的处理效果有限,近年来在地表环境和污水处理厂二级出水中大环内酯类抗生素被高频检出〔11, 13, 15〕.表 2列出了我国地表水中四种常见MA的浓度水平. ...
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
13〕
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
13〕
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
13〕
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
Concentration and reduction of antibiotic residues in selected wastewater treatment plants and receiving waterbodies in Durban, South Africa
4
2019
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
14〕
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
14〕
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
14〕
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
Occurrence, removal and risk of organic micropollutants in wastewater treatment plants across China: Comparison of wastewater treatment processes
6
2018
... 抗生素被服用后,只有部分可以得到有效地利用,大量的大环内酯类抗生素未被利用就通过代谢排入到环境中〔9, 24〕.现有污水处理厂的污水处理工艺对MA的处理效果有限,近年来在地表环境和污水处理厂二级出水中大环内酯类抗生素被高频检出〔11, 13, 15〕.表 2列出了我国地表水中四种常见MA的浓度水平. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
15〕
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
15〕
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
15〕
注:"—"代表未说明或未检测. ...
Antibiotics in hospital effluent and domestic wastewater treatment plants in Doha, Qatar
3
2019
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 国内外污水厂大环内酯类抗生素的浓度分布
| 化合物 | 取样地 | 进水质量浓度/(ng·L-1) | 出水质量浓度/(ng·L-1) | 去除率/% | 参考文献 |
| ERY | 克罗地亚 | 26 | 19 | - | 〔11〕 |
| 南非 | 40.3 | - | 99 | 〔14〕 |
| 卡塔尔 | 376 | 167 | - | 〔16〕 |
| 捷克 | 50.88~148.70 | 45.72~82.55 | 12.91 | 〔12〕 |
| 贵州 | 258.64 | 148.21 | - | 〔13〕 |
| 大连 | 99.7~564.8 | 13.2~338.7 | -73.5~97.4 | 〔10〕 |
| 中国 | 1.1~1151.6 | 0.1~473.6 | - | 〔15〕 |
| AZI | 克罗地亚 | 5837 | 5453 | -11 | 〔11〕 |
| 南非 | 81.3 | - | - | 〔14〕 |
| 卡塔尔 | 85570 | 40327 | - | 〔16〕 |
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
... 〔
16〕
| 捷克 | 1291~1731 | 926.5~1404.0 | 26.07 | 〔12〕 |
| 贵州 | 376.39 | 83.12 | - | 〔13〕 |
| 大连 | 5.2~501.3 | 1.9~287.5 | -106.6~86.7 | 〔10〕 |
| 中国 | 1.5~1687.2 | 1.4~795.1 | - | 〔15〕 |
| CLA | 克罗地亚 | 828 | 266 | -56 | 〔11〕 |
| 南非 | 788.2 | - | 27.22 | 〔14〕 |
| 捷克 | 1283~1849 | 935.3~1394 | 27.22 | 〔12〕 |
| 贵州 | 37.21 | 5.39 | - | 〔13〕 |
| 大连 | 2.1~137.0 | 0.3~115.0 | -189.9~89.3 | 〔10〕 |
| 中国 | 4.9~550.3 | 1.3~214.6 | - | 〔15〕 |
| ROX | 南非 | 70.3 | - | 75 | 〔14〕 |
| 捷克 | 34.56~98.46 | 1800~4132 | 33.05 | 〔12〕 |
| 贵州 | 443.32 | 329.55 | - | 〔13〕 |
| 中国 | 38.8~1035.7 | 0.5~673.9 | - | 〔15〕 |
注:"—"代表未说明或未检测. ...
Efficient removal of the pharmaceutical pollutants included in the EU Watch List (Decision 2015/495) by modified magnetite/H2O2
5
2019
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
17〕
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
17〕
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... Fenton氧化所使用的试剂溶解性铁盐和H2O2所需成本较低且不会对环境构成威胁,体系产生的·OH又可以有效提升MA的去除率,所以Fenton法和类Fenton法被认为是最有效的降解新兴污染物的高级氧化法〔62-63〕.实际废水水质复杂,对催化体系影响因素的探究成为研究的热点,多数研究表明无机离子和天然有机物(NOM)的存在会影响Fenton氧化对MA的去除.Wei Li等〔55〕通过UV/H2O2工艺对ROX的降解实验发现,无机离子和高浓度NOM会使ROX的降解率降低,这表明在实际废水中该催化体系对ROX的降解将受到强抑制.Meng Li等〔39〕的研究也发现水体中NOM和阴离子的存在会对·OH主导的非均相Fenton过程有明显的抑制效果.因此,研究者试图通过材料改性等手段减轻离子及NOM对催化氧化过程的抑制,以期实现该体系在实际废水中的有效应用.E. Serrano等〔17〕探究了改性的磁铁矿和H2O2构成的催化体系对不同污水处理厂实际污水中ERY、CLA和AZI的去除效果,结果表明,改性磁铁矿体系在实际废水催化过程中,在保持低的铁浸出与高稳定性的基础上,达到了污染物和总大肠菌群的协同清除. ...
Health and ecological risk assessment of emerging contaminants(pharmaceuticals, personal care products, and artificial sweeteners) in surface and groundwater(drinking water) in the Ganges River Basin, India
3
2019
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... , 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
Occurrence, fate and environmental risk assessment of the organic microcontaminants included in the Watch Lists set by EU Decisions 2015/495 and 2018/840 in the groundwater of Spain
1
2019
... 大环内酯类抗生素(macrolide antibiotic,MA)是一种由12~16个碳原子的大中心环和一个或多个糖苷键共同组成的碱性亲脂性抗生素.MA可以对革兰氏阳性菌显示强的杀伤力,已经被广泛用于呼吸道和组织感染的抗菌治疗〔8〕.然而生物体对大环内酯类抗生素的吸收有限〔4〕,大比例的MA在生物体内未分解就被释放到环境中,造成了MA在环境中的暴露〔9〕.目前已经在多个城市污水处理厂周围水域中检测到MA的存在〔10-16〕.同时,欧盟(EU)已将红霉素(ERY)、克拉霉素(CLA)和阿奇霉素(AZI)这三种MA列为了水环境潜在危险化合物观察名单〔17〕.研究表明,MA在传统污水处理厂中的去除效果不明显〔18〕,这可能导致污水处理厂成为环境中大环内酯类抗生素的主要来源〔10, 18-19〕.因此,污水中MA的深度去除逐渐成为了降低水环境生态风险的必要措施. ...
林可霉素和3种大环内酯类抗生素对厌氧消化的影响
2
2021
... MA通常为无色的弱碱性化合物,有着较大的辛醇-水分配系数(LogKow),易溶于有机溶剂〔20〕.MA在水中溶解性差,但可与酸成盐(葡萄糖酸盐、乳糖酸盐、十二烷基硫酸盐)而变得易溶于水.这些物质在环境中可以持久性存在并有一定的生物富集性〔21〕.结构上,MA是一类以糖苷键与单糖或多糖相连的14~16元的大环,在酸性条件下易发生苷键水解,在碱性条件下其内酯容易换环破裂.其中,ERY、AZI、CLA和罗红霉素(ROX)这四种常见的大环内酯类抗生素的结构和性质如表 1所示〔20, 22-23〕. ...
... 〔20, 22-23〕. ...
Biotransformation of macrolide antibiotics using enriched activated sludge culture: Kinetics, transformation routes and ecotoxicological evaluation
6
2018
... MA通常为无色的弱碱性化合物,有着较大的辛醇-水分配系数(LogKow),易溶于有机溶剂〔20〕.MA在水中溶解性差,但可与酸成盐(葡萄糖酸盐、乳糖酸盐、十二烷基硫酸盐)而变得易溶于水.这些物质在环境中可以持久性存在并有一定的生物富集性〔21〕.结构上,MA是一类以糖苷键与单糖或多糖相连的14~16元的大环,在酸性条件下易发生苷键水解,在碱性条件下其内酯容易换环破裂.其中,ERY、AZI、CLA和罗红霉素(ROX)这四种常见的大环内酯类抗生素的结构和性质如表 1所示〔20, 22-23〕. ...
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
21〕
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
21〕
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为抗菌药物有较高的生物毒性,可对生物体甚至非靶标生物的生长和代谢产生抑制作用,而生物处理技术对于MA的毒性削减可以起到积极的作用〔21, 45〕.通过生物强化或共代谢等方式筛选和富集特异性降解MA的微生物是MA生物降解的关键.Shuting Zeng等〔54〕在厌氧消化工艺中通过高质量浓度CLA(> 10 mg/L)的环境富集和筛选了可降解CLA的微生物,进而放大了生物技术对MA毒性的削减作用.H. Fakhri等〔43〕也通过在HF-MBR反应器中添加限制假单胞菌使得细菌在抗生素和生长真菌的压力下进行特异性筛选,得到可以作为群体感应抑制剂的次生代谢物,来抵抗抗生素化合物对微生物的毒害作用.另一方面,MA的毒性生物削减工艺也促进了其他污染物的共代谢.G. T. H. Ooi等〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
... 四种MA有着相似的生物降解机理,大环内酯酶ERE酶解开环是MA生物降解过程的起始〔21, 45〕.之后涉及两种可能的降解途径,其一是开环中间产物通过连续酶解发生羟基氧化或磷酸化、N-氧化和N-去甲基化反应脱去脱糖胺和枝糖形成中间产物,中间产物进一步氧化脱水生成更小分子质量的降解产物.另一种反应途径是在开环后首先发生羟基氧化形成中间产物,进而遵循第一种反应途径完成降解过程〔45〕. ...
Pharmaceuticals and personal care products in water, sediments, aquatic organisms, and fish feeds in the Pearl River Delta: Occurrence, distribution, potential sources, and health risk assessment
2
2019
... MA通常为无色的弱碱性化合物,有着较大的辛醇-水分配系数(LogKow),易溶于有机溶剂〔20〕.MA在水中溶解性差,但可与酸成盐(葡萄糖酸盐、乳糖酸盐、十二烷基硫酸盐)而变得易溶于水.这些物质在环境中可以持久性存在并有一定的生物富集性〔21〕.结构上,MA是一类以糖苷键与单糖或多糖相连的14~16元的大环,在酸性条件下易发生苷键水解,在碱性条件下其内酯容易换环破裂.其中,ERY、AZI、CLA和罗红霉素(ROX)这四种常见的大环内酯类抗生素的结构和性质如表 1所示〔20, 22-23〕. ...
... 四种常见的MA结构中有多个含O或含N官能团,因而可以通过静电作用、氢键作用、π-π作用、n-π作用、孔填充效应及疏水协同作用等作用力被吸附材料吸附去除〔22, 57, 66-67〕.如在BCN对ROX的吸附中,化学吸附过程中的疏水作用和静电作用是影响材料吸附性能的重要因素〔57〕. ...
抗生素在城市污水处理过程中的去除研究进展
1
2019
... MA通常为无色的弱碱性化合物,有着较大的辛醇-水分配系数(LogKow),易溶于有机溶剂〔20〕.MA在水中溶解性差,但可与酸成盐(葡萄糖酸盐、乳糖酸盐、十二烷基硫酸盐)而变得易溶于水.这些物质在环境中可以持久性存在并有一定的生物富集性〔21〕.结构上,MA是一类以糖苷键与单糖或多糖相连的14~16元的大环,在酸性条件下易发生苷键水解,在碱性条件下其内酯容易换环破裂.其中,ERY、AZI、CLA和罗红霉素(ROX)这四种常见的大环内酯类抗生素的结构和性质如表 1所示〔20, 22-23〕. ...
Occurrence and fate of antibiotics, antibiotic resistant genes(ARGs) and antibiotic resistant bacteria(ARB) in municipal wastewater treatment plant: An overview
2
2020
... 抗生素被服用后,只有部分可以得到有效地利用,大量的大环内酯类抗生素未被利用就通过代谢排入到环境中〔9, 24〕.现有污水处理厂的污水处理工艺对MA的处理效果有限,近年来在地表环境和污水处理厂二级出水中大环内酯类抗生素被高频检出〔11, 13, 15〕.表 2列出了我国地表水中四种常见MA的浓度水平. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
Occurrence and ecological risk of pharmaceutical and personal care products in surface water of the Dongting Lake, China-during rainstorm period
5
2019
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
25〕
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
25〕
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 从表 2可以看出,ERY、AZI、CLA和ROX这四种抗生素在我国的许多江河湖泊中高频检出,可见我国的水环境普遍存在MA污染.地表水中这四类MA的平均质量浓度大多在3 ng/L以上,其中平均浓度最高的水域是洞庭湖.ROX在洞庭湖的平均质量浓度达到了惊人的1 250 ng/L,ERY和CLA也均高于100 ng/L,分别是107 ng/L和496 ng/L〔25〕.同时,最大浓度方面,多项检测远远高于200 ng/L,尤其是洞庭湖水体中的ROX达到了惊人的4 870 ng/L.此外,MA在地表水中的浓度分布存在区域差异和季节性差异,不同的湖泊其MA浓度存在较大差异〔7, 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
... , 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
Occurrence and ecological risk assessment of 22 emerging contaminants in the Jilin Songhua River(Northeast China)
1
2018
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
The distribution and partitioning of common antibiotics in water and sediment of the Pearl River Estuary, South China
6
2013
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
27〕
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
27〕
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
27〕
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 从表 2可以看出,ERY、AZI、CLA和ROX这四种抗生素在我国的许多江河湖泊中高频检出,可见我国的水环境普遍存在MA污染.地表水中这四类MA的平均质量浓度大多在3 ng/L以上,其中平均浓度最高的水域是洞庭湖.ROX在洞庭湖的平均质量浓度达到了惊人的1 250 ng/L,ERY和CLA也均高于100 ng/L,分别是107 ng/L和496 ng/L〔25〕.同时,最大浓度方面,多项检测远远高于200 ng/L,尤其是洞庭湖水体中的ROX达到了惊人的4 870 ng/L.此外,MA在地表水中的浓度分布存在区域差异和季节性差异,不同的湖泊其MA浓度存在较大差异〔7, 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
... 〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
Antibiotic contamination in a typical developing city in south China: Occurrence and ecological risks in the Yongjiang River impacted by tributary discharge and anthropogenic activities
7
2013
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
28〕
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
Occurrence of pharmaceuticals and personal care products and associated environmental risks in the central and lower Yangtze river, China
4
2014
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
29〕
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
29〕
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
29〕
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
Occurrence of pharmaceuticals and personal care products, and their associated environmental risks in a large shallow lake in north China
3
2018
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 〔
30〕
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
... 从表 2可以看出,ERY、AZI、CLA和ROX这四种抗生素在我国的许多江河湖泊中高频检出,可见我国的水环境普遍存在MA污染.地表水中这四类MA的平均质量浓度大多在3 ng/L以上,其中平均浓度最高的水域是洞庭湖.ROX在洞庭湖的平均质量浓度达到了惊人的1 250 ng/L,ERY和CLA也均高于100 ng/L,分别是107 ng/L和496 ng/L〔25〕.同时,最大浓度方面,多项检测远远高于200 ng/L,尤其是洞庭湖水体中的ROX达到了惊人的4 870 ng/L.此外,MA在地表水中的浓度分布存在区域差异和季节性差异,不同的湖泊其MA浓度存在较大差异〔7, 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
太湖表层沉积物中PPCPs的时空分布特征及潜在风险
1
2016
... 中国地表水中大环内酯类抗生素的浓度水平
| 化合物 | 取样地 | 最小质量浓度/(ng·L-1) | 最大质量浓度/(ng·L-1) | 平均质量浓度/(ng·L-1) | 中位质量浓度/(ng·L-1) | 参考文献 |
| ERY | 洞庭湖 | ND | 780 | 107 | - | 〔25〕 |
| 松花江 | ND | 121 | 29.9 | 21 | 〔26〕 |
| 珠江旱季 | - | 20 | 13.6 | 12.5 | 〔27〕 |
| 珠江雨季 | - | 7.3 | 2.1 | 1.5 | 〔27〕 |
| 邕江干流 | 2.6 | 46.4 | 7.7 | 3.6 | 〔28〕 |
| 邕江支流 | 2.9 | 174 | 43.5 | 17.2 | 〔28〕 |
| 长江中下游 | - | 808 | 296 | - | 〔29〕 |
| 白洋淀 | ND | 107.26 | 37.89 | 20.69 | 〔30〕 |
| AZI | 邕江干流 | ND | 5.8 | 0.62 | 0.27 | 〔28〕 |
| 邕江支流 | ND | 17.7 | 3.7 | 0.87 | 〔28〕 |
| 白洋淀 | ND | 215.06 | 45.277 | 25.55 | 〔30〕 |
| 太湖 | ND | 159 | 27.5 | 62.3 | 〔31〕 |
| CLA | 洞庭湖 | ND | 1720 | 496 | - | 〔25〕 |
| 邕江干流 | ND | 5.8 | 0.62 | ND | 〔28〕 |
| 邕江支流 | ND | 17.8 | 3 | ND | 〔28〕 |
| 长江中下游 | - | 103 | 18 | - | 〔29〕 |
| 鄱阳湖 | - | - | 0.4 | - | 〔29〕 |
| 巢湖 | - | - | 10.6 | - | 〔29〕 |
| ROX | 洞庭湖 | ND | 4870 | 1250 | - | 〔25〕 |
| 黄浦江 | 0.4 | 6.9 | 3.9 | - | 〔27〕 |
| 黄浦江 | 0.2 | 2.2 | 0.9 | - | 〔27〕 |
| 邕江干流 | ND | 6.1 | 0.51 | 0.3 | 〔28〕 |
| 邕江支流 | ND | 19.2 | 4.9 | 1.6 | 〔2〕 |
注:ND代表未检出;"—"代表未说明或未检测. ...
Antibiotics in soil and water in China-A systematic review and source analysis
2
2020
... 从表 2可以看出,ERY、AZI、CLA和ROX这四种抗生素在我国的许多江河湖泊中高频检出,可见我国的水环境普遍存在MA污染.地表水中这四类MA的平均质量浓度大多在3 ng/L以上,其中平均浓度最高的水域是洞庭湖.ROX在洞庭湖的平均质量浓度达到了惊人的1 250 ng/L,ERY和CLA也均高于100 ng/L,分别是107 ng/L和496 ng/L〔25〕.同时,最大浓度方面,多项检测远远高于200 ng/L,尤其是洞庭湖水体中的ROX达到了惊人的4 870 ng/L.此外,MA在地表水中的浓度分布存在区域差异和季节性差异,不同的湖泊其MA浓度存在较大差异〔7, 25-27, 30〕,同一水体在雨季和旱季MA的浓度也有很明显的差异〔27〕.即使不同水体中MA的浓度分布存在一定的差异,但总体来讲其浓度已经超过了环境风险的临界值.目前中国已经是抗生素生产最多的国家之一,随着社会经济的发展,MA的环境风险很可能进一步升高〔32〕. ...
... 除了生产量大之外,我国还是主要的抗生素消费国〔32〕.MA主要用于人类治疗和畜禽以及水产养殖的使用〔3-6〕.我国2013年消费了约16.2万t的抗生素,其中至少5万t的抗生素被排入到水和土壤中,因此污水处理厂成了接收抗生素废水的主要场所〔24〕.近年来MA在国内外各大污水处理厂中高频检出,其浓度水平存在区域差异,质量浓度在ng/L到μg/L之间.表 3列出了国内外各污水处理厂MA的进出水浓度分布水平及去除率情况.Weiwei Ben等〔15〕调研了中国14个污水处理厂中的42种微量污染物后发现,大环内酯类抗生素是污水处理厂出水中主要的微量污染物.Xin Zhang等〔10〕对大连市12个污水处理厂的29种抗生素研究后发现ERY、CLA和AZI在出水中检出最多.值得注意的是,这三种抗生素在部分污水处理厂的出水浓度远远大于进水浓度,造成去除率的负增长.同时经过验证,ERY和CLA的风险熵(RQ)值均大于1,可见传统的污水处理过程并不能对MA进行有效去除且易对污水处理厂排污点附近的水生生物造成生态风险,值得进一步的关注. ...
The antibiotic resistance "mobilome": Searching for the link between environment and clinic
1
2013
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
Adverse-effects of macrolide antibacterials
0
1993
Pharmaceuticals in freshwater aquatic environments: A comparison of the African and European challenge
1
2019
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
1
... 大多数药用MA被人类和动物使用后通过排泄进入下水道管网而汇入城市污水处理厂,进而排入水环境〔4, 9, 18〕.尽管与COD等常规指标相比,二级出水中MA的浓度不是很高,但由于物质的富集作用,留存于水环境中的MA可以通过一定的途径进入生物体,进而引发抗生素抗性的表达,造成肠胃刺激和过敏等应激反应,危害人体健康〔9, 33-35〕.针对这些可能的环境风险,我国食品安全国家标准《GB 31650- 2019》对MA的最大残留限量做了相关的规定.规定要求,在食品中残留的ERY的质量浓度为40~60 μg/kg,CLA的质量浓度为100~400 μg/kg.与此同时,欧洲共同体已经完全禁止了MA作为饲料添加剂的使用〔36〕. ...
Elimination of macrolides in water bodies using photochemical oxidation
3
2018
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
37〕
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 相比于Fenton氧化需要耗费大量的试剂且运行条件受水质影响较大的特点,光催化氧化处理的成本低,运行稳定,被广泛应用于抗生素废水的处理〔38, 47〕.单独的光催化处理效果有限,需通过强化技术进一步加强光催化对MA的去除能力.S. Wohl- muth da Silva等〔49〕利用电化学强化了紫外光催化对AZI的矿化效果,因为低浓度下传质限制被克服,相比于单独电化学和单独的光催化处理,强化工艺对AZI的矿化率分别提升33%和12%.与此同时,现有的光催化研究已经展现出了良好的毒性削减效果.M. Voigt等〔37〕在研究紫外光照射对ERY和AZI的光诱导降解作用时发现,光辐射在促进MA降解的同时,可以有效削减MA及其光降解产物的毒性.N. F. F. Moreira等〔40〕也通过TiO2光催化处理市政污水处理厂实际废水验证了复杂水质下光催化对母体污染物及反应产物毒性的有效削减. ...
TiO2 assisted photocatalytic degradation of macrolide antibiotics
4
2017
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
38〕
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
38〕
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 相比于Fenton氧化需要耗费大量的试剂且运行条件受水质影响较大的特点,光催化氧化处理的成本低,运行稳定,被广泛应用于抗生素废水的处理〔38, 47〕.单独的光催化处理效果有限,需通过强化技术进一步加强光催化对MA的去除能力.S. Wohl- muth da Silva等〔49〕利用电化学强化了紫外光催化对AZI的矿化效果,因为低浓度下传质限制被克服,相比于单独电化学和单独的光催化处理,强化工艺对AZI的矿化率分别提升33%和12%.与此同时,现有的光催化研究已经展现出了良好的毒性削减效果.M. Voigt等〔37〕在研究紫外光照射对ERY和AZI的光诱导降解作用时发现,光辐射在促进MA降解的同时,可以有效削减MA及其光降解产物的毒性.N. F. F. Moreira等〔40〕也通过TiO2光催化处理市政污水处理厂实际废水验证了复杂水质下光催化对母体污染物及反应产物毒性的有效削减. ...
Enhanced oxidation of erythromycin by persulfate activated iron powder-H2O2 system: Role of the surface Fe species and synergistic effect of hydroxyl and sulfate radicals
2
2017
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... Fenton氧化所使用的试剂溶解性铁盐和H2O2所需成本较低且不会对环境构成威胁,体系产生的·OH又可以有效提升MA的去除率,所以Fenton法和类Fenton法被认为是最有效的降解新兴污染物的高级氧化法〔62-63〕.实际废水水质复杂,对催化体系影响因素的探究成为研究的热点,多数研究表明无机离子和天然有机物(NOM)的存在会影响Fenton氧化对MA的去除.Wei Li等〔55〕通过UV/H2O2工艺对ROX的降解实验发现,无机离子和高浓度NOM会使ROX的降解率降低,这表明在实际废水中该催化体系对ROX的降解将受到强抑制.Meng Li等〔39〕的研究也发现水体中NOM和阴离子的存在会对·OH主导的非均相Fenton过程有明显的抑制效果.因此,研究者试图通过材料改性等手段减轻离子及NOM对催化氧化过程的抑制,以期实现该体系在实际废水中的有效应用.E. Serrano等〔17〕探究了改性的磁铁矿和H2O2构成的催化体系对不同污水处理厂实际污水中ERY、CLA和AZI的去除效果,结果表明,改性磁铁矿体系在实际废水催化过程中,在保持低的铁浸出与高稳定性的基础上,达到了污染物和总大肠菌群的协同清除. ...
Photocatalytic ozonation of urban wastewater and surface water using immobilized TiO2 with LEDs: Micropollutants, antibiotic resistance genes and estrogenic activity
3
2016
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
40〕
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 相比于Fenton氧化需要耗费大量的试剂且运行条件受水质影响较大的特点,光催化氧化处理的成本低,运行稳定,被广泛应用于抗生素废水的处理〔38, 47〕.单独的光催化处理效果有限,需通过强化技术进一步加强光催化对MA的去除能力.S. Wohl- muth da Silva等〔49〕利用电化学强化了紫外光催化对AZI的矿化效果,因为低浓度下传质限制被克服,相比于单独电化学和单独的光催化处理,强化工艺对AZI的矿化率分别提升33%和12%.与此同时,现有的光催化研究已经展现出了良好的毒性削减效果.M. Voigt等〔37〕在研究紫外光照射对ERY和AZI的光诱导降解作用时发现,光辐射在促进MA降解的同时,可以有效削减MA及其光降解产物的毒性.N. F. F. Moreira等〔40〕也通过TiO2光催化处理市政污水处理厂实际废水验证了复杂水质下光催化对母体污染物及反应产物毒性的有效削减. ...
Removal of pharmaceutically active compounds by using low-pressure membrane processes
2
2017
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 膜分离技术是利用两相之间理化性质的差异达到二者分离的过程.砂滤、纳滤、超滤等膜分离技术是水环境中MA的有效去除手段.溶液的pH以及溶质的解离常数和辛醇-水分配系数等理化性质影响着膜分离过程〔41〕,通过其他技术来强化膜分离过程也是提高MA去除效率的有效手段.P. Kulkarni等〔50〕用ZVI强化砂滤过程来抵抗pH对MA的吸附影响,使得未经pH调整的再生水中的MA可被有效去除.L. Sbardella等〔51〕则通过生物活性炭滤池强化了超滤过程对MA的去除效果,使得AZI的去除率提升了32%. ...
Efficient removal of antibiotics by a novel magnetic adsorbent: Magnetic activated carbon/chitosan(MACC) nanocomposite
4
2017
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 四种常见的MA均有较大的辛醇-水分配系数,疏水性极强,可以利用吸附技术将MA从水相吸附到固相吸附剂上来达到去除污染物的目的.一直以来吸附剂的再生性能和吸附性能的提升是研究者主要的关注点〔42, 53, 57〕.S. T. Danalioǧlu等〔42〕合成了磁铁矿壳聚糖活性炭(MACC)用于吸附去除ERY,材料在保持高比表面积的同时也有良好的磁选回收性能.Gang Wang等〔57〕制备的多孔氮化硼-碳纳米片(BCN)吸附材料通过空气中简单的高温处理即可实现吸附剂的再生,且6次循环后仍能保持91.9%以上的吸附容量.吸附性能方面,MA的吸附过程会受到静电作用等分子间作用的影响,强化这些分子间的作用是提升材料吸附性能的有效途径〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... 〔42〕合成了磁铁矿壳聚糖活性炭(MACC)用于吸附去除ERY,材料在保持高比表面积的同时也有良好的磁选回收性能.Gang Wang等〔57〕制备的多孔氮化硼-碳纳米片(BCN)吸附材料通过空气中简单的高温处理即可实现吸附剂的再生,且6次循环后仍能保持91.9%以上的吸附容量.吸附性能方面,MA的吸附过程会受到静电作用等分子间作用的影响,强化这些分子间的作用是提升材料吸附性能的有效途径〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... 〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
Bioaugmentation with immobilized endophytic Penicillium restrictum to improve quorum quenching activity for biofouling control in an aerobic hollow-fiber membrane bioreactor treating antibiotic-containing wastewater
2
2021
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为抗菌药物有较高的生物毒性,可对生物体甚至非靶标生物的生长和代谢产生抑制作用,而生物处理技术对于MA的毒性削减可以起到积极的作用〔21, 45〕.通过生物强化或共代谢等方式筛选和富集特异性降解MA的微生物是MA生物降解的关键.Shuting Zeng等〔54〕在厌氧消化工艺中通过高质量浓度CLA(> 10 mg/L)的环境富集和筛选了可降解CLA的微生物,进而放大了生物技术对MA毒性的削减作用.H. Fakhri等〔43〕也通过在HF-MBR反应器中添加限制假单胞菌使得细菌在抗生素和生长真菌的压力下进行特异性筛选,得到可以作为群体感应抑制剂的次生代谢物,来抵抗抗生素化合物对微生物的毒害作用.另一方面,MA的毒性生物削减工艺也促进了其他污染物的共代谢.G. T. H. Ooi等〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
Cometabolic removal of organic micropollutants by enriched nitrite-dependent anaerobic methane oxidizing cultures
3
2021
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
44〕
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为抗菌药物有较高的生物毒性,可对生物体甚至非靶标生物的生长和代谢产生抑制作用,而生物处理技术对于MA的毒性削减可以起到积极的作用〔21, 45〕.通过生物强化或共代谢等方式筛选和富集特异性降解MA的微生物是MA生物降解的关键.Shuting Zeng等〔54〕在厌氧消化工艺中通过高质量浓度CLA(> 10 mg/L)的环境富集和筛选了可降解CLA的微生物,进而放大了生物技术对MA毒性的削减作用.H. Fakhri等〔43〕也通过在HF-MBR反应器中添加限制假单胞菌使得细菌在抗生素和生长真菌的压力下进行特异性筛选,得到可以作为群体感应抑制剂的次生代谢物,来抵抗抗生素化合物对微生物的毒害作用.另一方面,MA的毒性生物削减工艺也促进了其他污染物的共代谢.G. T. H. Ooi等〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
Biological removal of pharmaceuticals from hospital wastewater in a pilot-scale staged moving bed biofilm reactor(MBBR) utilising nitrifying and denitrifying processes
7
2018
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
45〕
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
45〕
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为抗菌药物有较高的生物毒性,可对生物体甚至非靶标生物的生长和代谢产生抑制作用,而生物处理技术对于MA的毒性削减可以起到积极的作用〔21, 45〕.通过生物强化或共代谢等方式筛选和富集特异性降解MA的微生物是MA生物降解的关键.Shuting Zeng等〔54〕在厌氧消化工艺中通过高质量浓度CLA(> 10 mg/L)的环境富集和筛选了可降解CLA的微生物,进而放大了生物技术对MA毒性的削减作用.H. Fakhri等〔43〕也通过在HF-MBR反应器中添加限制假单胞菌使得细菌在抗生素和生长真菌的压力下进行特异性筛选,得到可以作为群体感应抑制剂的次生代谢物,来抵抗抗生素化合物对微生物的毒害作用.另一方面,MA的毒性生物削减工艺也促进了其他污染物的共代谢.G. T. H. Ooi等〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
... 〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
... 四种MA有着相似的生物降解机理,大环内酯酶ERE酶解开环是MA生物降解过程的起始〔21, 45〕.之后涉及两种可能的降解途径,其一是开环中间产物通过连续酶解发生羟基氧化或磷酸化、N-氧化和N-去甲基化反应脱去脱糖胺和枝糖形成中间产物,中间产物进一步氧化脱水生成更小分子质量的降解产物.另一种反应途径是在开环后首先发生羟基氧化形成中间产物,进而遵循第一种反应途径完成降解过程〔45〕. ...
... 〔45〕. ...
Effective elimination of fifteen relevant pharmaceuticals in hospital wastewater from Colombia by combination of a biological system with a sonochemical process
4
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
46〕
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 〔
46〕
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为微量污染物,单独的处理工艺往往很难做到污染物降解和毒性削减的协同.从MA去除的有效性和出水生物毒性来考虑,耦合工艺是一种比较好的选择.E. A. Serna-Galvis等〔46〕将生物-超声/光Fenton工艺有效组合起来,利用生物工艺预处理去除糖、肽和脂类等宏量污染物,利用催化氧化体系来氧化降解医疗废水中MA药物,相比于单独的化学处理,组合工艺有很好的协同效果,药物去除率从58.82%提升至82.86%.Haidong Zhou等〔58〕则将ZVI和厌氧消化工艺耦合起来,利用ZVI作为还原剂来降低系统的氧化还原电位(ORP值),在增加系统微生物多样性的同时,驯化出适宜抗生素去除及毒性削减的特异菌群,原位强化了厌氧消化工艺对MA的去除. ...
石墨烯负载TiO2光催化降解阿奇霉素废水
4
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 相比于Fenton氧化需要耗费大量的试剂且运行条件受水质影响较大的特点,光催化氧化处理的成本低,运行稳定,被广泛应用于抗生素废水的处理〔38, 47〕.单独的光催化处理效果有限,需通过强化技术进一步加强光催化对MA的去除能力.S. Wohl- muth da Silva等〔49〕利用电化学强化了紫外光催化对AZI的矿化效果,因为低浓度下传质限制被克服,相比于单独电化学和单独的光催化处理,强化工艺对AZI的矿化率分别提升33%和12%.与此同时,现有的光催化研究已经展现出了良好的毒性削减效果.M. Voigt等〔37〕在研究紫外光照射对ERY和AZI的光诱导降解作用时发现,光辐射在促进MA降解的同时,可以有效削减MA及其光降解产物的毒性.N. F. F. Moreira等〔40〕也通过TiO2光催化处理市政污水处理厂实际废水验证了复杂水质下光催化对母体污染物及反应产物毒性的有效削减. ...
... ERY、ROX和CLA有着相似的分子结构,因而其氧化降解机理类似〔47〕.图 1所示为化学氧化过程中·OH对MA分子的可能进攻位点〔68〕.在·OH主导的MA化学氧化过程中,·OH亲电攻击MA上的l-枝糖取代基,使得MA羟基化或羟基取代基被氧化,进而生成一系列羟基化产物、甲基化产物、羟甲基化产物、无机物和小分子物质.以红霉素的降解为例,冯奇奇〔69〕在研究光催化下ERY的降解机理时发现在·OH的攻击下ERY有三条降解途径.其一是·OH的攻击脱下了ERY上的去氧氨糖、克拉定糖和内酯环,之后中间产物继续被攻击开环而变成分子质量更小的物质;其二是ERY分子首先脱甲基成m/z=719的中间产物,该中间产物继续在脱甲基、脱氨、脱水、开环和羟基取代作用下生成一系列小分子物质;其三是ERY直接开环,进而继续逐步降解为小分子物质. ...
... AZI因为分子结构与其他三种MA差异较大,其化学降解有所不同.郝彤遥等〔47〕在研究AZI的光催化降解机理中发现,AZI会经过"AZI→去胺基糖阿奇霉素→内酯环→简单化合物"这一途径降解.在·OH的攻击下内酯环、胺基糖和克拉糖被氧化成羰基,导致AZI瞬间裂解生成一系列中间产物,其具体的中间产物及降解途径如图 2所示.由于这些中间产物中的内酯环类会因·OH的持续攻击其他中间产物而生成,在彻底降解前会有一段浓度增高的时期. ...
Sonochemical degradation of azithromycin in aqueous solution
1
2018
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
Antibiotics mineralization by electrochemical and UV-based hybrid processes: Evaluation of the synergistic effect
2
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 相比于Fenton氧化需要耗费大量的试剂且运行条件受水质影响较大的特点,光催化氧化处理的成本低,运行稳定,被广泛应用于抗生素废水的处理〔38, 47〕.单独的光催化处理效果有限,需通过强化技术进一步加强光催化对MA的去除能力.S. Wohl- muth da Silva等〔49〕利用电化学强化了紫外光催化对AZI的矿化效果,因为低浓度下传质限制被克服,相比于单独电化学和单独的光催化处理,强化工艺对AZI的矿化率分别提升33%和12%.与此同时,现有的光催化研究已经展现出了良好的毒性削减效果.M. Voigt等〔37〕在研究紫外光照射对ERY和AZI的光诱导降解作用时发现,光辐射在促进MA降解的同时,可以有效削减MA及其光降解产物的毒性.N. F. F. Moreira等〔40〕也通过TiO2光催化处理市政污水处理厂实际废水验证了复杂水质下光催化对母体污染物及反应产物毒性的有效削减. ...
Zerovalent iron-sand filtration can reduce the concentration of multiple antimicrobials in conventionally treated reclaimed water
2
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 膜分离技术是利用两相之间理化性质的差异达到二者分离的过程.砂滤、纳滤、超滤等膜分离技术是水环境中MA的有效去除手段.溶液的pH以及溶质的解离常数和辛醇-水分配系数等理化性质影响着膜分离过程〔41〕,通过其他技术来强化膜分离过程也是提高MA去除效率的有效手段.P. Kulkarni等〔50〕用ZVI强化砂滤过程来抵抗pH对MA的吸附影响,使得未经pH调整的再生水中的MA可被有效去除.L. Sbardella等〔51〕则通过生物活性炭滤池强化了超滤过程对MA的去除效果,使得AZI的去除率提升了32%. ...
Advanced biological activated carbon filter for removing pharmaceutically active compounds from treated wastewater
2
2018
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 膜分离技术是利用两相之间理化性质的差异达到二者分离的过程.砂滤、纳滤、超滤等膜分离技术是水环境中MA的有效去除手段.溶液的pH以及溶质的解离常数和辛醇-水分配系数等理化性质影响着膜分离过程〔41〕,通过其他技术来强化膜分离过程也是提高MA去除效率的有效手段.P. Kulkarni等〔50〕用ZVI强化砂滤过程来抵抗pH对MA的吸附影响,使得未经pH调整的再生水中的MA可被有效去除.L. Sbardella等〔51〕则通过生物活性炭滤池强化了超滤过程对MA的去除效果,使得AZI的去除率提升了32%. ...
1
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
Enhanced adsorption of ionizable antibiotics on activated carbon fiber under electrochemical assistance in continuous-flow modes
3
2018
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 四种常见的MA均有较大的辛醇-水分配系数,疏水性极强,可以利用吸附技术将MA从水相吸附到固相吸附剂上来达到去除污染物的目的.一直以来吸附剂的再生性能和吸附性能的提升是研究者主要的关注点〔42, 53, 57〕.S. T. Danalioǧlu等〔42〕合成了磁铁矿壳聚糖活性炭(MACC)用于吸附去除ERY,材料在保持高比表面积的同时也有良好的磁选回收性能.Gang Wang等〔57〕制备的多孔氮化硼-碳纳米片(BCN)吸附材料通过空气中简单的高温处理即可实现吸附剂的再生,且6次循环后仍能保持91.9%以上的吸附容量.吸附性能方面,MA的吸附过程会受到静电作用等分子间作用的影响,强化这些分子间的作用是提升材料吸附性能的有效途径〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... 〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
The impact and fate of clarithromycin in anaerobic digestion of waste activated sludge for biogas production
3
2021
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为抗菌药物有较高的生物毒性,可对生物体甚至非靶标生物的生长和代谢产生抑制作用,而生物处理技术对于MA的毒性削减可以起到积极的作用〔21, 45〕.通过生物强化或共代谢等方式筛选和富集特异性降解MA的微生物是MA生物降解的关键.Shuting Zeng等〔54〕在厌氧消化工艺中通过高质量浓度CLA(> 10 mg/L)的环境富集和筛选了可降解CLA的微生物,进而放大了生物技术对MA毒性的削减作用.H. Fakhri等〔43〕也通过在HF-MBR反应器中添加限制假单胞菌使得细菌在抗生素和生长真菌的压力下进行特异性筛选,得到可以作为群体感应抑制剂的次生代谢物,来抵抗抗生素化合物对微生物的毒害作用.另一方面,MA的毒性生物削减工艺也促进了其他污染物的共代谢.G. T. H. Ooi等〔45〕使用中试规模的MBBR对医院废水中COD和氮去除的同时,实现了包括MA类在内的22种药物的有效去除.M. Martinez-Quintela等〔44〕也通过膜生物反应器开发了基于亚硝酸盐厌氧甲烷氧化的新工艺,该工艺在去除亚硝酸盐的同时协同去除了ERY和ROX等抗生素. ...
... 大多数生物法能够利用微生物群落的代谢作用将MA去除或转化为无毒的化合物,运行成本低.然而生物工艺受外界环境的影响较大,甚至可能受到MA的抑制作用.同时,部分生物工艺中MA的浓度可能因为代谢产物的偶联或者吸附于悬浮固体上污染物的释放而发生出水浓度增大的现象〔54〕.因此,未来的研究重点应放在生物技术的强化和工艺的耦合上面,即利用强化生物工艺来有效抵抗外界干扰削减毒性的同时,通过耦合工艺提升MA的去除效率. ...
Degradation of typical macrolide antibiotic roxithromycin by hydroxyl radical: Kinetics, products, and toxicity assessment
2
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... Fenton氧化所使用的试剂溶解性铁盐和H2O2所需成本较低且不会对环境构成威胁,体系产生的·OH又可以有效提升MA的去除率,所以Fenton法和类Fenton法被认为是最有效的降解新兴污染物的高级氧化法〔62-63〕.实际废水水质复杂,对催化体系影响因素的探究成为研究的热点,多数研究表明无机离子和天然有机物(NOM)的存在会影响Fenton氧化对MA的去除.Wei Li等〔55〕通过UV/H2O2工艺对ROX的降解实验发现,无机离子和高浓度NOM会使ROX的降解率降低,这表明在实际废水中该催化体系对ROX的降解将受到强抑制.Meng Li等〔39〕的研究也发现水体中NOM和阴离子的存在会对·OH主导的非均相Fenton过程有明显的抑制效果.因此,研究者试图通过材料改性等手段减轻离子及NOM对催化氧化过程的抑制,以期实现该体系在实际废水中的有效应用.E. Serrano等〔17〕探究了改性的磁铁矿和H2O2构成的催化体系对不同污水处理厂实际污水中ERY、CLA和AZI的去除效果,结果表明,改性磁铁矿体系在实际废水催化过程中,在保持低的铁浸出与高稳定性的基础上,达到了污染物和总大肠菌群的协同清除. ...
Insight into antibiotics removal: Exploring the photocatalytic performance of a Fe3O4/ZnO nanocomposite in a novel magnetic sequential batch reactor
1
2019
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
Adsorption performance and mechanism of antibiotics from aqueous solutions on porous boron nitride-carbon nanosheets
6
2020
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... 四种常见的MA均有较大的辛醇-水分配系数,疏水性极强,可以利用吸附技术将MA从水相吸附到固相吸附剂上来达到去除污染物的目的.一直以来吸附剂的再生性能和吸附性能的提升是研究者主要的关注点〔42, 53, 57〕.S. T. Danalioǧlu等〔42〕合成了磁铁矿壳聚糖活性炭(MACC)用于吸附去除ERY,材料在保持高比表面积的同时也有良好的磁选回收性能.Gang Wang等〔57〕制备的多孔氮化硼-碳纳米片(BCN)吸附材料通过空气中简单的高温处理即可实现吸附剂的再生,且6次循环后仍能保持91.9%以上的吸附容量.吸附性能方面,MA的吸附过程会受到静电作用等分子间作用的影响,强化这些分子间的作用是提升材料吸附性能的有效途径〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... 〔57〕制备的多孔氮化硼-碳纳米片(BCN)吸附材料通过空气中简单的高温处理即可实现吸附剂的再生,且6次循环后仍能保持91.9%以上的吸附容量.吸附性能方面,MA的吸附过程会受到静电作用等分子间作用的影响,强化这些分子间的作用是提升材料吸附性能的有效途径〔42, 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... , 57〕.Sitan Wang等〔53〕以电化学辅助下的活性炭来强化抗生素的吸附去除,与单纯的活性炭吸附相比,静电作用的加强使得吸附剂的吸附容量增大了5倍,对50 mg/L的微量CLA的吸附去除率可达99.9%. ...
... 四种常见的MA结构中有多个含O或含N官能团,因而可以通过静电作用、氢键作用、π-π作用、n-π作用、孔填充效应及疏水协同作用等作用力被吸附材料吸附去除〔22, 57, 66-67〕.如在BCN对ROX的吸附中,化学吸附过程中的疏水作用和静电作用是影响材料吸附性能的重要因素〔57〕. ...
... 〔57〕. ...
Zero-valent iron enhanced in-situ advanced anaerobic digestion for the removal of antibiotics and antibiotic resistance genes in sewage sludge
2
2021
... 四种常见大环内酯类抗生素的深度去除技术
| 化合物 | | 去除技术 | 水质类型 | 进水质量浓度 | 实验条件 | 去除率/% | 参考文献 |
| ERY | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量
2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 30 | 〔38〕 |
| 过硫酸盐活化Fenton氧化 | 合成废水 | 1 mg/L | 过硫酸盐0.05 mmol/L; H2O2 0.05 mmol/L; 零价铁(ZVI)2.8 mg/L; t=4 h | 69.5 | 〔39〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm3/ min; t=1 h | 100 | 〔40〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 物化 | 低压超滤 | 合成废水 | 500 μg/L | 操作压力0.3 MPa; pH=7;t=0.5 h | 78.6 | 〔41〕 |
磁铁矿壳聚糖活性炭
(MACC)吸附 | 合成废水 | 60 mg/L | MACC 20 mg/L; t=2 h | 54 | 〔42〕 |
| 生物 | 中空纤维膜生物反应器(HF-MBR) | 合成废水 | 100 mg/L | TSS=4 630 mg/L; 外加限制青霉菌2.5 mg/L | 94.8 | 〔43〕 |
| 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| AZI | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol/(min·L); t=10 min | 100 | 〔37〕 |
| 二氧化钛光催化 | 实际废水 | 1.36 ng/L | λ=382 nm,20 W; t=3 h | 50 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| TiO2光催化 | 合成废水 | 10 mg/L | TiO2 0.005 g; 光强4.05 mW/cm2; t光=t暗=0.5 h | 98 | 〔47〕 |
| 超声化学降解 | 合成废水 | 20 mg/L | H2O2 50 mg/L; ZnO 1 g//L; t=15 min | 98.4 | 〔48〕 |
| 电化学/UV | 合成废水 | 200 μg/L | λ=254 nm; 电流密度10 mA/cm2; t=6 h | 46 | 〔49〕 |
| 物化 | ZVI砂滤 | 实际废水 | 320 ng/L | ZVI 0.98 L/L; 砂滤流速18 L/(min·m2); 孔隙率0.52 | > 90 | 〔50〕 |
| 生物活性炭超滤(BAC-UF) | 实际废水 | 480 ng/L | 空床接触时间(EBCT)50 min; 截留分子量2 000 u; 流量13 L/(m2·h) | 63 | 〔51〕 |
| 生物 | 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| 真空紫外(VUV)-化学氧化 | 合成废水 | 33 100 mg/L | λ=185 nm; 催化剂20 g; H2O2 75 mL; t=60 min | 93.2 | 〔52〕 |
| CLA | 化学氧化 | 光化学氧化 | 合成废水 | 20 mg/L | λ=580 nm; 总光子通量2 mmol(min·L); t=10 min | > 95 | 〔38〕 |
| 磁铁矿催化H2O2 | 合成废水 | 1 000 μg/L | Fe3O4 0.2 g/L; H2O2 4~6 mg/L; t=1.5 h | 100 | 〔17〕 |
| 臭氧光催化 | 实际废水 | 1 000 mg/L | λ=382 nm; O3进口质量浓度50 g/Nm3,O3流速15 Ncm/ min; ;t=1 h | 100 | 〔40〕 |
| 物化 | 电化学吸附 | 合成废水 | 50 mg/L | 活性炭阳极(3 mm厚,14 g); 活性炭阴极(1 mm厚,4.6 g); 电压-1.0 V; t=1 h | 99.9 | 〔53〕 |
| 生物 | 厌氧消化 | 合成废水 | 100 mg/L | TS=(22 287±323) mg/L; T=(35.0±1.0) ℃; SRT=20 d | 81.73 | 〔54〕 |
| 移动床生物膜反应器(MBBR) | 实际废水 | 3~20 μg/L | T=20 ℃; 填充比50%;容积900 L; HRT=1.13 h | > 20 | 〔45〕 |
| 活性污泥法 | 合成废水 | 10 mg/L | T=28 ℃; MLSS=3.5 g/L | > 99 | 〔21〕 |
| 耦合 | 生物-超声-光Fenton | 实际废水 | 101 μg/L | T=22 ℃; TSS=9.11 mg/L; 超声频率315 kHz; Fe2+ 5 mg/L; 无需外加H2O2 | 82.86 | 〔46〕 |
| ROX | 化学氧化 | UV/H2O2 | 合成废水 | 10 mg/L | λ=365 nm; H2O2 20 mmol/L; t=6 h | 100 | 〔55〕 |
| 磁性材料光催化 | 合成废水 | 100 μg/L | λ=365 nm; H2O2 100 mg/L; 磁性催化剂100 mg/L; t=6 h | 100 | 〔56〕 |
| 物化 | 多孔氮化硼-碳纳米片(BCN)吸附 | 合成废水 | 50~1 000 mg/L | 催化剂5 mg; t=1 h | > 91.9 | 〔57〕 |
| 生物 | 膜生物反应器(MBR) | 合成废水 | 1 μg/L | T=28 ℃; HRT=23.76 h; TS=0.5 g/L | 30 | 〔44〕 |
| 耦合 | ZVI-厌氧消化 | 实际废水 | 0.231~1.023 μg/L | ZVI 1 000 mg/L; TSS=(10±2) g/L; SRT=20 d | 56.58 | 〔58〕 |
3.1 物化法大环内酯类抗生素的物化去除方法主要是吸附法和膜分离技术. ...
... MA作为微量污染物,单独的处理工艺往往很难做到污染物降解和毒性削减的协同.从MA去除的有效性和出水生物毒性来考虑,耦合工艺是一种比较好的选择.E. A. Serna-Galvis等〔46〕将生物-超声/光Fenton工艺有效组合起来,利用生物工艺预处理去除糖、肽和脂类等宏量污染物,利用催化氧化体系来氧化降解医疗废水中MA药物,相比于单独的化学处理,组合工艺有很好的协同效果,药物去除率从58.82%提升至82.86%.Haidong Zhou等〔58〕则将ZVI和厌氧消化工艺耦合起来,利用ZVI作为还原剂来降低系统的氧化还原电位(ORP值),在增加系统微生物多样性的同时,驯化出适宜抗生素去除及毒性削减的特异菌群,原位强化了厌氧消化工艺对MA的去除. ...
Performance of activated carbon and bentonite for adsorption of amoxicillin from wastewater: Mechanisms, isotherms and kinetics
1
2009
... 吸附和膜分离技术对MA有着较好的去除能力,去除过程中也不会有其他的污染物出现,有着良好的应用前景〔59〕.然而这两类技术在实际工程应用中很容易受到操作条件和操作环境的影响.吸附剂的吸附效率是材料的比表面积、材料孔径等一系列变量的因变量,且吸附技术选择性较低,实际水体水质复杂,存在其他污染物与目标污染物竞争吸附位点的情况,导致材料吸附容量降低.另外,吸附材料达到饱和后的回收及脱附也是必须要解决的难点.对于膜材料,膜污染及膜材料表面通道堵塞增加了物化法的使用成本,也是抗生素水处理技术中不可忽视的问题.而且物化处理只是对MA起到了分离和富集的作用,并没有实现对污染物的降解消除,所以该法对于水环境中的MA去除仍有一定的局限性.近期,Ying Wang等〔60〕采用基于磁性杂化碳材料的多模板分子印迹聚合物对水溶液中的β-内酰胺类抗生素实现了选择性去除.Yaohui Liu等〔61〕也通过分子印迹聚合物包被木尖环境质谱法对复杂食品样品中痕量MA实现了特异性识别.在之后关于MA的物化去除研究中,应该着手于物化法对抗生素的选择性去除,提高材料的可回收性,简化实际操作条件,以期在实际的抗生素废水工程化去除中得到应用. ...
Selective and fast removal and determination of β-lactam antibiotics in aqueous solution using multiple templates imprinted polymers based on magnetic hybrid carbon material
1
2021
... 吸附和膜分离技术对MA有着较好的去除能力,去除过程中也不会有其他的污染物出现,有着良好的应用前景〔59〕.然而这两类技术在实际工程应用中很容易受到操作条件和操作环境的影响.吸附剂的吸附效率是材料的比表面积、材料孔径等一系列变量的因变量,且吸附技术选择性较低,实际水体水质复杂,存在其他污染物与目标污染物竞争吸附位点的情况,导致材料吸附容量降低.另外,吸附材料达到饱和后的回收及脱附也是必须要解决的难点.对于膜材料,膜污染及膜材料表面通道堵塞增加了物化法的使用成本,也是抗生素水处理技术中不可忽视的问题.而且物化处理只是对MA起到了分离和富集的作用,并没有实现对污染物的降解消除,所以该法对于水环境中的MA去除仍有一定的局限性.近期,Ying Wang等〔60〕采用基于磁性杂化碳材料的多模板分子印迹聚合物对水溶液中的β-内酰胺类抗生素实现了选择性去除.Yaohui Liu等〔61〕也通过分子印迹聚合物包被木尖环境质谱法对复杂食品样品中痕量MA实现了特异性识别.在之后关于MA的物化去除研究中,应该着手于物化法对抗生素的选择性去除,提高材料的可回收性,简化实际操作条件,以期在实际的抗生素废水工程化去除中得到应用. ...
Sensitive analysis of trace macrolide antibiotics in complex food samples by ambient mass spectrometry with molecularly imprinted polymer-coated wooden tips
1
2019
... 吸附和膜分离技术对MA有着较好的去除能力,去除过程中也不会有其他的污染物出现,有着良好的应用前景〔59〕.然而这两类技术在实际工程应用中很容易受到操作条件和操作环境的影响.吸附剂的吸附效率是材料的比表面积、材料孔径等一系列变量的因变量,且吸附技术选择性较低,实际水体水质复杂,存在其他污染物与目标污染物竞争吸附位点的情况,导致材料吸附容量降低.另外,吸附材料达到饱和后的回收及脱附也是必须要解决的难点.对于膜材料,膜污染及膜材料表面通道堵塞增加了物化法的使用成本,也是抗生素水处理技术中不可忽视的问题.而且物化处理只是对MA起到了分离和富集的作用,并没有实现对污染物的降解消除,所以该法对于水环境中的MA去除仍有一定的局限性.近期,Ying Wang等〔60〕采用基于磁性杂化碳材料的多模板分子印迹聚合物对水溶液中的β-内酰胺类抗生素实现了选择性去除.Yaohui Liu等〔61〕也通过分子印迹聚合物包被木尖环境质谱法对复杂食品样品中痕量MA实现了特异性识别.在之后关于MA的物化去除研究中,应该着手于物化法对抗生素的选择性去除,提高材料的可回收性,简化实际操作条件,以期在实际的抗生素废水工程化去除中得到应用. ...
A review on the occurrence of micropollutants in the aquatic environment and their fate and removal during wastewater treatment
1
2014
... Fenton氧化所使用的试剂溶解性铁盐和H2O2所需成本较低且不会对环境构成威胁,体系产生的·OH又可以有效提升MA的去除率,所以Fenton法和类Fenton法被认为是最有效的降解新兴污染物的高级氧化法〔62-63〕.实际废水水质复杂,对催化体系影响因素的探究成为研究的热点,多数研究表明无机离子和天然有机物(NOM)的存在会影响Fenton氧化对MA的去除.Wei Li等〔55〕通过UV/H2O2工艺对ROX的降解实验发现,无机离子和高浓度NOM会使ROX的降解率降低,这表明在实际废水中该催化体系对ROX的降解将受到强抑制.Meng Li等〔39〕的研究也发现水体中NOM和阴离子的存在会对·OH主导的非均相Fenton过程有明显的抑制效果.因此,研究者试图通过材料改性等手段减轻离子及NOM对催化氧化过程的抑制,以期实现该体系在实际废水中的有效应用.E. Serrano等〔17〕探究了改性的磁铁矿和H2O2构成的催化体系对不同污水处理厂实际污水中ERY、CLA和AZI的去除效果,结果表明,改性磁铁矿体系在实际废水催化过程中,在保持低的铁浸出与高稳定性的基础上,达到了污染物和总大肠菌群的协同清除. ...
Costs of the electrochemical oxidation of wastewaters: A comparison with ozonation and Fenton oxidation processes
1
2009
... Fenton氧化所使用的试剂溶解性铁盐和H2O2所需成本较低且不会对环境构成威胁,体系产生的·OH又可以有效提升MA的去除率,所以Fenton法和类Fenton法被认为是最有效的降解新兴污染物的高级氧化法〔62-63〕.实际废水水质复杂,对催化体系影响因素的探究成为研究的热点,多数研究表明无机离子和天然有机物(NOM)的存在会影响Fenton氧化对MA的去除.Wei Li等〔55〕通过UV/H2O2工艺对ROX的降解实验发现,无机离子和高浓度NOM会使ROX的降解率降低,这表明在实际废水中该催化体系对ROX的降解将受到强抑制.Meng Li等〔39〕的研究也发现水体中NOM和阴离子的存在会对·OH主导的非均相Fenton过程有明显的抑制效果.因此,研究者试图通过材料改性等手段减轻离子及NOM对催化氧化过程的抑制,以期实现该体系在实际废水中的有效应用.E. Serrano等〔17〕探究了改性的磁铁矿和H2O2构成的催化体系对不同污水处理厂实际污水中ERY、CLA和AZI的去除效果,结果表明,改性磁铁矿体系在实际废水催化过程中,在保持低的铁浸出与高稳定性的基础上,达到了污染物和总大肠菌群的协同清除. ...
Peroxymonosulfate activation by nitrogen-doped biochar from sawdust for the efficient degradation of organic pollutants
1
2020
... 化学氧化法对于MA有着很好的去除效果,但是在实际的应用过程中会受到NOM和各种阴离子的抑制,影响其去除能力,并且化学药剂的使用也会增加工艺运行的成本.Lu Xu等〔64〕通过低成本的木屑制备了生物炭基g-C3N4催化剂,来活化过氧单硫酸盐(PMS)高效去除污水中的磺胺甲恶唑.另外,Fei Chen等〔65〕利用Fe/O共掺g-C3N4催化剂实现了对四环素等七种芳环抗生素选择性高效去除,为未来低成本、高活性、高选择性去除MA的化学催化技术的发展提供了新的思路. ...
Efficient decontamination of organic pollutants under high salinity conditions by a nonradical peroxymonosulfate activation system
1
2021
... 化学氧化法对于MA有着很好的去除效果,但是在实际的应用过程中会受到NOM和各种阴离子的抑制,影响其去除能力,并且化学药剂的使用也会增加工艺运行的成本.Lu Xu等〔64〕通过低成本的木屑制备了生物炭基g-C3N4催化剂,来活化过氧单硫酸盐(PMS)高效去除污水中的磺胺甲恶唑.另外,Fei Chen等〔65〕利用Fe/O共掺g-C3N4催化剂实现了对四环素等七种芳环抗生素选择性高效去除,为未来低成本、高活性、高选择性去除MA的化学催化技术的发展提供了新的思路. ...
3D assembly based on 2D structure of cellulose nanofibril/graphene oxide hybrid aerogel for adsorptive removal of antibiotics in water
1
2017
... 四种常见的MA结构中有多个含O或含N官能团,因而可以通过静电作用、氢键作用、π-π作用、n-π作用、孔填充效应及疏水协同作用等作用力被吸附材料吸附去除〔22, 57, 66-67〕.如在BCN对ROX的吸附中,化学吸附过程中的疏水作用和静电作用是影响材料吸附性能的重要因素〔57〕. ...
3D hierarchical porousstructured biochar aerogel for rapid and efficient phenicol antibiotics removal from water
1
2019
... 四种常见的MA结构中有多个含O或含N官能团,因而可以通过静电作用、氢键作用、π-π作用、n-π作用、孔填充效应及疏水协同作用等作用力被吸附材料吸附去除〔22, 57, 66-67〕.如在BCN对ROX的吸附中,化学吸附过程中的疏水作用和静电作用是影响材料吸附性能的重要因素〔57〕. ...
TiO2 assisted photocatalytic degradation of macrolide antibiotics
1
2017
... ERY、ROX和CLA有着相似的分子结构,因而其氧化降解机理类似〔47〕.图 1所示为化学氧化过程中·OH对MA分子的可能进攻位点〔68〕.在·OH主导的MA化学氧化过程中,·OH亲电攻击MA上的l-枝糖取代基,使得MA羟基化或羟基取代基被氧化,进而生成一系列羟基化产物、甲基化产物、羟甲基化产物、无机物和小分子物质.以红霉素的降解为例,冯奇奇〔69〕在研究光催化下ERY的降解机理时发现在·OH的攻击下ERY有三条降解途径.其一是·OH的攻击脱下了ERY上的去氧氨糖、克拉定糖和内酯环,之后中间产物继续被攻击开环而变成分子质量更小的物质;其二是ERY分子首先脱甲基成m/z=719的中间产物,该中间产物继续在脱甲基、脱氨、脱水、开环和羟基取代作用下生成一系列小分子物质;其三是ERY直接开环,进而继续逐步降解为小分子物质. ...
1
... ERY、ROX和CLA有着相似的分子结构,因而其氧化降解机理类似〔47〕.图 1所示为化学氧化过程中·OH对MA分子的可能进攻位点〔68〕.在·OH主导的MA化学氧化过程中,·OH亲电攻击MA上的l-枝糖取代基,使得MA羟基化或羟基取代基被氧化,进而生成一系列羟基化产物、甲基化产物、羟甲基化产物、无机物和小分子物质.以红霉素的降解为例,冯奇奇〔69〕在研究光催化下ERY的降解机理时发现在·OH的攻击下ERY有三条降解途径.其一是·OH的攻击脱下了ERY上的去氧氨糖、克拉定糖和内酯环,之后中间产物继续被攻击开环而变成分子质量更小的物质;其二是ERY分子首先脱甲基成m/z=719的中间产物,该中间产物继续在脱甲基、脱氨、脱水、开环和羟基取代作用下生成一系列小分子物质;其三是ERY直接开环,进而继续逐步降解为小分子物质. ...
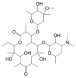
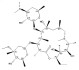
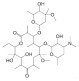
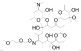



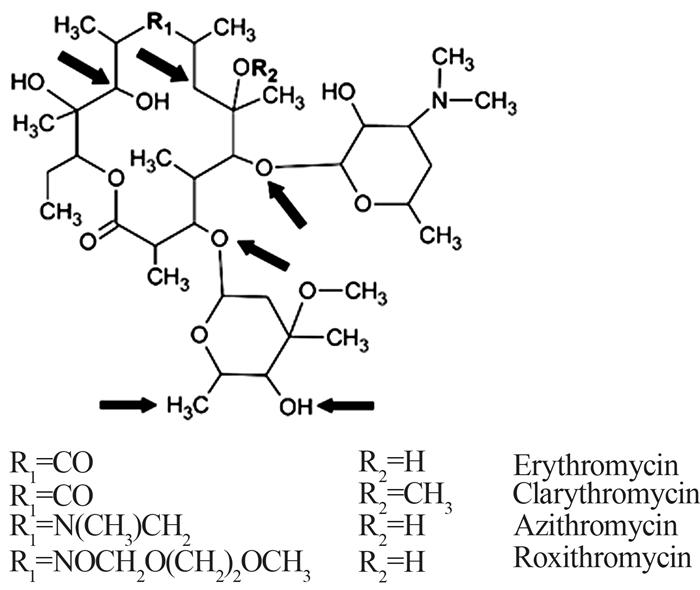
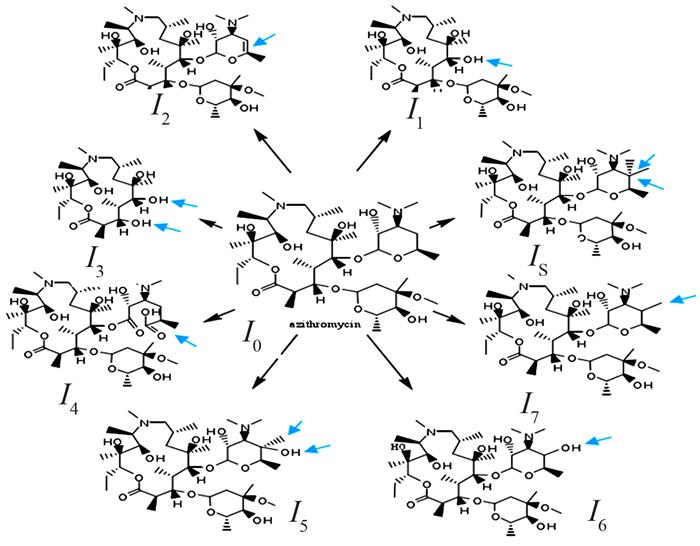


 津公网安备 12010602120337号
津公网安备 12010602120337号