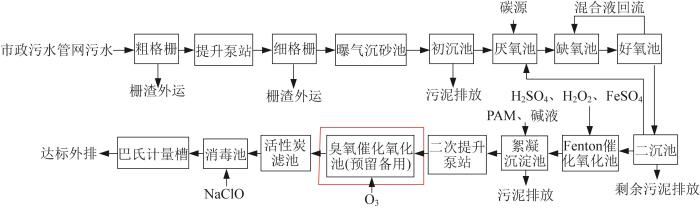
图1
表1 设计进出水水质
Table 1
| 项目 | COD | BOD5 | SS | TN | NH3-N | TP | pH |
|---|---|---|---|---|---|---|---|
| 进水 | ≤500 | ≤150 | ≤300 | ≤60 | ≤30 | ≤4.0 | 6.0~9.0 |
| 出水 | ≤30 | ≤10 | ≤10 | ≤15 | ≤1.5 | ≤1.5 | 6.0~9.0 |
催化臭氧氧化技术具有分解效率高、对污染物氧化彻底、二次污染少、操作简单等优点,引起广泛关注〔1-2〕。其基本原理是利用固态金属、金属氧化物或负载在载体上的金属或金属氧化物促进反应体系中臭氧分解,产生强氧化性的超氧自由基(O2·-)、羟基自由基(‧OH)等降解废水中的有机污染物〔3-4〕。S. I. ICHIKAWA等〔5〕采用催化臭氧氧化反应降解水中的氨氮,考察NiO、ZnO、Co3O4、Fe2O3、SnO2、Mn3O4、CuO、MgO和Al2O3等为催化剂时氨氮的去除效果,结果表明Co3O4对氨氮的去除效率最高,最终产物以氮气为主,有部分硝氮。可见,选择合适的金属氧化物为催化剂,催化臭氧氧化技术能在去除有机污染物的同时,将水中的氨氮氧化为氮气或转化为硝氮。
笔者采用专属催化剂代替污水处理厂催化臭氧氧化池中现有催化剂(活性组分为氧化铁),同时去除COD和氨氮。为证实方案的可行性,以絮凝沉淀出水为催化臭氧工艺进水,进行小试及中试。并对臭氧投加量、催化剂用量、接触反应时间等工艺参数进行优化,为项目运行提供技术参数。
1 材料与方法
1.1 废水水质
实验用水取自污水处理厂絮凝沉淀出水,其水质见表2。
表2 絮凝沉淀出水水质
Table 2
| 项目 | COD | pH | TN | NH3-N | 硝氮 |
|---|---|---|---|---|---|
| 范围 | 30.5~39.8 | 7.8~8.1 | 9.11~12.28 | 1.24~2.37 | 6.25~8.81 |
| 均值 | 37.2 | 8.0 | 10.54 | 2.01 | 7.25 |
1.2 实验装置与方法
1.2.1 小试方法
催化臭氧氧化装置模拟催化氧化塔,主体材料由有机玻璃制成。一定体积废水由顶部进水口注入,同时臭氧从底部进气口进入反应器,经曝气头布气后与废水充分混合,曝气头材质为钛合金。尾气通过顶部出气口进入尾气吸收装置。用自行研制的DL-002和DL-004铝基催化剂分别进行催化臭氧氧化小试实验。催化剂参考文献〔6〕采用浸渍法制备。实验所用催化剂参数如表3所示。反应条件:催化剂投加体积1 L,水量2 L,间歇式,臭氧发生器产量4.84 g/h,O3质量浓度57.6 g/m3,气量1.4 L/min。每隔15 min从中部取样口取水样,分别测定COD、氨氮,考察催化臭氧工艺的可行性,并筛选适合处理此类废水的催化剂。重复实验3次,计算平均值。
表3 催化剂参数 (Catalyst Index)
Table 3
| 项目 | DL-002 | DL-004 |
|---|---|---|
| 粒径/mm | 3~5 | 3~5 |
| 基材 | 氧化铝 | 氧化铝 |
| 抗压强度/N | ≥100 | ≥100 |
| 比表面积/(m2·g-1) | ≥230 | ≥230 |
| 堆密度/(g·cm-3) | 0.68~0.72 | 0.68~0.72 |
| 磨耗率/% | ≤1 | ≤1 |
| 吸水率/% | ≥30 | ≥30 |
| 活性组分 | 锰、钴的金属氧化物 | 锰、铈的金属氧化物 |
1.2.2 中试方法
中试催化臭氧氧化反应塔主体材料由SUS-316L不锈钢制成,塔高6.7 m,支撑半径2 m,空塔容积190 L,有效水深6 m。塔体顶部法兰可装填催化剂,催化剂填充体积为120 L(此时水力停留时间与接触反应时间相同)。催化臭氧氧化装置从下到上共分为4个部分,分别是反应器基座、气水混合层、催化氧化层、气水分离层。废水由自吸泵从底部进水口注入,同时臭氧从底部进气口进入反应器与废水充分混合,之后依次通过气水混合层、催化氧化层、气水分离层,尾气由尾气破坏装置处理后排放。工业用液氧钢瓶为氧气源,氧气经臭氧发生器后接入反应塔进气口。CF-G-2-50g臭氧发生器(青岛国林科技有限公司),额定功率为0.5 kW,最高产量50 g/h,臭氧质量浓度为80~120 g/m3。连续进水,稳定后间隔取水样,分别测定COD、氨氮等。通过改变进水量、臭氧投加量来优化工艺参数。
1.3 分析方法
pH采用玻璃电极法(GB/T 6920—1986)测定;COD采用重铬酸盐法(HJ 828—2017)测定;氨氮采用纳氏试剂分光光度法(HJ 535—2009)测定;硝氮 采用紫外分光光度法(HJ/T 346—2007)测定;总氮采用碱性过硫酸钾消解紫外分光光度法(HJ 636—2012)测定。
2 结果与讨论
2.1 小试结果
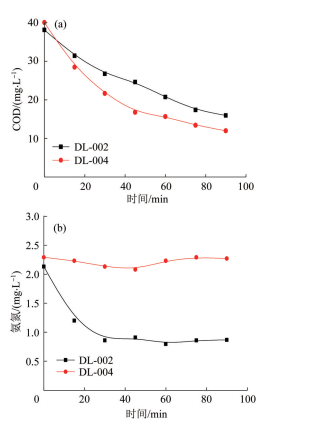
以絮凝沉淀池出水为原水,DL-002、DL-004为催化剂进行催化臭氧氧化小试。COD和氨氮的变化情况见图2。
图2
由图2可见,对于DL-002催化剂,催化反应30 min,COD由37.5 mg/L 降低至26.3 mg/L,可以满足当地对出水COD(≤30 mg/L)的要求,继续延长反应时间,COD继续降低,但变化幅度明显减缓。催化反应15 min后,氨氮由2.13 mg/L降为1.20 mg/L,可以满足要求(该污水处理厂出水NH3-N需≤1.5 mg/L),随着反应时间的进一步延长,出水氨氮在0.8 mg/L左右波动,不再继续降低。采用DL-004催化剂时,COD去除效果更佳,催化反应15 min时出水COD为28 mg/L,可满足出水COD≤30 mg/L的要求。但DL-004催化剂对氨氮完全没有去除,反应90 min出水氨氮几乎没有变化,无法达到出水要求。这表明DL-004催化剂仅能去除COD,对氨氮的去除或转化没有任何帮助。结合文献分析,臭氧分子在锰、钴氧化物表面的Lewis、Bronsted酸位催化生成活性较高的单原子氧,并在水溶液中经过一系列反应生成羟基自由基、超氧自由基、单线态氧等氧化能力强的活性含氧物质,将氨氮氧化为硝氮、亚硝氮和部分氮气〔7-8〕。反应机理见式(
锰、铈氧化物的反应活性比较弱,不足以与氨氮发生反应。因此,在后续中试中选用DL-002催化剂。
2.2 催化臭氧氧化法处理中试结果
2.2.1 工艺参数优化
表4 实验因素水平
Table 4
| 因素 | 水平 | ||||
|---|---|---|---|---|---|
| -1.414 | -1 | 0 | 1 | 1.414 | |
| A/min | 18.96 | 20 | 22.5 | 25 | 26.04 |
| B/(mg·L-1) | 18.34 | 20.0 | 24.0 | 28.0 | 29.66 |
表5 中心组合设计方案与结果
Table 5
| 序号 | 接触反应时间/min | 臭氧投加量/(mg·L-1) | COD去除量/(mg·L-1) | 氨氮去除量/(mg·L-1) |
|---|---|---|---|---|
| 1 | 26.04 | 24.00 | 10.5 | 0.65 |
| 2 | 18.96 | 24.00 | 9.75 | 0.58 |
| 3 | 22.50 | 24.00 | 9.60 | 0.57 |
| 4 | 20.00 | 20.00 | 9.00 | 0.39 |
| 5 | 22.50 | 24.00 | 9.60 | 0.57 |
| 6 | 20.00 | 28.00 | 10.6 | 0.68 |
| 7 | 25.00 | 28.00 | 10.8 | 0.71 |
| 8 | 22.50 | 24.00 | 9.60 | 0.62 |
| 9 | 22.50 | 24.00 | 9.60 | 0.57 |
| 10 | 22.50 | 24.00 | 9.60 | 0.57 |
| 11 | 25.00 | 20.00 | 9.85 | 0.49 |
| 12 | 22.50 | 18.34 | 8.84 | 0.41 |
| 13 | 22.50 | 29.66 | 11.5 | 0.75 |
采用Design-Expert 软件对所得数据进行回归分析,得到COD和氨氮去除量的二次多元回归模型,用以分析多个自变量和响应值变化关系:
表6 COD去除量响应面回归分析结果
Table 6
| 方差来源 | 平方和 | 自由度 | 均方差 | F值 | P值 |
|---|---|---|---|---|---|
| 模型 | 6.43 | 5 | 1.29 | 45.45 | < 0.000 1 |
| A(接触反应时间) | 0.56 | 1 | 0.56 | 19.68 | 0.003 0 |
| B(臭氧的投加量) | 4.98 | 1 | 4.98 | 176.03 | < 0.000 1 |
| AB | 0.11 | 1 | 0.11 | 3.73 | 0.094 6 |
| A2 | 0.40 | 1 | 0.40 | 14.31 | 0.006 9 |
| B2 | 0.48 | 1 | 0.48 | 17.11 | 0.004 4 |
| 残差 | 0.20 | 7 | 0.028 | ||
| 失拟项 | 0.20 | 3 | 0.066 | ||
| 纯误差 | 0.000 | 4 | 0.000 | ||
| R2 | 0.970 1 | ||||
| R | 0.948 8 | ||||
| R | 0.787 5 | ||||
表7 氨氮去除量响应面回归分析结果
Table 7
| 方差来源 | 平方和 | 自由度 | 均方差 | F值 | P值 |
|---|---|---|---|---|---|
| 模型 | 0.13 | 5 | 0.026 | 45.81 | <0.000 1 |
| A(接触反应时间) | 6.555×10-3 | 1 | 6.555×10-3 | 11.40 | 0.011 8 |
| B(臭氧的投加量) | 0.12 | 1 | 0.12 | 213.34 | <0.000 1 |
| AB | 1.225×10-3 | 1 | 1.225×10-3 | 2.13 | 0.187 8 |
| A2 | 6.957×10-4 | 1 | 6.957×10-4 | 1.21 | 0.307 8 |
| B2 | 3.913×10-4 | 1 | 3.913×10-4 | 0.68 | 0.436 7 |
| 残差 | 4.027×10-3 | 7 | 5.752×10-4 | ||
| 失拟项 | 2.027×10-3 | 3 | 6.755×10-4 | 1.35 | 0.376 9 |
| 纯误差 | 2.000×10-3 | 4 | 5.000×10-4 | ||
| R2 | 0.970 3 | ||||
| R | 0.942 9 | ||||
| R | 0.870 8 | ||||
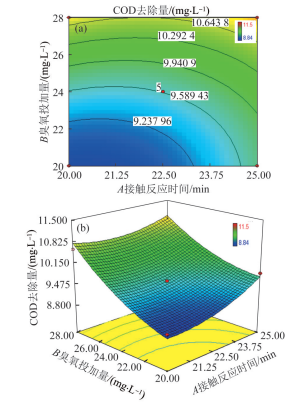
图3
图3
臭氧投加量和接触反应时间对COD去除量的影响
Fig. 3
Effect of ozone dosage and contact reaction time on COD removal
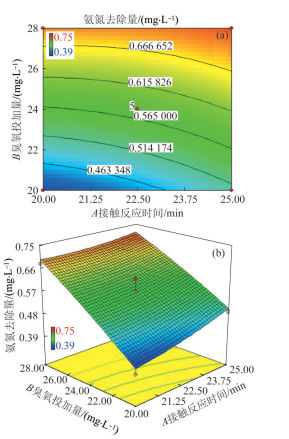
图4
图4
臭氧投加量和接触反应时间对氨氮去除量的影响
Fig. 4
Effect of ozone dosage and contact reaction time on ammonia nitrogen removal
用Design-Expert 软件的优化功能,在设定各影响因素的约束条件下,得出COD去除量为10 mg/L、氨氮去除量为0.65 mg/L时,最佳工艺条件为:接触反应时间20 min,臭氧投加量25 mg/L,在此条件下进行了后续实验。
2.2.2 最佳反应条件下的运行效果
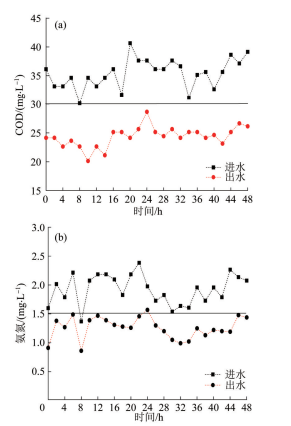
为验证响应曲面分析确定的最佳工艺参数,在接触反应时间为20 min,臭氧投加量为25 mg/L条件下进行48 h连续实验,每隔2 h取样分析COD和氨氮,结果见图5。
图5
由图5可知,进水COD在30~40 mg/L、氨氮在1.45~2.5 mg/L范围内波动时,可以保证出水COD<30 mg/L、氨氮<1.5 mg/L的设计出水要求,预测结果与实验结果之间具有良好的一致性,验证了模型的有效性。
2.2.3 现有项目改造方案
根据中试结果,确定催化臭氧工艺工程设计参数:臭氧投加量25 mg/L,进水COD 38 mg/L,出水COD≤30 mg/L,进水氨氮2.0 mg/L,出水氨氮≤1.5 mg/L,处理水量为20 000 m3/d,反应停留时间为20 min,DL-002催化剂用量为278 m3。
采用真空变压吸附(VPSA)制氧+臭氧发生器形式,单位质量O3运行功耗为11 kW·h/kg,运行费用为11 kW·h/kg×电费〔0.65元/(kW·h)〕×每吨水消耗的臭氧量,得到吨水运行费用0.179元。
3 结论
(1)小试结果表明DL-002催化剂具有催化臭氧氧化同时去除COD和氨氮的性能。
(2)基于中心组合设计的响应面法建立了以COD和氨氮去除量为响应值的二次响应曲面模型,方差分析结果显示这种拟合方法是可靠的,能够很好地描述实验结果。
(3)臭氧投加量对COD和氨氮去除量有更显著的影响,增加臭氧投加量或延长接触反应时间可以提高COD和氨氮去除量。
(4)在接触反应时间为20 min,臭氧投加量为25 mg/L条件下,COD去除量为10 mg/L、氨氮去除量为0.65 mg/L。
参考文献
催化臭氧氧化深度处理工业废水的研究及应用
[J].
Research on catalytic ozonation and its application to the advanced treatment of industrial wastewater
[J].
难降解石油化工废水臭氧氧化处理催化剂研究进展
[J].
An overview of catalysts in ozonation treatment of refractory petrochemical wastewaters
[J].
Catalytic ozonation and methods of enhancing molecular ozone reactions in water treatment
[J].
Preparation and structural characterization of Co/Al2O3 catalysts for the ozonation of pyruvic acid
[J].
Catalytic oxidation of ammonium ion in water with ozone over metal oxide catalysts
[J].
铝基催化剂制备、臭氧氧化有机物和氨氮性能与应用研究
[D].
Preparation,properity and application of alumina-supported catalyst by ozonation process for degradation of organic compounds and ammonia nitrogen
[D].
Ozonation of ammonia in wastewater
[J].
Catalytic ozonation of trace nitrobenzene in water with synthetic goethite
[J].
响应面法在生物过程优化中的应用
[J].
Application of response surface method on biological process optimization
[J].





 津公网安备 12010602120337号
津公网安备 12010602120337号