1
2005
... 重金属因其高毒性、易富集、难以生物降解等特点,严重威胁环境安全和公众健康,重金属污染的治理是全球普遍面临的难题.目前,我国重金属废水不适当和不充分的处理现象非常普遍,使得水体重金属污染十分严重〔1〕.水体中的重金属难以降解,通过大自然的物质循环后,污染物会富集在土壤和生物体内,隐蔽在大自然的各个角落〔2〕.废水中的镉、汞、铅、砷、镍等重金属在水体中不断富集,严重危害了水体环境,较为典型的就是含有大量重金属的工业废水的违规排放,导致了“癌症村”的频繁涌现.这样的事件频繁发生,极大损害了广大人民群众的生命安全.因此,如何去除水体中的重金属引起了人们极大地重视与关注. ...
Physico-chemical treatment techniques for wastewater laden with heavy metals
1
2006
... 重金属因其高毒性、易富集、难以生物降解等特点,严重威胁环境安全和公众健康,重金属污染的治理是全球普遍面临的难题.目前,我国重金属废水不适当和不充分的处理现象非常普遍,使得水体重金属污染十分严重〔1〕.水体中的重金属难以降解,通过大自然的物质循环后,污染物会富集在土壤和生物体内,隐蔽在大自然的各个角落〔2〕.废水中的镉、汞、铅、砷、镍等重金属在水体中不断富集,严重危害了水体环境,较为典型的就是含有大量重金属的工业废水的违规排放,导致了“癌症村”的频繁涌现.这样的事件频繁发生,极大损害了广大人民群众的生命安全.因此,如何去除水体中的重金属引起了人们极大地重视与关注. ...
废水中的重金属处理方法分析
1
2019
... 重金属零排放背景下,传统物化法净化低浓度重金属废水存在低效、不经济和二次污染等问题,如何高效经济地净化大量低浓度重金属废水已成为涉重环保行业的难点.目前,我国重金属废水不适当和不充分的处理现象非常普遍,严重威胁环境安全和公众健康.重金属废水处理方法的选择及有效性,同废水中重金属离子的含量及赋存形态关系紧密.在中高浓度范围,传统能源密集型物理化学方法通常表现出较高的处理效率和经济性,如中和、化学沉淀、混凝、化学还原、电解和电絮凝等.但对于低质量浓度(小于1~100 mg/L)这些方法往往非常低效甚至失效,或者表现出不经济性〔3〕.膜过滤、离子交换法和吸附法等高新技术虽对低浓度重金属废水处理有效,但对于大量低浓度重金属废水处理,均存在容量有限、再生频繁和运行成本高等不足,应用受到极大限制.然而,工矿企业排放的重金属废水大多为中低浓度范畴且水量巨大,如酸性矿山废水、浮选废水和电镀废水等.因此,为应对持续增加的重金属威胁,重金属废水零排放需求迫切,需要发展既对低浓度重金属有较高的去除效率,又能适应较大水量的净化方法. ...
废水中的重金属处理方法分析
1
2019
... 重金属零排放背景下,传统物化法净化低浓度重金属废水存在低效、不经济和二次污染等问题,如何高效经济地净化大量低浓度重金属废水已成为涉重环保行业的难点.目前,我国重金属废水不适当和不充分的处理现象非常普遍,严重威胁环境安全和公众健康.重金属废水处理方法的选择及有效性,同废水中重金属离子的含量及赋存形态关系紧密.在中高浓度范围,传统能源密集型物理化学方法通常表现出较高的处理效率和经济性,如中和、化学沉淀、混凝、化学还原、电解和电絮凝等.但对于低质量浓度(小于1~100 mg/L)这些方法往往非常低效甚至失效,或者表现出不经济性〔3〕.膜过滤、离子交换法和吸附法等高新技术虽对低浓度重金属废水处理有效,但对于大量低浓度重金属废水处理,均存在容量有限、再生频繁和运行成本高等不足,应用受到极大限制.然而,工矿企业排放的重金属废水大多为中低浓度范畴且水量巨大,如酸性矿山废水、浮选废水和电镀废水等.因此,为应对持续增加的重金属威胁,重金属废水零排放需求迫切,需要发展既对低浓度重金属有较高的去除效率,又能适应较大水量的净化方法. ...
Electrochemically assisted microbial production of hydrogen from acetate
2
2005
... 微生物电解池(MECs)有机集成了电化学与微生物氧化还原等特点,为低浓度重金属经济净化回收提供了当代解决思路.MECs在2005年被研究团队发现,是基于微生物燃料电池(microbial fuel cells,MFCs)发展而来的〔4〕.该技术在生物产电、海水淡化、产氢、有机污染物降解、重金属还原以及与其他工艺耦合方面具有巨大潜力,近几年来,研究人员在以上方面取得了诸多成果〔5〕.但目前MECs去除废水重金属的研究进展和总结较少,其相关的性能特征与去除机制也未见整理与报道.因此,笔者通过总结基于MECs技术处理重金属废水的研究进展,概括其影响因素,总结MECs去除废水中重金属的性能特征与去除机制,辨别其存在的不足及研究方向,以期对MECs去除废水重金属离子应用的未来研究与推广提供参考. ...
... MECs反应器构型主要分为两类:单室型和双室型(如图1所示).因MECs衍生于MFCs,其早期研究反应器的构型多为双室结构〔4〕,双室反应器的阴阳两极之间用隔膜隔开,这样有效避免了阴极产物被阳极产电微生物利用,可以生成更为纯净的产物,同时也增强了阴极材料的稳定性和使用寿命.但因隔膜的存在,双室MECs不可避免地产生了一些问题:(1)隔膜的存在使得阴阳两极的间距较大,增大了内阻,降低了反应效率;(2)随着反应的进行,隔膜的存在使得质子扩散受到阻碍,容易增大阴阳两极的pH梯度,进而降低了阳极微生物的生物丰度与活性;(3)质子交换膜的价格高昂,增大了反应器的成本,也限制了双室反应器的放大.基于上述不足,研究人员开发了单室无膜MECs反应器〔8〕.单室结构中,取消了隔膜之后,阴阳两极间的距离进一步缩小,反应器的传质阻力大大降低,获得了比双室MECs更高的电流密度,使反应效率得到大幅提高.此外,没有了隔膜的存在,单室的设计也更加简单,便于构建,减少了装置的投资成本,为MECs的放大与工程化运用提供了方便. ...
微生物电解池应用研究进展
1
2017
... 微生物电解池(MECs)有机集成了电化学与微生物氧化还原等特点,为低浓度重金属经济净化回收提供了当代解决思路.MECs在2005年被研究团队发现,是基于微生物燃料电池(microbial fuel cells,MFCs)发展而来的〔4〕.该技术在生物产电、海水淡化、产氢、有机污染物降解、重金属还原以及与其他工艺耦合方面具有巨大潜力,近几年来,研究人员在以上方面取得了诸多成果〔5〕.但目前MECs去除废水重金属的研究进展和总结较少,其相关的性能特征与去除机制也未见整理与报道.因此,笔者通过总结基于MECs技术处理重金属废水的研究进展,概括其影响因素,总结MECs去除废水中重金属的性能特征与去除机制,辨别其存在的不足及研究方向,以期对MECs去除废水重金属离子应用的未来研究与推广提供参考. ...
微生物电解池应用研究进展
1
2017
... 微生物电解池(MECs)有机集成了电化学与微生物氧化还原等特点,为低浓度重金属经济净化回收提供了当代解决思路.MECs在2005年被研究团队发现,是基于微生物燃料电池(microbial fuel cells,MFCs)发展而来的〔4〕.该技术在生物产电、海水淡化、产氢、有机污染物降解、重金属还原以及与其他工艺耦合方面具有巨大潜力,近几年来,研究人员在以上方面取得了诸多成果〔5〕.但目前MECs去除废水重金属的研究进展和总结较少,其相关的性能特征与去除机制也未见整理与报道.因此,笔者通过总结基于MECs技术处理重金属废水的研究进展,概括其影响因素,总结MECs去除废水中重金属的性能特征与去除机制,辨别其存在的不足及研究方向,以期对MECs去除废水重金属离子应用的未来研究与推广提供参考. ...
微生物电解池制氢技术研究进展
1
2015
... MECs自2005年被研究发现以来,在有机物污染处理、产能及重金属还原回收方面显示出巨大的开发潜力,为解决当下重金属污染和回收金属资源提供了新的处理方法,MECs原理见图1〔6〕.在阳极室中,废水中的有机质被阳极微生物氧化生成质子、电子、二氧化碳,电子在辅助电压的驱动下,从微生物转移到阳极,再经外电路到达阴极;质子则传递到阴极与电子结合发生催化作用,结合生成氢气〔7〕. ...
微生物电解池制氢技术研究进展
1
2015
... MECs自2005年被研究发现以来,在有机物污染处理、产能及重金属还原回收方面显示出巨大的开发潜力,为解决当下重金属污染和回收金属资源提供了新的处理方法,MECs原理见图1〔6〕.在阳极室中,废水中的有机质被阳极微生物氧化生成质子、电子、二氧化碳,电子在辅助电压的驱动下,从微生物转移到阳极,再经外电路到达阴极;质子则传递到阴极与电子结合发生催化作用,结合生成氢气〔7〕. ...
Hydrogen gas production in a microbial electrolysis cell by electrohydrogenesis
1
2010
... MECs自2005年被研究发现以来,在有机物污染处理、产能及重金属还原回收方面显示出巨大的开发潜力,为解决当下重金属污染和回收金属资源提供了新的处理方法,MECs原理见图1〔6〕.在阳极室中,废水中的有机质被阳极微生物氧化生成质子、电子、二氧化碳,电子在辅助电压的驱动下,从微生物转移到阳极,再经外电路到达阴极;质子则传递到阴极与电子结合发生催化作用,结合生成氢气〔7〕. ...
Hydrogen production in a single chamber microbial electrolysis cell lacking a membrane
1
2008
... MECs反应器构型主要分为两类:单室型和双室型(如图1所示).因MECs衍生于MFCs,其早期研究反应器的构型多为双室结构〔4〕,双室反应器的阴阳两极之间用隔膜隔开,这样有效避免了阴极产物被阳极产电微生物利用,可以生成更为纯净的产物,同时也增强了阴极材料的稳定性和使用寿命.但因隔膜的存在,双室MECs不可避免地产生了一些问题:(1)隔膜的存在使得阴阳两极的间距较大,增大了内阻,降低了反应效率;(2)随着反应的进行,隔膜的存在使得质子扩散受到阻碍,容易增大阴阳两极的pH梯度,进而降低了阳极微生物的生物丰度与活性;(3)质子交换膜的价格高昂,增大了反应器的成本,也限制了双室反应器的放大.基于上述不足,研究人员开发了单室无膜MECs反应器〔8〕.单室结构中,取消了隔膜之后,阴阳两极间的距离进一步缩小,反应器的传质阻力大大降低,获得了比双室MECs更高的电流密度,使反应效率得到大幅提高.此外,没有了隔膜的存在,单室的设计也更加简单,便于构建,减少了装置的投资成本,为MECs的放大与工程化运用提供了方便. ...
Microbial fuel cells to recover heavy metals
3
2014
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
... 〔9〕. ...
Enhanced removal of copper by electroflocculation and electroreduction in a novel bioelectrochemical system assisted microelectrolysis
0
2020
Copper reduction in a pilot-scale membrane-free bioelectrochemical reactor
1
2011
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
The modeling of gold recovery from tetrachloroaurate wastewater using a microbial fuel cell
2
2013
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
Recovery of silver from wastewater coupled with power generation using a microbial fuel cell
2
2012
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
Microbial electrolysis cells turning to be versatile technology:Recent advances and future challenges
3
2014
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
Enhanced Cd(Ⅱ) removal with simultaneous hydrogen production in biocathode microbial electrolysis cells in the presence of acetate or NaHCO3
2
2016
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
... 〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Performance of Pb(Ⅱ) reduction on different cathodes of microbial electrolysis cell driven by Cr(Ⅵ)-reduced microbial fuel cell
0
2019
Metals removal and recovery in bioelectrochemical systems:A review
3
2015
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
A comprehensive review of microbial electrochemical systems as a platform technology
3
2013
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... 与传统电化学方法类似,Pd、Au、Pt等贵金属,过渡金属及氧化物和石墨烯/碳纳米管碳基等化学催化剂常被选用与研究催化阴极反应,在催化氧气、硝酸盐、金属离子还原和制氢等方面效果比较显著〔18,24〕.但在环境污染修复应用中,上述化学催化剂其复杂的制备程序、高昂的价格以及复杂环境介质中容易坍塌与中毒,导致催化性能不可逆地下降,在很大程度上成为了制约MECs在实际重金属废水处理中推广应用的重要壁垒.因此,开发容易再生、成本低廉并具有较好催化性能的阴极催化材料对推动MECs的环境应用显得十分重要.不锈钢网以其价格低廉、性能稳定脱颖而出〔32〕,在强化不锈钢网的催化性能时,研究人员发现,网状结构不锈钢的电化学活性表面积是平面结构不锈钢的3倍以上,前者具有更优的催化活性〔33〕.之后研究者又对不锈钢网表面结构进行了改进,将鬃毛刷子插入不锈钢网中制成了比表面积更大的不锈钢网刷,进一步减少了MECs体系的能耗,提高了反应效能〔34〕. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Self-sustained reduction of multiple metals in a microbial fuel cell-microbial electrolysis cell hybrid system
0
2015
Bioelectrochemical recovery of Cu,Pb,Cd,and Zn from dilute solutions
5
2012
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... 〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Complete cobalt recovery from lithium cobalt oxide in self-driven microbial fuel cell-Microbial electrolysis cell systems
3
2014
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
... (1)离子浓度.离子浓度的大小关系着微生物的活性和重金属还原效率,因此离子浓度的大小是影响MECs净化重金属效能的影响因素之一.众所周知,重金属具有很高的生物毒性,会降低微生物的生物活性,且各种微生物对重金属的耐受能力都有一定的限度.因此,重金属浓度过大会使微生物的活性降低,甚至失活,而重金属浓度过低,却可能会达不到最佳的重金属去除效率.有研究表明〔49〕,在0.7 V、初始pH=6.0的条件下,重金属离子去除率随着离子浓度的增加,先在波动中略有上升而后逐渐降低.在达到耐受质量浓度之前(5~12.5 mg/L),去除率在66.5%~70.6%之间波动,波动小且较为稳定,但达到耐受质量浓度(12.5 mg/L)之后,去除率明显降低,说明不断累积的重金属使得微生物的活性降低,以致其还原沉积的效率低下.对于其他的金属离子如Co(Ⅲ)〔21,50〕、Hg(Ⅱ)〔51〕等也有相似的结论.由此而言,控制离子浓度的高低对净化重金属的效能及效率具有重要意义. ...
Recovery of flakey cobalt from aqueous Co(Ⅱ) with simultaneous hydrogen production in microbial electrolysis cells
4
2014
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Removal of heavy metals from fly ash leachate using combined bioelectrochemical systems and electrolysis
1
2014
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
Assessment of cathode materials for Ni(Ⅱ) reduction in microbial electrolysis cells
3
2016
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
... 与传统电化学方法类似,Pd、Au、Pt等贵金属,过渡金属及氧化物和石墨烯/碳纳米管碳基等化学催化剂常被选用与研究催化阴极反应,在催化氧气、硝酸盐、金属离子还原和制氢等方面效果比较显著〔18,24〕.但在环境污染修复应用中,上述化学催化剂其复杂的制备程序、高昂的价格以及复杂环境介质中容易坍塌与中毒,导致催化性能不可逆地下降,在很大程度上成为了制约MECs在实际重金属废水处理中推广应用的重要壁垒.因此,开发容易再生、成本低廉并具有较好催化性能的阴极催化材料对推动MECs的环境应用显得十分重要.不锈钢网以其价格低廉、性能稳定脱颖而出〔32〕,在强化不锈钢网的催化性能时,研究人员发现,网状结构不锈钢的电化学活性表面积是平面结构不锈钢的3倍以上,前者具有更优的催化活性〔33〕.之后研究者又对不锈钢网表面结构进行了改进,将鬃毛刷子插入不锈钢网中制成了比表面积更大的不锈钢网刷,进一步减少了MECs体系的能耗,提高了反应效能〔34〕. ...
Cadmium(Ⅱ) removal mechanisms in microbial electrolysis cells
4
2016
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
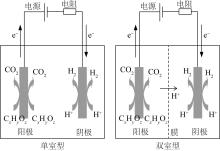
... MECs去除废水中重金属离子的机制主要与电解池中发生的氧化还原反应和微生物群落的活性有关.MECs去除废水中重金属关键在于协调微生物与电化学反应之间的关系,即在发生电化学反应的同时不影响微生物的生理特征,通过调控各种因素(如辅助电压等)来促进反应的进行或改善微生物的生理状况,以获得理想的净化重金属废水的效果.笔者根据目前的研究成果,总结了以下关于MECs去除重金属的机理研究,其可能的机理详情见图2〔25,57-59〕. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Hydrophilic graphene aerogel anodes enhance the performance of microbial electrochemical systems
1
2020
... 随着金属矿产资源的逐渐减少,从不同渠道回收重金属资源成为全球性需求与课题,且重金属的危害较大,故大量的中低浓度重金属废水既是环境问题,又是潜在的金属资源.目前,有关利用MECs净化重金属废水的研究已有大批报道,详见表1.利用MECs去除废水中重金属离子存在多种可能机制,具有较好的净化性能和开发潜力.对于Cr(Ⅵ)、Cu(Ⅱ)和Ag(Ⅰ)等氧化还原电位较高重金属离子基团,可以直接作为阴极电子受体形成自发MFCs还原去除并产电〔9-11〕,如双室MFCs阳极室接种混合污泥,碳布阴极在中低浓度范围内可很好还原沉积游离或络合Au(Ⅲ)和Ag(Ⅰ),效率可达99.0%以上,且具有较高的纯度和回收价值〔12-13〕.而对于Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难以利用MFCs自发反应而去除,需辅助一定的外电压以构建MECs才能实现还原去除,外电压可由外接电源或自发MFCs提供〔14-17〕.众多研究报道证实,MECs被广泛用于净化酸性矿山废水、飞灰浸出液等含重金属废水,与电解等传统电化学相比,可有效减少供电能耗,配合MFCs或电位电控,可以实现多种金属离子的分步还原去除〔18-20〕.随着研究的不断进行,更多的重金属被进行回收处理,如Co(Ⅱ)〔21-22〕、Pb(Ⅱ)〔20,23〕、Ni(Ⅱ)〔24〕等.MECs去除重金属离子的机制,除还原沉积外,还存在生物吸附和次生沉淀等其他可能,如MECs中重金属析氢还原下,因阴极区局部pH升高,促使Cd(Ⅱ)以Cd(OH)2和CdCO3沉淀析出〔25〕.此外,MECs还原重金属涉及复杂的生物电化学过程.其中,阴极催化性能是重金属离子有效利用电子的关键,显著影响重金属催化还原沉积.如前所述,MECs重金属还原等功能的实现与成本,依赖于生物阳极提供和阴极有效利用电子的能力.MECs反应过程涉及复杂的生物电化学过程,大致上包括阳极电化学活性微生物(EAM)厌氧氧化、跨细胞膜电子传递、胞外界面电子传递、阴极电子传递和电子受体还原等过程〔26〕.相应的,MECs阳极高效产电和阴极催化污染去除性能的提高依赖于对上述反应过程的调控,主要受阴/阳极材料、EAM生物膜性能、构型、电子传递中间体、阴极催化性能及其他常规环境参数的影响. ...
Cr(Ⅵ) reduction at rutile-catalyzed cathode in microbial fuel cells
1
2009
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
Nickel ion removal from wastewater using the microbial electrolysis cell
2
2012
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
Heavy metal recovery combined with H2 production from artificial acid mine drainage using the microbial electrolysis cell
1
2014
... Research results of removal of heavy metal ions from wastewater
Table 1| 序号 | 目标离子 | 装置布置及关键参数 | 净化效果 | 途径与机制 | 参考文献 |
|---|
| 1 | Co2+ | 双室MFCs-MECs耦合系统;石墨毡为MFCs和MECs阳极,以及MFCs阴极,碳棒为MECs阴极 | 可有效回收Co2+ | 阴极还原 | 〔21〕 |
| 2 | Ni2+ | 双室MECs;石墨纤维刷为阳极,铜片为阴极 | 去除率达40.7% | 阴极还原 | 〔24〕 |
| 3 | Cd2+ | 单室MECs;石墨纤维刷为阳极,不锈钢网为阴极 | 24 h内去除率达50%~67% | 阴极还原/Cd(OH)2沉淀/CdCO3沉淀 | 〔25〕 |
| 4 | Cr6+ | 双室MFCs;阴极由天然金红石涂层抛光石墨制成,阳极为未抛光的石墨板 | 去除率达97%(26 h) | Cr2O72-被还原为Cr2O3/Cr(OH)3沉淀 | 〔27〕 |
| 5 | Ni2+ | 双室MECs;碳毡为阳极,不锈钢网为阴极;外加电压1.1 V | 去除率达67% | 阴极还原 | 〔28〕 |
| 6 | Zn2+ | 双室MECs;碳毡为阳极,钛丝为阴极;外加电压1.7 V | 3 h内去除率达65.8% | 阴极还原 | 〔20〕 |
| 7 | Cu2+、Ni2+ | 双室MECs;石墨刷为阳极,载铂碳布为阴极;外加电压1.0 V | 24 h内Cu2+去除率达95%,42 h内Ni2+去除率达87% | 阴极还原 | 〔29〕 |
| 8 | Co2+ | 双室MECs;石墨刷为阳极,石墨毡为阴极;外加电压0.3~0.5 V | 6 h内去除率达92.2% | 阴极还原 | 〔22〕 |
| 9 | Ag+ | 双室MFCs;碳刷为阳极,带钛丝的碳纤维为阴极 | 去除率达98.26%~99.91% | 阴极还原 | 〔13〕 |
| 10 | Au3+ | 双室MFCs;碳刷为阳极,碳布为阴极 | 回收率达99.89% | 阴极还原 | 〔12〕 |
2.2 影响MECs去除重金属离子的因素MECs反应过程涉及复杂的生物电化学过程,其影响因素复杂多变.目前,MECs处理重金属废水的影响因素大体上包括阴极材料、溶液特征、辅助电压以及微生物等因素.在众多影响因素中,阴极材料、溶液特征以及辅助电压等对MECs去除重金属离子的影响最为重要,分析清楚这些因素的影响特征和机制是进一步完善MECs去除废水中重金属研究的关键所在. ...
Microbial electrochemical technologies:Electronic circuitry and characterization tools
2
2020
... 在众多影响因素中,阴极作为接受电子的最终场所,阴极催化性能显得尤为重要,决定着目标污染物利用电子发生反应的性能,优化其性能是研究强化污染还原的重要途径〔30-31〕.阴极的设计通常采用化学阴极或生物阴极来增强其催化活性,降低阴极反应过电势,加快反应速率,提高能量利用效率和产品产率.因此,寻求高活性、高性价比的催化剂,一直是MECs阴极的研究重点. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Field tests of cubic-meter scale microbial electrochemical system in a municipal wastewater treatment plant
2
2019
... 在众多影响因素中,阴极作为接受电子的最终场所,阴极催化性能显得尤为重要,决定着目标污染物利用电子发生反应的性能,优化其性能是研究强化污染还原的重要途径〔30-31〕.阴极的设计通常采用化学阴极或生物阴极来增强其催化活性,降低阴极反应过电势,加快反应速率,提高能量利用效率和产品产率.因此,寻求高活性、高性价比的催化剂,一直是MECs阴极的研究重点. ...
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
The use of stainless steel and nickel alloys as low-cost cathodes in microbial electrolysis cells
1
2009
... 与传统电化学方法类似,Pd、Au、Pt等贵金属,过渡金属及氧化物和石墨烯/碳纳米管碳基等化学催化剂常被选用与研究催化阴极反应,在催化氧气、硝酸盐、金属离子还原和制氢等方面效果比较显著〔18,24〕.但在环境污染修复应用中,上述化学催化剂其复杂的制备程序、高昂的价格以及复杂环境介质中容易坍塌与中毒,导致催化性能不可逆地下降,在很大程度上成为了制约MECs在实际重金属废水处理中推广应用的重要壁垒.因此,开发容易再生、成本低廉并具有较好催化性能的阴极催化材料对推动MECs的环境应用显得十分重要.不锈钢网以其价格低廉、性能稳定脱颖而出〔32〕,在强化不锈钢网的催化性能时,研究人员发现,网状结构不锈钢的电化学活性表面积是平面结构不锈钢的3倍以上,前者具有更优的催化活性〔33〕.之后研究者又对不锈钢网表面结构进行了改进,将鬃毛刷子插入不锈钢网中制成了比表面积更大的不锈钢网刷,进一步减少了MECs体系的能耗,提高了反应效能〔34〕. ...
The use and optimization of stainless steel mesh cathodes in microbial electrolysis cells
1
2010
... 与传统电化学方法类似,Pd、Au、Pt等贵金属,过渡金属及氧化物和石墨烯/碳纳米管碳基等化学催化剂常被选用与研究催化阴极反应,在催化氧气、硝酸盐、金属离子还原和制氢等方面效果比较显著〔18,24〕.但在环境污染修复应用中,上述化学催化剂其复杂的制备程序、高昂的价格以及复杂环境介质中容易坍塌与中毒,导致催化性能不可逆地下降,在很大程度上成为了制约MECs在实际重金属废水处理中推广应用的重要壁垒.因此,开发容易再生、成本低廉并具有较好催化性能的阴极催化材料对推动MECs的环境应用显得十分重要.不锈钢网以其价格低廉、性能稳定脱颖而出〔32〕,在强化不锈钢网的催化性能时,研究人员发现,网状结构不锈钢的电化学活性表面积是平面结构不锈钢的3倍以上,前者具有更优的催化活性〔33〕.之后研究者又对不锈钢网表面结构进行了改进,将鬃毛刷子插入不锈钢网中制成了比表面积更大的不锈钢网刷,进一步减少了MECs体系的能耗,提高了反应效能〔34〕. ...
High surface area stainless steel brushes as cathodes in microbial electrolysis cells
1
2009
... 与传统电化学方法类似,Pd、Au、Pt等贵金属,过渡金属及氧化物和石墨烯/碳纳米管碳基等化学催化剂常被选用与研究催化阴极反应,在催化氧气、硝酸盐、金属离子还原和制氢等方面效果比较显著〔18,24〕.但在环境污染修复应用中,上述化学催化剂其复杂的制备程序、高昂的价格以及复杂环境介质中容易坍塌与中毒,导致催化性能不可逆地下降,在很大程度上成为了制约MECs在实际重金属废水处理中推广应用的重要壁垒.因此,开发容易再生、成本低廉并具有较好催化性能的阴极催化材料对推动MECs的环境应用显得十分重要.不锈钢网以其价格低廉、性能稳定脱颖而出〔32〕,在强化不锈钢网的催化性能时,研究人员发现,网状结构不锈钢的电化学活性表面积是平面结构不锈钢的3倍以上,前者具有更优的催化活性〔33〕.之后研究者又对不锈钢网表面结构进行了改进,将鬃毛刷子插入不锈钢网中制成了比表面积更大的不锈钢网刷,进一步减少了MECs体系的能耗,提高了反应效能〔34〕. ...
Microbial electrochemical systems for sustainable biohydrogen production:Surveying the experiences from a start-up viewpoint
1
2017
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Effect of applied voltage and temperature on methane production and microbial community in microbial electrochemical anaerobic digestion systems treating swine manure
1
2019
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Electrochemical and biochemical profiling of the enhanced hydrogenotrophic denitrification through cathode strengthening using bioelectrochemical system(BES)
1
2020
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Autotrophic biocathode for high efficient sulfate reduction in microbial electrolysis cells
1
2014
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
A novel single chamber vertical baffle flow biocathode microbial electrochemical system with microbial separator
1
2019
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Metabolic activity and pathway study of aspirin biodegradation using a microbial electrochemical system supplied by an alternating current
1
2019
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Microbial electrolysis cells with biocathodes and driven by microbial fuel cells for simultaneous enhanced Co(Ⅱ) and Cu(Ⅱ) removal
1
2015
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Operation strategy of cubic-meter scale microbial electrochemistry system in a municipal wastewater treatment plant
1
2019
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Development of methanogens within cathodic biofilm in the single-chamber microbial electrolysis cell
1
2019
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
A study of microbial communities on terracotta separator and on biocathode of air breathing microbial fuel cells
1
2018
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
含铬污水的生物修复技术研究现状及展望
1
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
含铬污水的生物修复技术研究现状及展望
1
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Biological chromium(Ⅵ) reduction in microbial fuel cell:A three in one approach
1
2009
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
Enhancement of hexavalent chromium reduction and electricity production from a biocathode microbial fuel cell
1
2010
... 生物阴极在生物催化去除重金属等污染过程中表现出诸多优势.近十年来,生物阴极在辅助催化产氢〔35〕、产甲烷〔14,36〕、脱氮〔17,37〕、硫酸盐还原〔38〕、有机物降解〔39-40〕和重金属还原〔15,41〕等方面的研究得到了很大发展.研究表明,生物阴极在电化学微生物合成、金属还原回收等方面具有较大的开发潜力〔31,42-43〕.生物阴极应用于重金属离子去除,要克服的问题是重金属对微生物存在的毒害作用,因此,定向筛选构建具有多种重金属耐受性能的EAM菌群生物膜则比较关键〔15,44〕.已有部分研究利用生物阴极净化含重金属废水,通过希瓦氏菌等单菌〔45〕、反硝化混合液〔46〕、污染场地本土微生物〔47〕、生物阳极反转驯化和藻类〔9,18,30〕等作为阴极接种物,构建了多种生物阴极MFCs和MECs反应器,对中低浓度含Cr(Ⅵ)、Cd(Ⅱ)、Co(Ⅱ)等废水处理均起到了很理想的去除效果.更有研究表明,生物阴极上的生物膜可以利用阴极和氧化有机物等获得的电子,发生阴极生物催化反应,在外部电压辅助下,重金属离子去除被有效强化〔9〕. ...
定量评价不同阴极材料对Cd(Ⅱ)还原微生物电解池影响研究
2
2020
... 溶液特征包含多个方面,其中显著影响净化重金属效能的有离子浓度、离子强度、溶解氧以及pH等因素〔48〕. ...
... (4)溶解氧.与溶液pH对重金属去除效能的影响类似,溶液中氧含量的增加会影响净化重金属的效能〔48〕.在有氧环境下利用MECs净化Co(Ⅱ)时发现,Co(Ⅱ)还原回收效率大大降低,而阳极COD的消耗却显著增强〔55〕.这表明氧气的存在会与Co(Ⅱ)竞争电子,使Co(Ⅱ)还原速率和产氢速率都下降,不利于MECs中Co(Ⅱ)的还原. ...
定量评价不同阴极材料对Cd(Ⅱ)还原微生物电解池影响研究
2
2020
... 溶液特征包含多个方面,其中显著影响净化重金属效能的有离子浓度、离子强度、溶解氧以及pH等因素〔48〕. ...
... (4)溶解氧.与溶液pH对重金属去除效能的影响类似,溶液中氧含量的增加会影响净化重金属的效能〔48〕.在有氧环境下利用MECs净化Co(Ⅱ)时发现,Co(Ⅱ)还原回收效率大大降低,而阳极COD的消耗却显著增强〔55〕.这表明氧气的存在会与Co(Ⅱ)竞争电子,使Co(Ⅱ)还原速率和产氢速率都下降,不利于MECs中Co(Ⅱ)的还原. ...
单室微生物电解池处理含镍模拟废水
3
2017
... (1)离子浓度.离子浓度的大小关系着微生物的活性和重金属还原效率,因此离子浓度的大小是影响MECs净化重金属效能的影响因素之一.众所周知,重金属具有很高的生物毒性,会降低微生物的生物活性,且各种微生物对重金属的耐受能力都有一定的限度.因此,重金属浓度过大会使微生物的活性降低,甚至失活,而重金属浓度过低,却可能会达不到最佳的重金属去除效率.有研究表明〔49〕,在0.7 V、初始pH=6.0的条件下,重金属离子去除率随着离子浓度的增加,先在波动中略有上升而后逐渐降低.在达到耐受质量浓度之前(5~12.5 mg/L),去除率在66.5%~70.6%之间波动,波动小且较为稳定,但达到耐受质量浓度(12.5 mg/L)之后,去除率明显降低,说明不断累积的重金属使得微生物的活性降低,以致其还原沉积的效率低下.对于其他的金属离子如Co(Ⅲ)〔21,50〕、Hg(Ⅱ)〔51〕等也有相似的结论.由此而言,控制离子浓度的高低对净化重金属的效能及效率具有重要意义. ...
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
单室微生物电解池处理含镍模拟废水
3
2017
... (1)离子浓度.离子浓度的大小关系着微生物的活性和重金属还原效率,因此离子浓度的大小是影响MECs净化重金属效能的影响因素之一.众所周知,重金属具有很高的生物毒性,会降低微生物的生物活性,且各种微生物对重金属的耐受能力都有一定的限度.因此,重金属浓度过大会使微生物的活性降低,甚至失活,而重金属浓度过低,却可能会达不到最佳的重金属去除效率.有研究表明〔49〕,在0.7 V、初始pH=6.0的条件下,重金属离子去除率随着离子浓度的增加,先在波动中略有上升而后逐渐降低.在达到耐受质量浓度之前(5~12.5 mg/L),去除率在66.5%~70.6%之间波动,波动小且较为稳定,但达到耐受质量浓度(12.5 mg/L)之后,去除率明显降低,说明不断累积的重金属使得微生物的活性降低,以致其还原沉积的效率低下.对于其他的金属离子如Co(Ⅲ)〔21,50〕、Hg(Ⅱ)〔51〕等也有相似的结论.由此而言,控制离子浓度的高低对净化重金属的效能及效率具有重要意义. ...
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
Synergetic interactions improve cobalt leaching from lithium cobalt oxide in microbial fuel cells
1
2013
... (1)离子浓度.离子浓度的大小关系着微生物的活性和重金属还原效率,因此离子浓度的大小是影响MECs净化重金属效能的影响因素之一.众所周知,重金属具有很高的生物毒性,会降低微生物的生物活性,且各种微生物对重金属的耐受能力都有一定的限度.因此,重金属浓度过大会使微生物的活性降低,甚至失活,而重金属浓度过低,却可能会达不到最佳的重金属去除效率.有研究表明〔49〕,在0.7 V、初始pH=6.0的条件下,重金属离子去除率随着离子浓度的增加,先在波动中略有上升而后逐渐降低.在达到耐受质量浓度之前(5~12.5 mg/L),去除率在66.5%~70.6%之间波动,波动小且较为稳定,但达到耐受质量浓度(12.5 mg/L)之后,去除率明显降低,说明不断累积的重金属使得微生物的活性降低,以致其还原沉积的效率低下.对于其他的金属离子如Co(Ⅲ)〔21,50〕、Hg(Ⅱ)〔51〕等也有相似的结论.由此而言,控制离子浓度的高低对净化重金属的效能及效率具有重要意义. ...
Removal of Hg2+ as an electron acceptor coupled with power generation using a microbial fuel cell
2
2011
... (1)离子浓度.离子浓度的大小关系着微生物的活性和重金属还原效率,因此离子浓度的大小是影响MECs净化重金属效能的影响因素之一.众所周知,重金属具有很高的生物毒性,会降低微生物的生物活性,且各种微生物对重金属的耐受能力都有一定的限度.因此,重金属浓度过大会使微生物的活性降低,甚至失活,而重金属浓度过低,却可能会达不到最佳的重金属去除效率.有研究表明〔49〕,在0.7 V、初始pH=6.0的条件下,重金属离子去除率随着离子浓度的增加,先在波动中略有上升而后逐渐降低.在达到耐受质量浓度之前(5~12.5 mg/L),去除率在66.5%~70.6%之间波动,波动小且较为稳定,但达到耐受质量浓度(12.5 mg/L)之后,去除率明显降低,说明不断累积的重金属使得微生物的活性降低,以致其还原沉积的效率低下.对于其他的金属离子如Co(Ⅲ)〔21,50〕、Hg(Ⅱ)〔51〕等也有相似的结论.由此而言,控制离子浓度的高低对净化重金属的效能及效率具有重要意义. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Factors affecting the performance of microbial fuel cells for sulfide and vanadium(Ⅴ) treatment
2
2010
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
... (3)溶液pH.溶液pH在很大程度上影响和控制着MECs体系中重金属离子形态和微生物生长状况,是影响净化重金属效果的重要因素之一.因溶液处于电解状态,溶液中的相关分子在电场作用下会电离产生大量OH-和H+,若反应器为双室结构,隔膜的存在还会使得质子扩散受到阻碍,增大阴阳两极的pH梯度,大大降低重金属的净化效率.若不控制上述变化,过高或过低的pH都将影响微生物的丰度与活性,不利于净化重金属的效果.此外,在MECs处理重金属废水时,通常还要看氢离子是否参与.对有氢离子参与的〔54〕,较低的pH更利于金属还原,如、等的回收.而无需氢离子参与的,低pH的溶液环境会使还原反应与氢离子发生竞争,降低还原效能,如Zn(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)、Co(Ⅱ)等的回收.为了减小pH变化带来的负向影响,目前主要采用的缓解措施有:确定需去除重金属的类型,选择适当的pH范围,添加pH缓冲调节剂,定期更换电解液来有效控制溶液pH,以达到最佳的去除效率〔52,54〕. ...
微生物燃料电池中硫化物氧化和生物阴极的研究
1
2010
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
微生物燃料电池中硫化物氧化和生物阴极的研究
1
2010
... (2)离子强度.MECs内电阻的大小与离子强度联系密切,调控离子强度可以降低内电阻,进而改善重金属还原的效能.在使用MECs进行还原Co(Ⅱ)的实验中发现〔22〕,通过调节离子强度使溶液电导率得到提升(从3.8 mS/cm到5.8 mS/cm),从而增大了回路电流,提高了16.0%的还原效率.在净化Ni(Ⅱ)的实验中,也得出了以上结果〔49〕.上述实验均表明离子强度的增加,加速了反应的进行,提高了金属还原效率.虽然可以通过提高离子强度的方式来提升溶液电导率,降低内阻,但离子强度并不是越高越好.首先,过高的离子浓度对微生物活性存在抑制作用.研究人员在阳极电导率分别为7.4、9.1、12.3、16.1 mS/cm时进行实验,发现污染物去除率在电导率为12.3 mS/cm时达到最大(91%),而电导率为16.1 mS/cm时,污染物的去除率反而下降〔52〕.分析认为,离子强度过大,改变了溶液的渗透压,打破了微生物细胞内部离子平衡,使反应效率大大降低.其次,离子强度太大,容易使得电极钝化,影响反应的进行〔53〕.因此必须确定合适的离子强度,以达到快速去除重金属的目的. ...
Electricity production during the treatment of real electroplating wastewater containing Cr6+ using microbial fuel cell
2
2008
... (3)溶液pH.溶液pH在很大程度上影响和控制着MECs体系中重金属离子形态和微生物生长状况,是影响净化重金属效果的重要因素之一.因溶液处于电解状态,溶液中的相关分子在电场作用下会电离产生大量OH-和H+,若反应器为双室结构,隔膜的存在还会使得质子扩散受到阻碍,增大阴阳两极的pH梯度,大大降低重金属的净化效率.若不控制上述变化,过高或过低的pH都将影响微生物的丰度与活性,不利于净化重金属的效果.此外,在MECs处理重金属废水时,通常还要看氢离子是否参与.对有氢离子参与的〔54〕,较低的pH更利于金属还原,如、等的回收.而无需氢离子参与的,低pH的溶液环境会使还原反应与氢离子发生竞争,降低还原效能,如Zn(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)、Co(Ⅱ)等的回收.为了减小pH变化带来的负向影响,目前主要采用的缓解措施有:确定需去除重金属的类型,选择适当的pH范围,添加pH缓冲调节剂,定期更换电解液来有效控制溶液pH,以达到最佳的去除效率〔52,54〕. ...
... ,54〕. ...
Assessment of five different cathode materials for Co(Ⅱ) reduction with simultaneous hydrogen evolution in microbial electrolysis cells
2
2015
... (4)溶解氧.与溶液pH对重金属去除效能的影响类似,溶液中氧含量的增加会影响净化重金属的效能〔48〕.在有氧环境下利用MECs净化Co(Ⅱ)时发现,Co(Ⅱ)还原回收效率大大降低,而阳极COD的消耗却显著增强〔55〕.这表明氧气的存在会与Co(Ⅱ)竞争电子,使Co(Ⅱ)还原速率和产氢速率都下降,不利于MECs中Co(Ⅱ)的还原. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Efficacy of single-chamber microbial fuel cells for removal of cadmium and zinc with simultaneous electricity production
1
2014
... 外加电源是MECs体系的核心组成之一,在不同电压梯度下,溶液中的阴阳离子受到的迁移、电泳等作用强度差异显著,因此,电压梯度是影响MECs技术的重要因素.有关文献表明,电压梯度能影响微生物的活性,进而影响微生物的生长代谢.如在对Ni2+进行净化时发现〔28〕,当辅助电压从0.5 V到1.1 V时,电流密度从(32±1.9)A/m3增加到(304±23.1)A/m3,去除效率从(51±4.6)%增加到(67±5.3)%.去除效率的增加与阴极电位的绝对值随辅助电压的增加而增加有关.在较高的外加电压下,更多的电子可用于阴极反应,导致更多的Ni2+被还原.概括而言,在电压梯度较低的电场条件下,电场刺激不够,无法发挥促进微生物生长代谢和活化重金属离子等作用.在中等强度电场条件下,进一步增大了重金属离子的还原净化量,提高了MECs的效率.而过高的电压梯度虽然对离子迁移有更大的推动力,可以增强净化重金属的效率,但对于微生物而言,过高的电压梯度则会抑制微生物的活性,对微生物的生命活动造成影响,进而降低反应效率,减少重金属的还原量〔49〕.此外,当重金属在阴极还原沉积时,如Cd(Ⅱ)、Zn(Ⅱ)、Ni(Ⅱ)等氧化还原电位为负的重金属离子,难于利用自发反应去除,需安排一定的辅助电压才能实现还原去除〔14-17〕,在配合MFCs或不同梯度的辅助电压下,还可以有效实现多种金属离子的分步还原去除〔20,56〕. ...
Heavy metal removal from wastewater using microbial electrolysis cells
1
2016
... MECs去除废水中重金属离子的机制主要与电解池中发生的氧化还原反应和微生物群落的活性有关.MECs去除废水中重金属关键在于协调微生物与电化学反应之间的关系,即在发生电化学反应的同时不影响微生物的生理特征,通过调控各种因素(如辅助电压等)来促进反应的进行或改善微生物的生理状况,以获得理想的净化重金属废水的效果.笔者根据目前的研究成果,总结了以下关于MECs去除重金属的机理研究,其可能的机理详情见图2〔25,57-59〕. ...
Adsorption of nickel on husk of Lathyrus sativus:Behavior and binding mechanism
1
2007
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
Cadmium recovery by coupling double microbial fuel cells
2
2014
... MECs去除废水中重金属离子的机制主要与电解池中发生的氧化还原反应和微生物群落的活性有关.MECs去除废水中重金属关键在于协调微生物与电化学反应之间的关系,即在发生电化学反应的同时不影响微生物的生理特征,通过调控各种因素(如辅助电压等)来促进反应的进行或改善微生物的生理状况,以获得理想的净化重金属废水的效果.笔者根据目前的研究成果,总结了以下关于MECs去除重金属的机理研究,其可能的机理详情见图2〔25,57-59〕. ...
... 在MECs中,通常研究的重金属去除机理是阴极还原.在高浓度重金属溶液或酸性条件下,阴极还原可能是主要的去除机制〔22,55〕.众所周知,MECs的镉去除是通过阴极还原〔20,59〕.除阴极还原外,还存在着生成化学沉淀的可能,如MECs去除重金属发生析氢还原反应时,因阴极区局部pH升高,使得Cd(Ⅱ)以Cd(OH)2或CdCO3沉淀析出〔25〕.此外,有研究表明,在利用MECs净化Pb2+的过程中,在阳极和阴极室中都观察到独立的Pb2+去除.通过分析阳极电位和阳极沉积,证实了Pb2+在阳极被还原去除,而使用乙醇灭活阳极产电微生物后则不会导致Pb2+的去除〔51〕,这表明阳极微生物也与重金属的去除机制有关.除此之外,重金属的去除也会与生物吸附相关,微生物细胞表面的多聚物、官能团(羧基、羟基和氨基等)会和某些重金属离子结合形成配合物〔58〕. ...
In-situ Cr(Ⅵ) reduction with electrogenerated hydrogen peroxide driven by iron-reducing bacteria
1
2011
... 对于微生物群落,有研究表明,在利用MFCs去除Cr(Ⅵ)时,采用了两种不同类型的微生物,单一菌种和混合菌群.实验结果发现净化能力最好的是混合菌群,而Shewanella decolorationis S12、Klebsiella pneumoniae L17等单一菌种的净化能力较低〔60〕.这表明微生物群落之间的共同作用可以提高重金属离子的还原效率.综合上述研究成果,MECs可以通过阴极还原、阴极化学沉淀、微生物吸附以及加强微生物群落共同作用等实现废水中重金属的去除. ...
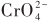 、
、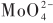 等的回收。而无需氢离子参与的,低pH的溶液环境会使还原反应与氢离子发生竞争,降低还原效能,如Zn(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)、Co(Ⅱ)等的回收。为了减小pH变化带来的负向影响,目前主要采用的缓解措施有:确定需去除重金属的类型,选择适当的pH范围,添加pH缓冲调节剂,定期更换电解液来有效控制溶液pH,以达到最佳的去除效率〔52,54〕。
等的回收。而无需氢离子参与的,低pH的溶液环境会使还原反应与氢离子发生竞争,降低还原效能,如Zn(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)、Co(Ⅱ)等的回收。为了减小pH变化带来的负向影响,目前主要采用的缓解措施有:确定需去除重金属的类型,选择适当的pH范围,添加pH缓冲调节剂,定期更换电解液来有效控制溶液pH,以达到最佳的去除效率〔52,54〕。





 津公网安备 12010602120337号
津公网安备 12010602120337号