本研究以SMX为目标污染物,在电絮凝(EC)/过单硫酸盐(PMS)体系中考察了电流、PMS浓度、初始pH、SMX初始质量浓度等因素对SMX降解过程的影响,并基于猝灭实验对体系中产生的自由基的分析,对电絮凝活化过硫酸盐机理进行了探究,以期为电絮凝活化PMS技术的应用和推广提供参考。
1 材料与方法
1.1 实验材料
磺胺甲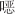 唑(C10H11N3O3S,质量分数≥98%)与过硫酸氢钾(PMS),均为分析纯,购于Aladdin公司;氢氧化钠、硫酸、甲酸、叔丁醇,均为分析纯,购于国药集团化学试剂有限公司;甲醇,HPLC级,购于美国Fisher公司;电极材质为纯铁片(铁质量分数>99.5%),尺寸为8 cm × 1.5 cm;实验用水均为电阻率18.25 MΩ·cm的超纯水。
唑(C10H11N3O3S,质量分数≥98%)与过硫酸氢钾(PMS),均为分析纯,购于Aladdin公司;氢氧化钠、硫酸、甲酸、叔丁醇,均为分析纯,购于国药集团化学试剂有限公司;甲醇,HPLC级,购于美国Fisher公司;电极材质为纯铁片(铁质量分数>99.5%),尺寸为8 cm × 1.5 cm;实验用水均为电阻率18.25 MΩ·cm的超纯水。
1.2 实验仪器
高效液相色谱仪(FL2200,浙江福立分析仪器股份有限公司),配套C18色谱柱(4.6 mm×250 mm×5 µm,岛津技迩商贸有限公司);多功能水质分析仪(XLD-Multi-350i,德国WTW集团);超纯水机(ZWM,湖南中沃水务环保科技有限公司);电子天平(AL204,瑞士Mettler Toledo集团);直流电源(GPS-2303C,台湾固纬电子有限公司);电流表(F15B+,美国Fluke公司);超声波清洁仪器(PS-30AD,深圳市洁康洗净电器有限公司)。
1.3 实验方法
实验装置如图1所示,采用550 mL的圆柱形玻璃反应器进行实验,内装有500 mL电解液,置有2片纯铁电极(8 cm×1.5 cm),极板间距为2 cm。选择10 mmol/L Na2SO4溶液为电解液,电解过程中采用磁力搅拌器使溶液保持完全混合;稳压直流电源供电,采用电流表对电流进行监测。
图1
具体实验步骤如下:将500 mL超纯水置于550 mL的玻璃容器中,加入一定量SMX和Na2SO4,通过0.1 mol/L的H2SO4和0.1 mol/L的NaOH调节初始pH至一定值,加入PMS并通电后开始计时。分别在0、0.5、1、2、4、6、8 min取样,并将样品用0.22 μm滤膜过滤,取1 mL过滤液,加入过量的甲醇猝灭,分析其中SMX的浓度。所有实验至少重复2次及以上。实验中所配SMX反应液初始pH为7。下文若未特殊说明,反应基本条件均控制为:SMX初始质量浓度为1 mg/L,初始pH为7,电解质Na2SO4浓度为10 mmol/L,电流为10 mA,极板间距为2 cm。
1.4 分析方法
SMX质量浓度采用高效液相色谱(FL2200)测定。色谱柱条件:柱温20 ℃,流动相采用体积比为35∶65的甲醇和0.1%甲酸溶液,流速为1 mL/min,进样量为20 μL,检测波长270 nm。
2 结果与讨论
2.1 不同反应体系对SMX的降解效率
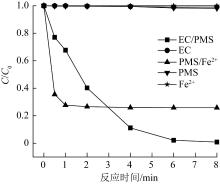
考察单独EC、单独投加Fe2+(37 μmol/L)、单独投加PMS(20 μmol/L)、PMS(20 μmol/L)/Fe2+(37 μmol/L)和EC/PMS(20 μmol/L)共计5种不同体系降解SMX的效率,实验结果见图2。
图2
由图2可以看出,6 min内EC、Fe2+、PMS体系对SMX的降解极少,说明这3种体系基本上对SMX不降解。PMS/Fe2+体系在1 min内对SMX的降解率为72.3%,6 min时降解率为74.2%,说明直接投加Fe2+能够快速活化PMS。EC/PMS体系随反应时间延长,降解率逐渐增加,在6 min时对SMX的降解率可达到97.8%,这说明,与直接投加Fe2+的PMS/Fe2+体系相比,通过铁电絮凝缓慢地释放出Fe2+更有利于对SMX的降解,这是因为PMS/Fe2+体系在短时间内Fe2+活化PMS产生的大量SO4•-会发生猝灭而被消耗,如
2.2 电流对SMX 降解的影响
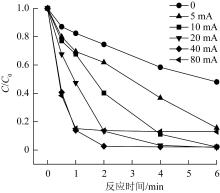
根据法拉第电解定律,EC/PMS体系电解过程中产生的Fe2+的量与电流、通电时间成正比。为了研究电流对PMS/EC体系降解SMX的影响,考察了反应时间6 min时不同电流对PMS/EC体系降解SMX的影响,实验结果见图3。
图3
图3
电流对EC/PMS体系降解SMX的影响
Fig. 3
The effect of current on the degradation of SMX in EC/PMS system
由图3可知,当电流为0时,铁片在水中因被腐蚀而产生Fe2+,从而活化PMS产生SO4·-降解SMX,SMX的降解率为52.9%;当电流为5 mA时,SMX的降解率为84.4%;电流从10 mA增加到40 mA时,不同电流条件下,SMX的降解率均能达到97.8%及以上;而当电流继续增加至80 mA时,反应在2 min内就结束了,但对SMX的降解率却仅有87.1%。这是因为,在一定范围内,提高电流会增加Fe2+的产生量,加快活化PMS的速率,生成·OH和SO4·-的量随之增加,从而提高了SMX的降解率,但当电流过大时,相同时间内产生的Fe2+就会过量,短时间内PMS大量分解产生·OH和SO4·-会加快SMX的降解速率,然而生成的·OH和SO4·-会与Fe2+发生反应造成消耗〔
式中:EEO——单位电能,kW·h/m³;
P——功率,kW;
t——电解时间,h;
V——处理体积,m³;
C0——初始时刻SMX的质量浓度,mg/L;
Ct ——t时刻SMX的质量浓度,mg/L。
当水中SMX初始质量浓度为1 mg/L,电流分别为10 mA和40 mA时,降解率基本持平时能耗如表1所示,显然二者在6 min反应时间内均能取得较好的降解效果,但电流为10 mA时能耗更低,而电流为40 mA时反应更快。考虑到电流为40 mA条件下短时间内体系中就会产生大量Fe2+,反应迅速,不利于考察其他反应因素对该实验的影响,故该实验选用电流10 mA为基本反应条件,以便于研究的开展。
表1 10 mA和40 mA电流下降解率基本持平时能耗比较
Table 1
| 电流/mA | 电解时间/min | 降解率/% | EEO/(kW·h·m-3) |
|---|---|---|---|
| 10 | 6 | 97.8 | 9.65×10-4 |
| 40 | 2 | 97.3 | 3.74×10-3 |
2.3 PMS浓度对 SMX 降解的影响
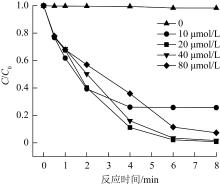
为确定EC/PMS反应体系中最佳PMS浓度,本研究设置了PMS浓度分别为0、10、20、40、80 μmol/L的5组实验进行考察,实验结果见图4。
图4
图4
PMS浓度对EC/PMS体系降解SMX的影响
Fig. 4
The effect of PMS concentration on the degradation of SMX in the EC/PMS system
2.4 初始pH对SMX降解的影响
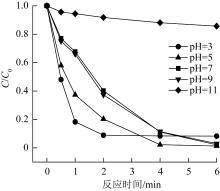
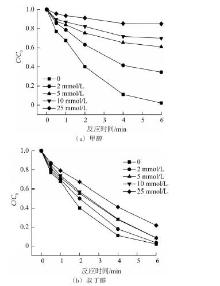
溶液pH会影响Fe2+的存在形态和PMS的活化效果,因此本研究设置了pH为3、5、7(原液)、9、11的5组实验,以探究溶液初始pH对EC/PMS反应体系的影响,实验结果见图5。
图5
图5
初始pH对EC/PMS体系降解SMX的影响
Fig. 5
The effect of initial pH on the degradation of SMX in the EC/PMS system
由图5可以看出,初始pH为3时,EC/PMS体系2 min内即可完成对SMX的降解,降解率为91.7%。这是因为铁片在强酸性条件下更易被腐蚀,能短时间内产生大量的Fe2+来活化PMS,加快了反应速率,但过量的Fe2+会消耗一定的自由基,从而一定程度上抑制了对SMX的降解,致使最终降解率不够理想。当初始pH为5、7、9时,SMX降解速率随着pH的提高有所降低,最终降解率分别为98.7%、97.8%、97.0%,相较于pH=3时最终降解率有所提高。当pH为11时,SMX降解速率和降解率均明显下降,这是因为在强碱性条件下,溶液中的大部分Fe2+形成氢氧化物沉淀,使得Fe2+减少,从而抑制了对SMX的降解;另外,在强碱性条件下,PMS中HSO5-会发生如式(
2.5 初始SMX质量浓度对SMX降解的影响
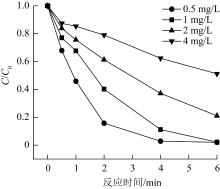
图6
图6
初始SMX质量浓度对EC/PMS体系降解SMX的影响
Fig. 6
The effect of initial SMX mass concentration on the degradation of SMX in the EC/PMS system
表2 不同SMX质量浓度下SMX的降解总量
Table 2
| 初始SMX质量浓度/(mg·L-1) | 0.5 | 1 | 2 | 4 |
|---|---|---|---|---|
| 降解总量/mg | 0.245 | 0.489 | 0.799 | 0.976 |
由图6可知,SMX初始质量浓度为0.5 mg/L时,在6 min内SMX的降解率为98%,当SMX初始质量浓度超过1 mg/L时,6 min内EC/PMS体系对SMX的降解率随着SMX浓度的增加而下降,SMX的初始质量浓度从1 mg/L增加至4 mg/L时,降解率从97.8%减少到48.8%。由表2知,SMX的降解率虽然有所降低,但SMX降解总量却是上升的。这是因为在电流和PMS的量一定的条件下,当SMX浓度较低时,反应中产生的·OH和SO4·-的量足够降解SMX,反应迅速;当SMX浓度增加时,由于·OH和SO4·-在体系中浓度相对减少会降低SMX降解率,但是一定量的·OH和SO4·-与SMX反应几率增加,即自由基利用更加充分,导致SMX被降解的总量增加〔18〕。
2.6 自由基的鉴定及反应机理分析
甲醇与·OH和SO4·-反应非常快,其反应速率常数分别为(1.2~2.8)×109 L/(mol·s)和(1.6~7.8)×107 L/(mol·s)〔19〕,对二者均有很好的猝灭效果。叔丁醇与·OH能快速反应,其反应速率常数为(3.8~7.6)×108 L/(mol·s),而叔丁醇与SO4·-的反应速率常数仅为(4.0~9.1)×105 L/(mol·s)〔20〕。利用甲醇和叔丁醇与不同自由基反应存在的反应速率常数的差异可以鉴别出反应中的主要自由基。实验设定SMX初始质量浓度为1 mg/L,初始pH为7,电解质Na2SO4浓度为10 mmol/L,PMS浓度为20 μmol/L,电流为10 mA,极板间距为2 cm,此条件下采用甲醇和叔丁醇作为猝灭剂进行自由基猝灭实验,并与空白组进行对照,以探究EC/PMS体系产生的主要自由基,结果见图7。
图7
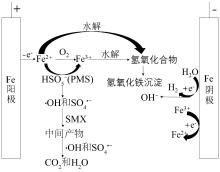
由图7可知,随着甲醇浓度从0逐渐上升到25 mmol/L,SMX的降解受到的抑制作用也越来越强烈,SMX降解率从最初的97.8%降低至15%。而叔丁醇浓度从0~25 mmol/L变化时,其对SMX降解的抑制作用相对甲醇较小,SMX降解率从97.8%降低至78.2%。因此,可以初步认为EC/PMS体系降解SMX过程中主要自由基为·OH和SO4·-,且SO4·-在反应中贡献率较大。据此,对EC/PMS体系降解SMX的机理进行推测,结果如图8所示。在外加电源的作用下,通过电解铁阳极产生Fe2+,同时阴极电解水产生H2,且Fe2+被空气氧化所形成的Fe3+可能在阴极又被还原为Fe2+,利用这些Fe2+活化PMS可生成活性自由基·OH和SO4·-,从而直接降解目标污染物。
图8
图8
EC/PMS体系降解SMX的机理示意
Fig. 8
Schematic diagram of the mechanism of degradation of SMX in EC/PMS system
3 结论
(1)在SMX初始质量浓度为1 mg/L、初始pH=7、PMS浓度为20 μmol/L、电流为10 mA的条件下,通过电絮凝缓慢地释放Fe2+,EC/PMS体系在6 min内对SMX降解率可达97.8%;
(2)增加电流和PMS浓度能提高SMX的降解效率,但是电流超过40 mA或PMS浓度超过20 μmmol/L均会抑制SMX的降解;体系初始pH为5~9时,对SMX都能有很好的降解效果,而初始pH为3时SMX的降解率会稍有降低,但初始pH为11时SMX的降解会受到严重抑制。
(3)EC/PMS体系产生的主要活性自由基为·OH和SO4·-,其中SO4·-所占比例较大。
参考文献
磺胺类抗生素污染现状及其环境行为的研究进展
[J].
Research progress in pollution situation and environmental behavior of Sulfonamides
[J].
Occurrence and toxicity of antibiotics in the aquatic environment:A review
[J].
过硫酸盐的非自由基氧化降解磺胺抗生素的效能及机制
[D].
Performance and mechanism of sulfonamides degradation by the nonradical oxidation of persulfates
[D].
中国典型河流水域抗生素的赋存状况及风险评估研究
[J].
Occurrence and risk assessment of antibiotics in typical river basins in China
[J].
Insights into the mechanism of persulfate activated by rice straw biochar for the degradation of aniline
[J].
A review of the recent advances on the treatment of industrial wastewaters by sulfate radical-based advanced oxidation processes(SR-AOPs)
[J].
Hydroxyl and sulfate radical-based oxidation of RhB dye in UV/H2O2 and UV/persulfate systems:Kinetics,mechanisms,and comparison
[J].
联合活化过硫酸盐及其去除污水中污染物研究进展
[J].
Joint activation of persulfate and its removal of pollutants in wastewater:Progresses and perspective
[J].
Generation of sulfate radical through heterogeneous catalysis for organic contaminants removal:Current development,challenges and prospects
[J].
Sulfate radical and its application in decontamination technologies
[J].
过硫酸盐活化方法的研究进展
[J].
Research progress on persulfate activation method
[J].
Improved sulfamethoxazole degradation by the addition of MoS2 into the Fe2+/peroxymonosulfate process
[J].
Challenges and opportunities for electrochemical processes as next-generation technologies for the treatment of contaminated water
[J].
Titanium dioxide/oxidized carbon fiber electrodes electrochemically produced and their influences on Brilliant Green dye degradation
[J].
Degradation of azo dye Orange G in aqueous solutions by persulfate with ferrous ion
[J].
Enhancement of ciprofloxacin degradation in the Fe(Ⅱ)/peroxymonosulfate system by protocatechuic acid over a wide initial pH range
[J].
Application of a peroxymonosulfate/cobalt〔PMS/Co(Ⅱ)〕 system to treat diesel-contaminated soil
[J].
四氧化三铁负载纳米零价铁类Fenton法降解水中磺胺甲 唑
唑
Degradation of sulfamethoxazole in water by Fenton-like process using ferriferrous oxide supported nanometer zero-valent iron
[J].
Degradation of sulfamethoxazole by Co3O4-palygorskite composites activated peroxymonosulfate oxidation
[J].
Synergistic effects of persistent free radicals and visible radiation on peroxymonosulfate activation by ferric citrate for the decomposition of organic contaminants
[J].



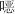 唑(SMX)是一种具有广谱抗菌性的磺胺类药物,临床用于治疗急性支气管炎、扁桃体炎等疾病〔
唑(SMX)是一种具有广谱抗菌性的磺胺类药物,临床用于治疗急性支气管炎、扁桃体炎等疾病〔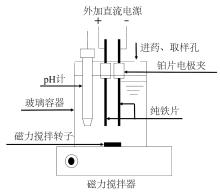


 津公网安备 12010602120337号
津公网安备 12010602120337号