近年来,来自冶炼、电镀、化工等行业的含重金属离子废水大量进入自然水体,已经对自然环境和生态链带来严重的威胁。在这些污染物中,重金属汞离子(主要以微量Hg2+的形式存在)由于具有高毒性、易在生物体内蓄积等特性而受到广泛关注。
因此,本实验采用一种安全、高效、绿色的方法,以L-半胱氨酸(L-Cysteine)和聚吡咯(Ppy)为改性前驱体,以Fe3O4为磁性载体,以高岭土为基体材料,形成L-Cysteine和Ppy双官能团改性的磁性高岭土复合材料m@Kaolin-LC/Ppy,并用于对水体中Hg2+的去除研究,旨在为高岭土材料在水处理领域中的进一步应用,尤其是对重金属离子的去除提供技术参考。
1 实验部分
1.1 材料与仪器
材料:高岭土(Kaolin)由江苏若焱环境设计有限公司提供,FeCl3·6H2O、吡咯单体(Py)、L-半胱氨酸(L-Cysteine)、十二烷基苯磺酸钠等购买于上海国药,均为分析纯。
仪器:FEG250型扫描电子显微镜(SEM);Autosorb-IQZ-MP-XR-VP 型N2吸附-解吸装置;Nicolet-6700型傅立叶变换红外光谱(FT-IR);D/MAX-2550型X射线衍射(XRD);PPMS-9型磁强计(VSM);F732-VJ型冷原子吸收测汞仪。
1.2 m@Kaolin-LC/Ppy的制备
采用课题组以往的方法得到磁性Fe3O4〔18〕。m@Kaolin-LC/Ppy的制备方法如下:将0.15 g高岭土和1.5 g L-半胱氨酸加入200 mL去离子水中,超声搅拌6 h,随后加入0.025 g十二烷基苯磺酸钠,搅拌30 min后,再缓慢加入0.2 mL吡咯。另取3.0 g FeCl3·6H2O溶解于10 mL去离子水中,超声分散10 min后,将其缓慢滴加到上述高岭土的溶液中,继续搅拌6 h后用外加磁场进行固液分离,所得固体材料用去离子水洗涤6~8次,然后以333 K的温度烘干即可获得L-半胱氨酸和聚吡咯改性的磁性高岭土复合材料m@Kaolin-LC/Ppy。
1.3 实验部分
称取一定量的m@Kaolin-LC/Ppy复合材料,置于含100 mL Hg2+溶液的锥形瓶中,于不同pH和温度条件下震荡8 h,再抽取3 mL混合液并经0.45 μm滤膜过滤后,采用分光光度计测定溶液中剩余的Hg2+浓度,并根据初始Hg2+质量浓度C0(mg/L)、Hg2+吸附平衡质量浓度Ce(mg/L)、溶液体积V(L)和投加的吸附剂质量m(g),可计算出m@Kaolin-LC/Ppy对 Hg2+的平衡吸附容量qe(mg/g)。
2 结果与讨论
2.1 表面特性
Kaolin、磁性高岭土(m@Kaolin)及m@Kaolin-LC/Ppy的表征结果见图1。
图1
图1
Kaolin、m@Kaolin和m@Kaolin-LC/Ppy的表征结果
Fig. 1
Characterization results of Kaolin,m@Kaolin and m@Kaolin-LC/Ppy
2.2 结构特性
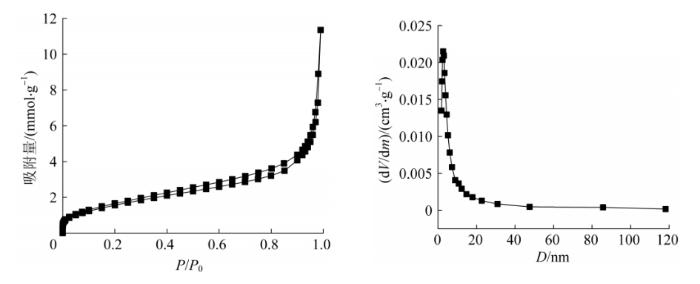
m@Kaolin-LC/Ppy的N2吸附脱附分析及孔径分布见图2。
图2
图2
m@Kaolin-LC/Ppy的N2吸附脱附分析及孔径分布
Fig.2
N2 adsorption/desorption plot and pore size distribution of m@Kaolin-LC/Ppy
由图2可知,高岭土在添加磁核并负载L-半胱氨酸和聚吡咯后,其比表面积由原来的10.30 m2/g增加到25.21 m2/g,平均孔径由原来的11.53 nm下降到6.51 nm。尽管改性后高岭土的平均孔径有所下降,但其孔容却由改性前的0.03 cm3/g增加到改性后的0.18 cm3/g。孔容及比表面积的增加,有利于m@Kaolin-LC/Ppy对Hg2+的吸附。
2.3 XRD
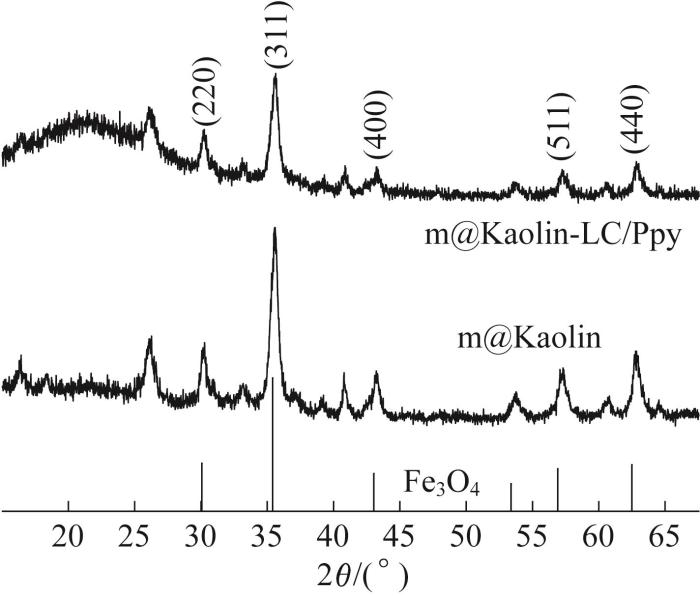
m@Kaolin-LC/Ppy的XRD见图3。
图3
由图3可知,30.6°、35.5°、43.6°、57.6°、63.0°处的特征衍射峰分别对应于m@Kaolin-LC/Ppy中Fe3O4的衍射面(220)、(311)、(400)、(511)、(440)。这些特征峰的位置及峰强与Fe3O4的XRD标准卡所示晶面完全一致,表明了Fe3O4已成功地负载到了高岭土的表面。
m@Kaolin-LC/Ppy在20°~25°出现的宽峰,是由于非晶态聚合物的典型特征引起的。由于聚吡咯的负载,m@Kaolin-LC/Ppy中m@Kaolin的特征峰减弱,再采用L-半胱氨酸改性后,m@Kaolin-LC/Ppy的峰与m@Kaolin的峰相比没有明显变化,表明Ppy和LC已成功负载到m@Kaolin的表面,且合成材料的结构较为稳定。
2.4 红外特征
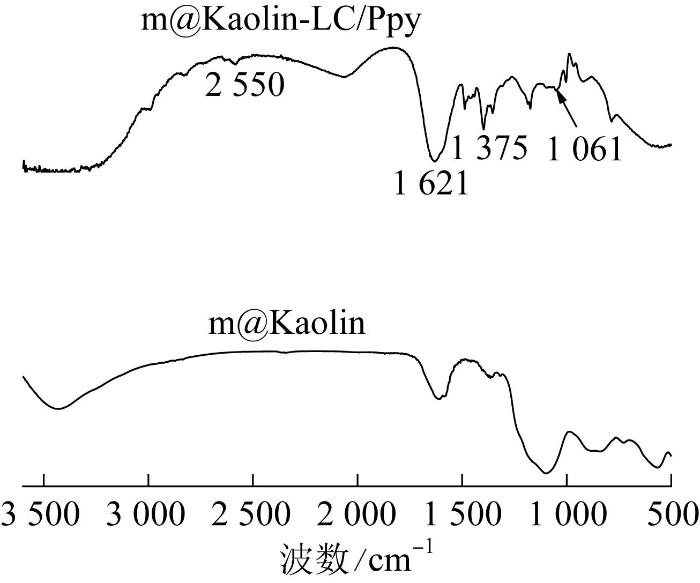
m@Kaolin-LC/Ppy的FT-IR见图4。
图4
2.5 磁化强度特征
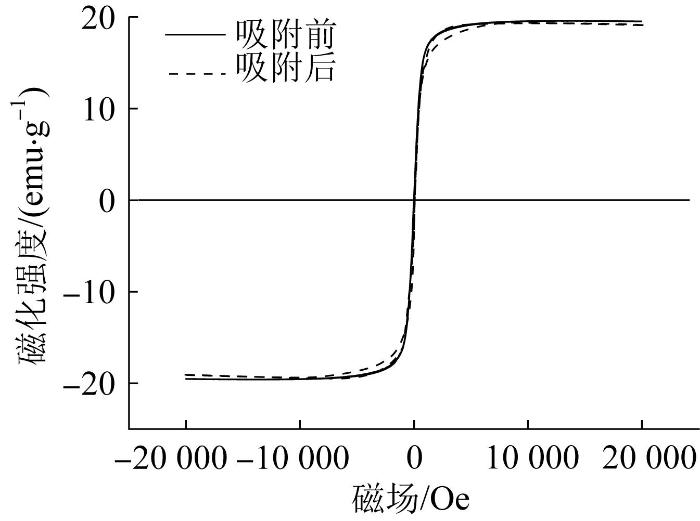
m@Kaolin-LC/Ppy的磁滞回线见图5。
图5
由图5可知,本实验制备的m@Kaolin-LC/Ppy材料具有典型的S型磁滞回线,其吸附前后的饱和磁化强度约为20 emu/g。在实际操作过程中,m@Kaolin-LC/Ppy吸附重金属汞离子后,20 emu/g的饱和磁化强度依然能够使其在外界磁场作用下快速从水中分离出来,表明了较好的应用潜力。
2.6 pH对Hg2+吸附的影响
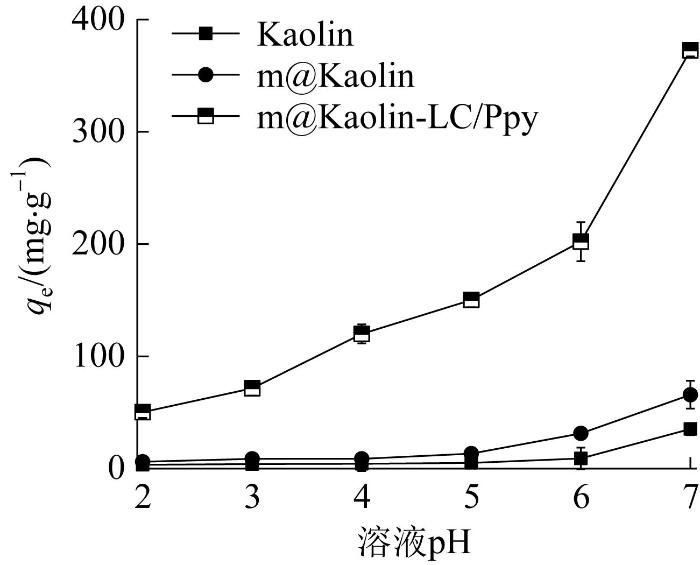
在Hg2+初始质量浓度为40 mg/L,吸附剂投加量为0.05 g/L,反应温度为25 ℃,吸附时间为8 h的条件下,考察不同溶液pH对m@Kaolin-LC/Ppy吸附性能的影响,结果见图6。
图6
由图6可知,随着pH的升高,m@Kaolin-LC/Ppy的吸附容量逐渐增加,m@Kaolin-LC/Ppy中的聚吡咯蕴含有丰富的氨基基团,当pH小于5时,氨基基团轻微质子化会使得氨原子具有孤对电子,为维持电荷中性会吸引更多阴离子。此时,负一价的巯基会与溶液中的汞离子形成—S—Hg+而带正电荷,从而影响对汞离子的吸附;当pH大于5时,共聚物上的氨基完成了去质子化,具有孤对电子的氨原子则成为汞离子的主要吸附位点,并与Hg2+形成稳定的金属络合物—N—Hg。同时在高pH下,Hg2+会以HgOH+和Hg(OH)2的形式出现,并与—SH形成中性的—S—HgOH,实现了在高pH下对Hg2+的高效去除。在pH=7时,m@Kaolin-LC/Ppy对Hg2+的吸附容量达到了372.5 mg/g。
m@Kaolin-LC/Ppy与其他吸附剂对Hg2+吸附能力的对比见表1。
表1 不同吸附剂对Hg2+的吸附能力比较
Table 1
由表1可知,m@Kaolin-LC/Ppy对Hg2+具有极高的吸附容量,优于许多其他吸附材料,表明m@Kaolin-LC/Ppy对去除水中重金属汞的明显优势与应用潜力。
2.7 吸附动力学
图7
图7
m@Kaolin-LC/Ppy对Hg2+吸附的动力学拟合
Fig. 7
Kinetic fitting of Hg2+ adsorption onto m@Kaolin-LC/Ppy
表2 拟合参数
Table 2
| 准一级动力学模型 | |||||
|---|---|---|---|---|---|
| qe,exp/(mg·g-1) | qe,cal/(mg·g-1) | k1/min-1 | R2 | X2 | |
| 372.5 | 366.24 | 0.01 | 0.978 5 | 0.960 5 | |
| 准二级动力学模型 | |||||
| qe,exp/(mg·g-1) | qe,cal/(mg·g-1) | k2/(g·mg-1·min-1) | R2 | X2 | |
| 372.5 | 398.25 | 2.11 | 0.990 3 | 0.991 2 | |
| 颗粒内扩散模型 | |||||
| Kd1/(mg·g-1·min-0.5) | C1/(mg·g-1) | R12 | |||
| 2.34 | 48.35 | 0.938 4 | |||
| Kd2/(mg·g-1·min-0.5) | C2/(mg·g-1) | R22 | |||
| 0.59 | 181.67 | 0.944 3 | |||
| Kd3/(mg·g-1·min-0.5) | C3/(mg·g-1) | R32 | |||
| 0.24 | 277.35 | 0.902 8 | |||
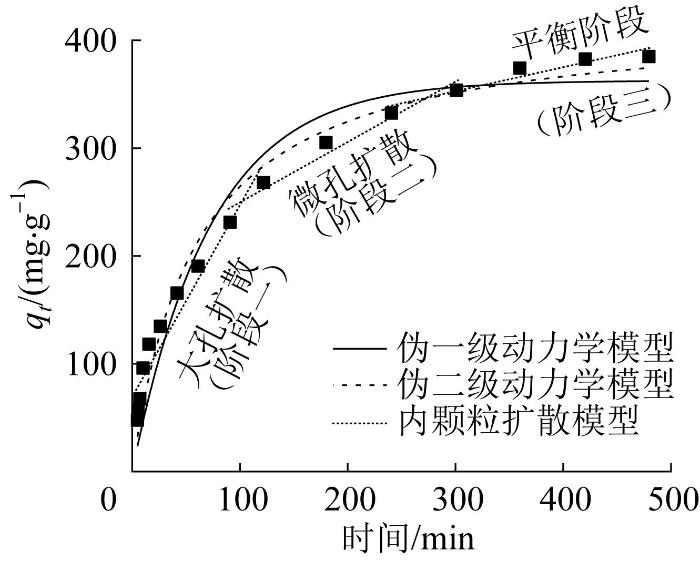
m@Kaolin-LC/Ppy对Hg2+的吸附过程可分为3个阶段,分别为第一阶段的大孔扩散过程、第二阶段的微孔扩散过程和第三阶段的吸附平衡阶段。在第一阶段和第二阶段,大量Hg2+在浓度梯度的作用下,快速由液相向固相(吸附剂外表面)扩散,同时,通过化学作用吸附在m@Kaolin-LC/Ppy的外表面上,相应的吸附常数Kd1、Kd2分别对应于Hg2+的快速、瞬时吸附。
在第三阶段,游离的Hg2+逐渐向m@Kaolin-LC/Ppy的孔内表面进行扩散,并逐渐达到吸附平衡,该过程进行得较为缓慢,相应的吸附常数与第一阶段相比下降了近90%,对应于Hg2+的缓慢、平衡吸附。另外,第三阶段的C3不为0,也进一步印证了Hg2+在m@Kaolin-LC/Ppy上的吸附过程涉及化学吸附〔25〕。
2.8 等温吸附
Langmuir和Freundlich等温模型用来对Hg2+在m@Kaolin-LC/Ppy上的吸附过程进行拟合,以进一步考察所制备吸附剂的性能,拟合结果见图8。
图8
图8
m@Kaolin-LC/Ppy对Hg2+的等温吸附拟合
Fig.8
Fitting results of Hg2+ isothermal adsorption onto m@Kaolin-LC/Ppy
表3 Hg2+的等温吸附拟合数据
Table 3
| T/K | Langmuir模型 | Freundlich模型 | ||||
|---|---|---|---|---|---|---|
| Qm/(mg·g-1) | KL/(L·mg-1) | R2 | KF | 1/n | R2 | |
| 298 | 517.72 | 0.09 | 0.985 6 | 88.82 | 0.53 | 0.920 2 |
| 308 | 551.44 | 0.45 | 0.991 5 | 204.64 | 0.34 | 0.988 6 |
| 318 | 652.73 | 0.79 | 0.975 4 | 278.94 | 0.30 | 0.970 4 |
2.9 再生实验
通过对吸附Hg2+后的m@Kaolin-LC/Ppy进行再生实验,考察吸附剂的循环利用性能。利用0.1 mol/L的稀盐酸作为洗脱剂,将已经对Hg2+吸附饱和的m@Kaolin-LC/Ppy材料置于0.1 mol/L的稀盐酸溶液中,在常温下搅拌4 h,停止搅拌后利用铷磁铁将吸附剂m@Kaolin-LC/Ppy从水溶液中分离出来,再用去离子水洗涤数次后置于烘箱内烘干,而后再投入下一次使用。结果表明:经过5次的吸附-脱附循环之后,m@Kaolin-LC/Ppy对Hg2+的吸附容量为328.1 mg/g,与第1次的吸附结果相比仅仅下降了11.9%。因此,m@Kaolin-LC/Ppy具有较高的经济性。对于Hg2+再生液的深度处理,可以考虑当再生液中的Hg2+达到某一浓度时,采用浓缩或化学法,将其中的Hg2+回收利用。
2.10 机理分析
m@Kaolin-LC/Ppy吸附Hg2+前后的FT-IR和XPS见图9。
图9
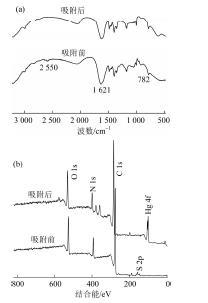
图9
m@Kaolin-LC/Ppy吸附Hg2+前后的FT-IR和XPS
Fig.9
FT-IR and XPS spectra of m@Kaolin-LC/Ppy before and after adsorption of Hg2+
由图9(a)的FT-IR谱图可知,原本处于782 cm-1的氨基特征峰在吸附Hg2+后发生了削弱,这种削弱可以归因于Ppy聚合物上的氨基基团与汞离子发生了络合作用,氨基与汞离子之间形成了稳定的金属络合物,即—N—Hg。另外,原本处于2 550 cm-1的—SH特征峰在吸附Hg2+后消失,这种现象出现的原因可以归因于巯基与汞离子之间进行了离子交换作用,与—SH形成结构稳定的—S—Hg,从而有效地去除了水溶液中的Hg2+。
由图9(b)可知,N 1s和S 2p的峰强变弱,特别是S 2p的峰;并且吸附后的XPS曲线在100 eV左右的位置上出现一个很强的Hg 4f特征峰,表明Hg2+由液相转移到了固相m@Kaolin-LC/Ppy的表面上,氨基与巯基参与了Hg2+的吸附过程,并且巯基的贡献度可能更大。
结合等温吸附与动力学研究可知,Hg2+是通过m@Kaolin-LC/Ppy上的氨基与巯基进行结合之后,完成了由液相到固相的空间变换,并且在该变换过程中,Hg2+与氨基和巯基之间通过某种化学键相结合,从而实现了对水中Hg2+的高效去除。
3 结论
本研究采用一种安全、高效和绿色的方法,成功合成出L-半胱氨酸与聚吡咯双官能团改性的磁性高岭土复合材料m@Kaolin-LC/Ppy。该磁性高岭土对Hg2+的吸附在pH=7时取得最佳吸附容量372.5 mg/g,吸附过程符合准二级动力学模型和Langmuir模型。吸附过程中,m@Kaolin-LC/Ppy上的氨基和巯基通过某种化学键参与了Hg2+的吸附。此外,m@Kaolin-LC/Ppy还具有良好的再生性、分散性和稳定性,是去除水中Hg2+的优良吸附剂。
参考文献
Preparation of ternary amino-functionalized magnetic nano-sized illite-smectite clay for adsorption of Pb(Ⅱ) ions in aqueous solution
[J].
Thiol functionalization of short channel SBA-15 through a safe,mild and facile method and application for the removal of mercury(Ⅱ)
[J].
硝酸镧改性文冠果活性炭对汞离子的吸附
[J].
Adsorption of Hg2+ on Xanthoceras sorbifolia bunge activated carbon modified by La(NO3)3·6H2O
[J].
Fe3O4磁性纳米氧化石墨烯制备及对汞(Ⅱ)的吸附
[J].
Synthesis of Fe3O4 magnetic graphene oxide nanocomposite and its adsorption for mercury(Ⅱ)
[J].
不同产地膨润土对汞(Ⅱ)离子吸附性能的研究
[J].
Comparative study on the adsorption properties of bentonite from different areas for mercury(Ⅱ) ions
[J].
巯基化多孔氧化硅纳米球及其对汞的吸附富集
[J].
Enrichment of mercury ions from aqueous solutions by thiol-modified porous silica nanospheres
[J].
螯合型聚氨酯微粒的制备及对Hg(Ⅱ)吸附行为
[J].
Preparation and adsorption behavior of chelated polyurethane particles of mercury ions
[J].
Efficient removal of naphthalene from aqueous solutions using a nanoporous Kaolin/Fe3O4 composite
[J].
Functionalized 2D clay derivative:Hybrid nanosheets with unique lead sorption behaviors and interface structure
[J].
Influence of acid activation of kaolinite and montmorillonite on adsorptive removal of Cd(Ⅱ) from water
[J].
Self-assembly of sponge-like Kaolin/chitosan/reduced graphene oxide composite hydrogels for adsorption of Cr(Ⅵ) and AYR
[J].
Comparison of sorption of Pb2+ and Cd2+ on Kaolinite clay and polyvinyl alcohol-modified Kaolinite clay
[J].
Di-and triethanolamine grafted kaolinites of different structural order as adsorbents of heavy metals
[J].
表面改性纳米高岭石材料的制备及其重金属离子吸附性能研究
[D].
Preparation of surface modified nano-kaolinite material and its adsorption properties of heavy metal ions
[D].
负载铬钴石墨烯基材料对汞(Ⅱ)的吸附性能研究
[J].
Study on the adsorption capacity for mercury(Ⅱ) with chromium/cobalt-doped graphene oxide materials
[J].
Removal of mercury by magnetic nanomaterial with bifunctional groups and core-shell structure:Synthesis,characterization and optimization of adsorption parameters
[J].
Synthesis of magnetic short-channel mesoporous silica SBA-15 modified with a polypyrrole/polyaniline copolymer for the removal of mercury ions from aqueous solution
[J].
Removal of Hg2+ with polypyrrole-functionalized Fe3O4/Kaolin:Synthesis,performance and optimization with response surface methodology
[J].
Design of l-cysteine functionalized UiO-66 MOFs for selective adsorption of Hg(Ⅱ) in aqueous medium
[J].
Adsorption of ibuprofen using cysteine-modified silane-coated magnetic nanomaterial
[J].
Adsorption of mercury(Ⅱ) with an Fe3O4 magnetic polypyrrole-graphene oxide nanocomposite
[J].
A mild and facile synthesis of amino functionalized CoFe2O4@SiO2 for Hg(Ⅱ) removal
[J].
Efficient removal of heavy metal ions by thiol-functionalized superparamagnetic carbon nanotubes
[J].
改性竹活性炭去除汞离子
[J].
Removal of mercury ion with modified bamboo activated carbon
[J].
Fabrication of ploydopamine-kaolin supported Ag nanoparticles as effective catalyst for rapid dye decoloration
[J].







 津公网安备 12010602120337号
津公网安备 12010602120337号