煤炭在我国能源结构中占首要地位,煤化工产业通过化学加工等方式,将煤炭转化为气、液、固燃料及多种化工产品。产业的不断深化发展保障了我国能源和化工原材料的需求,却也产生了大量的煤化工废水。煤化工废水色度高、成分复杂、可生化性差,此外还含有高浓度酚类、多环芳烃、杂环烃、氨氮、氰化物、硫化物等有毒有害污染物,属于典型的难降解工业废水〔1〕。随着行业废水排放标准的逐步提高,我国目前以“物化+生化”为主体的处理工艺已很难将煤化工废水处理至达标排放,对煤化工废水进行深度处理愈发必要。
1 材料与方法
1.1 实验材料
活性γ-Al2O3小球,粒径3~5 mm,购自上海麦克林生化科技有限公司;硝酸锰、硝酸镁、钛酸丁酯等试剂均为分析纯,购自阿拉丁试剂公司。煤化工废水取自内蒙古某煤企废水处理工艺中的生化池出水,废水pH=7.8,COD、BOD5、TOC、NH3-N分别为156.0、23.8、40.12、5.7 mg/L,UV254为1.25 cm-1。
1.2 实验方法
1.2.1 催化剂的制备和表征
采用浸渍法制备复合催化剂Mn-Ti-Mg/Al2O3。量取20 mL钛酸丁酯、5 mL浓硝酸、8 mL去离子水,依次在剧烈搅拌的条件下逐滴加入到100 mL无水乙醇中,形成TiO2溶胶。之后称取1.5 g硝酸锰、2.0 g硝酸镁溶解于10 mL无水乙醇中,再与TiO2溶胶混合。在上述混合液中加入10 g活性Al2O3小球,放入恒温振荡箱中于30 ℃、180 r/min振荡条件下浸渍24 h,之后取出Al2O3小球在65 ℃的干燥箱中烘烤12 h,再放入马弗炉中于550 ℃焙烧4 h得到复合催化剂Mn-Ti-Mg/Al2O3。
为了考察Mn-Ti-Mg/Al2O3复合催化剂的性能,另外还制备了Mn/Al2O3、Mg/Al2O3、Ti/Al2O3 3种单组分催化剂与之进行对比。称取1.5 g硝酸锰、2.0 g硝酸镁分别溶解于100 mL去离子中得到Mn/Al2O3、Mg/Al2O3催化剂的浸渍液,Ti/Al2O3催化剂的浸渍液为TiO2溶胶。之后参照Mn-Ti-Mg/Al2O3复合催化剂的制备过程,使各浸渍液与载体反应制备单组分催化剂。
采用场发射扫描电镜(蔡司,Supra 55)分析催化剂的表面形貌;采用物理吸附仪(BELSORP)测试催化剂的比表面积和平均孔径;采用X射线光电子能谱仪(Thermo ESCALAB 250XI)分析催化剂中金属元素的存在状态,键能的测量值参考C 1s能带(284.7 eV);采用Zeta电位仪(MALVERN,Nano ZS9)测试催化剂的等电点(pHzpc)。
1.2.2 臭氧催化氧化实验流程
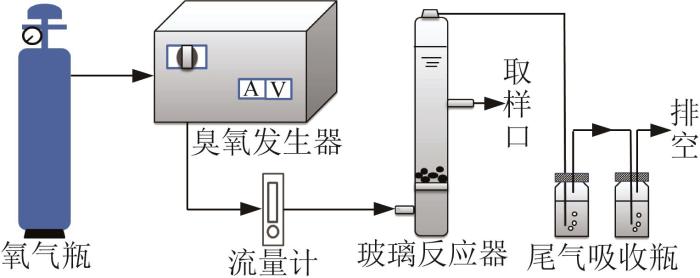
臭氧催化氧化实验装置如图1所示,将小球状催化剂放置于柱状玻璃反应器(高450 mm,内径47 mm)底部的砂芯板(平均孔径3~4 μm)上,反应器中加入500 mL煤化工废水。高纯氧气经臭氧发生器产生臭氧,由反应器中的砂芯板曝气释放到溶液中,臭氧尾气排出后被Na2S2O3溶液吸收。臭氧与氧气混合气体流量为0.1 L/min,通过调节发生器的电流改变臭氧气体浓度,反应过程中计时取样并检测水质。
图1
催化剂对臭氧的分解实验在恒温振荡箱中进行。将臭氧气体持续通入纯水中,30 min后得到饱和臭氧水溶液,分别量取200 mL饱和臭氧水溶液放入6个三角烧瓶中,再依次称取均为5 g的Al2O3、Mn/Al2O3、Mg/Al2O3、Ti/Al2O3、Mn-Ti-Mg/Al2O3分别放入5个三角烧瓶中,未放催化剂的三角烧瓶作为臭氧自分解的空白对照。将密封后的三角烧瓶放入恒温振荡箱振荡4 h(20 ℃,100 r/min),然后采用靛蓝法测定溶液中的臭氧浓度,根据臭氧浓度的降低比率衡量臭氧的分解情况。
1.2.3 水质分析方法
采用多参数水质分析仪(连华科技,5B-3C)测定煤化工废水的COD、NH3-N等指标;采用紫外可见分光光度计(莱伯泰科,Blue Star A)测定UV254;采用总有机碳分析仪(岛津,TOC-VCPH)测定废水TOC;采用酸度计(赛默飞世尔,410C-01A)检测废水的pH;采用稀释接种法测定废水BOD5;采用GC-MS分析废水中有机污染物。
煤化工废水GC-MS分析的预处理:(1)量取100 mL水样,用浓HCl调至pH≤2,加入10 mL二氯甲烷振荡萃取40 min,静置分层后取出有机相,重复萃取2次,合并有机相。(2)用0.1 mol/L NaOH溶液将上述萃取后水相调至pH≥11,加入二氯甲烷5 mL振荡萃取40 min,静置分层后取出有机相,重复萃取2次,合并有机相。(3)将上述有机相合并,过0.45 μm滤膜,用旋转蒸发仪(水浴60 ℃,真空度0.05 MPa)浓缩至近干,加入二氯甲烷定容至1 mL待测。
GC-MS(Agilent 6890/5973N)分析条件:采用石英毛细管柱(50 m×0.25 mm×0.25 μm),载气为氦气,流速1 mL/min,进样口温度250 ℃,柱温40 ℃,程序升温速度10 ℃/min,进样量 1 μL,分流比10∶1,传输线温度280 ℃,EI离子源,发射电子能量70 eV,扫描m/z范围45~500。
2 结果与讨论
2.1 复合催化剂的表征
2.1.1 SEM表征
对载体Al2O3,单组分催化剂Mn/Al2O3、Mg/Al2O3、Ti/Al2O3以及复合催化剂Mn-Ti-Mg/Al2O3的微观形貌进行SEM表征,结果见图2。
图2
由图2可知,Al2O3载体的表面并不平整,高低起伏并分布有沟壑、孔隙;与载体相比较,Mn/Al2O3和Mg/Al2O3催化剂的表面存在更多比较分散的细微颗粒,推测可能是负载于载体上的MnO2或MgO颗粒;Ti/Al2O3的表面更加致密化,并且存在非常明显的龟裂缝,推测可能是由于TiO2凝胶在载体表面包裹比较密实,因此在后续焙烧过程中形成了致密而分裂的表面形貌;Mn-Ti-Mg/Al2O3催化剂的表面形貌与Mn/Al2O3、Mg/Al2O3比较相似,有细小颗粒物质分散分布于载体上。
对单组分催化剂Mn/Al2O3、Mg/Al2O3、Ti/Al2O3以及复合催化剂Mn-Ti-Mg/Al2O3的组成进行EDS表征,结果见表1。
表1 催化剂的EDS分析
Table 1
| 催化剂 | 原子分数/% | ||||
|---|---|---|---|---|---|
| Al | O | Mn | Mg | Ti | |
| Mn/Al2O3 | 40.01 | 58.00 | 1.09 | — | — |
| Mg/Al2O3 | 41.20 | 57.67 | — | 1.13 | — |
| Ti/Al2O3 | 38.19 | 58.50 | — | — | 3.31 |
| Mn-Ti-Mg/Al2O3 | 40.18 | 57.80 | 0.23 | 0.74 | 1.05 |
如表1所示,对于3种单组分催化剂,Mn、Mg、Ti元素的原子分数分别为1.09%、1.13%、3.31%,复合催化剂中,Mn、Mg、Ti元素的原子分数分别为0.23%、0.74%、1.05%。由此可知,3种金属元素被成功负载于Al2O3载体上,但由于是表面负载,因此金属负载量不高。另外,复合催化剂中3种金属元素的负载量均低于单组分催化剂,说明载体表面的金属负载量是相对有限的。
2.1.2 XPS表征
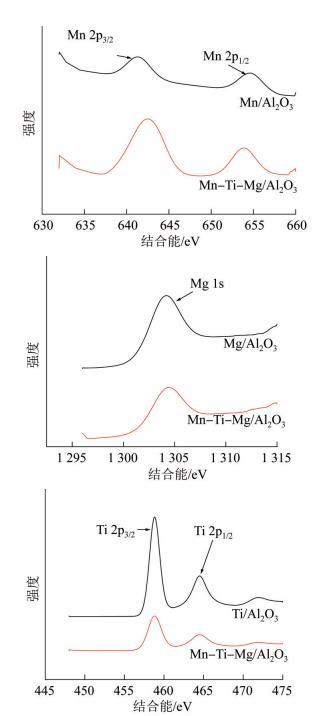
对复合催化剂Mn-Ti-Mg/Al2O3进行XPS表征,并与单组分催化剂Mn/Al2O3、Mg/Al2O3、Ti/Al2O3的XPS谱图进行对比,结果见图3。
图3
图3(a)所示为催化剂Mn/Al2O3和Mn-Ti-Mg/Al2O3的Mn 2p谱图。由图3(a)可知,2类催化剂的Mn 2p谱图均由2组峰组成,分别对应Mn 2p1/2和Mn 2p3/2的特征峰。根据文献〔11〕报道,Mn 2p3/2峰可对应Mn2+〔MnO或Mn(OH)2〕、Mn3+(Mn2O3或MnOOH)和Mn4+(MnO2),其中,MnO2中Mn 2p3/2标准电子结合能为642.1 eV。图3(a)中Mn/Al2O3和Mn-Ti-Mg/Al2O3催化剂中Mn 2p3/2的电子结合能分别为642.2、641.9 eV,非常接近MnO2的标准结合能,说明Mn元素在单组分催化剂和复合催化剂中主要以MnO2的形式存在。
2.1.3 BET分析和pHzpc测定
对载体Al2O3,单组分催化剂Mn/Al2O3、Mg/Al2O3、Ti/Al2O3以及复合催化剂Mn-Ti-Mg/Al2O3进行BET分析和pHzpc的测定,结果见表2。
表2 载体及催化剂的BET分析和pHzpc测定
Table 2
| 样品 | 比表面积/(m2·g-1) | 孔体积/(cm3·g-1) | 平均孔径/nm | pHzpc |
|---|---|---|---|---|
| Al2O3 | 327.22 | 0.49 | 5.72 | 7.3 |
| Mn/Al2O3 | 287.97 | 0.54 | 6.18 | 5.3 |
| Mg/Al2O3 | 222.09 | 0.45 | 6.81 | 5.2 |
| Ti/Al2O3 | 267.73 | 0.48 | 6.13 | 5.0 |
| Mn-Ti-Mg/Al2O3 | 292.45 | 0.59 | 6.77 | 6.6 |
由表2可知,活性Al2O3载体具有较大的比表面积,约为327.22 m2/g,但是负载金属活性成分之后,催化剂的比表面积均有所降低。这可能是因为在浸渍、焙烧过程中,载体的孔结构发生了变化,平均孔径增大,导致比表面积减小。3种单组分催化剂按照比表面积大小排序为Mn/Al2O3>Ti/Al2O3>Mg/Al2O3。复合催化剂Mn-Ti-Mg/Al2O3的比表面积约为292 m2/g,高于3种单组分催化剂的比表面积。
由表2还可知,活性Al2O3载体的等电点为7.3,与文献〔14〕报道比较相符。复合催化剂和3种单组分催化剂的等电点均明显低于Al2O3载体等电点,而复合催化剂的等电点略高于单组分催化剂等电点。显然,负载金属活性成分的过程使催化剂的等电点降低,究其原因,对于Mn/Al2O3和Ti/Al2O3来讲,一方面MnO2和TiO2的等电点分别位于2~5、4~6的范围〔15-16〕,明显低于Al2O3载体,因此它们负载于Al2O3表面导致催化剂等电点下降,另一方面催化剂等电点的变化可能与比表面积的降低有关,催化剂表面的金属原子可以吸附溶液中的水分子并使其发生解离,成为与金属原子配位的表面羟基和游离质子〔17〕,催化剂的比表面积降低,表面金属原子的数量减少,那么所生成的表面羟基和游离质子的数量也随之减少,固相表面倾向于在较低的pH条件下达到电荷平衡,因此催化剂的等电点较低。对于Mg/Al2O3来讲,MgO的等电点一般为9~11〔18〕,处于碱性范围。负载Mg元素应该使催化剂的等电点升高,但由于Mg/Al2O3的比表面积比Al2O3减小了32%,因此它的等电点也低于Al2O3载体。相对于Al2O3载体,Mn-Ti-Mg/Al2O3比表面积的减小幅度最低,它的等电点下降程度也最低。
2.2 复合催化剂的效能
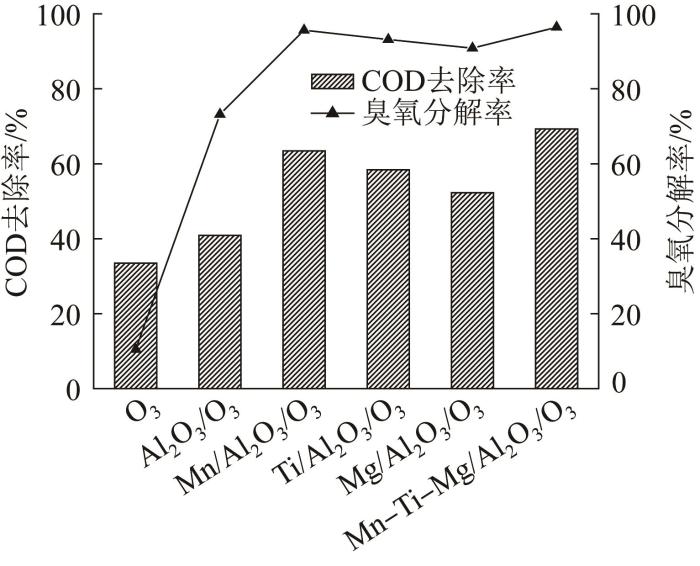
为考察复合催化剂催化臭氧氧化处理煤化工废水的效能,在温度22 ℃、初始pH 7.8、催化剂投加质量浓度10 g/L、O3流速1.0 mg/min、反应时间40 min条件下,分别采用单独O3、Al2O3/O3、Mn/Al2O3/O3、Ti/Al2O3/O3、Mg/Al2O3/O3、Mn-Ti-Mg/Al2O3/O3体系对煤化工废水进行处理,实验结果见图4。
图4
图4
各反应体系对煤化工废水的处理效能
Fig. 4
Treatment efficiency of various reaction systems for coal chemical wastewater
由图4可知,在反应时间为40 min时,单独O3氧化和Al2O3催化臭氧氧化过程分别使废水COD降低了33.47%、40.89%,说明Al2O3载体自身就有一定的催化能力。这是因为,一方面活性Al2O3小球在溶液中提供了较大的固相界面,臭氧分子在固液界面上的吸附、转移有利于促进臭氧气体溶于液相,另一方面,Al2O3表面的Lewis酸位也可能成为催化臭氧氧化反应的活性中心,促进臭氧分解并转化为自由基类物质〔19〕。Mn/Al2O3、Mg/Al2O3、Ti/Al2O3催化臭氧氧化过程分别使废水COD的去除率达到63.41%、52.58%、58.39%,3种单组分催化剂的活性均强于Al2O3载体催化活性,其中Mn/Al2O3的催化性能最优,其对废水COD的去除率比Al2O3载体相应的值提高了约22.52%。相比之下,复合催化剂的活性比单组分催化剂更强,Mn-Ti-Mg/Al2O3催化臭氧氧化过程使废水COD的去除率达到69.27%,体现出了3种金属活性成分的协同作用。
虽然Al2O3载体及几种金属负载催化剂具有较大的比表面积,但是它们对废水中有机污染物的吸附能力并不高,前期研究表明,催化剂的固相吸附作用对废水COD的去除率均低于4.00%,因此有机物的去除过程主要依赖于催化臭氧氧化反应。由图4(a)还可以看出,在没有催化剂存在的条件下,液相臭氧分子的自分解消耗率仅为10.46%;Al2O3载体可使臭氧的分解率达到73.19%,说明它对臭氧分子具有较强的分解作用;相比之下,复合催化剂和3种单组分催化剂对臭氧的分解能力更强,其中Mn-Ti-Mg/Al2O3使臭氧的分解率达到96.42%。对比表2和图4中的数据可以发现,催化剂的比表面积、对臭氧的分解能力、催化活性3者之间保持了良好的相关性。这意味着,金属负载催化剂的比表面积对它的催化性能具有显著影响。催化剂的比表面积越大、表面活性位越丰富,则它对臭氧的分解作用越强,可促使臭氧转化为更多的自由基类物质,从而更高效地降解废水中的有机污染物。
2.3 工艺参数的影响
为进一步探讨Mn-Ti-Mg/Al2O3复合催化剂催化臭氧氧化处理煤化工废水的影响因素,考察了催化剂投加量、O3流速、溶液初始pH对其催化效能的影响。因在实际工程中,为了控制处理成本,臭氧氧化反应的停留时间一般为30~60 min,故而本实验选择反应时间为40 min,以考察催化臭氧氧化过程在较短时间内的处理效果。
2.3.1 催化剂投加量
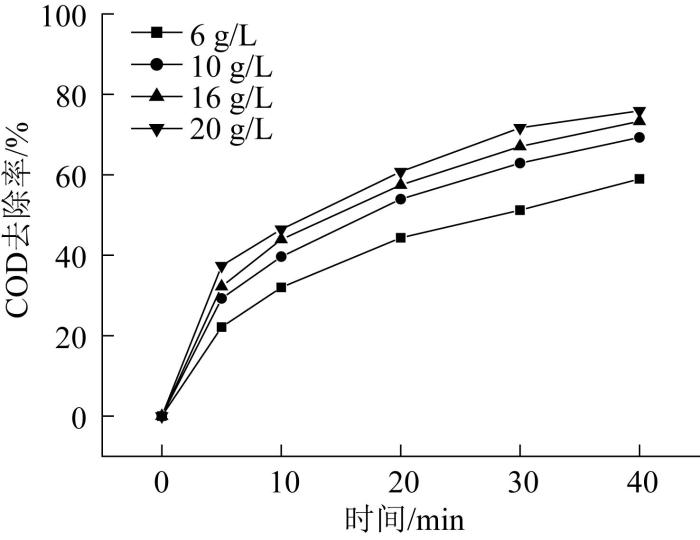
在温度22 ℃、初始pH 7.8、O3流速1.0 mg/min条件下,考察了Mn-Ti-Mg/Al2O3催化剂的投加量对煤化工废水处理效果的影响,实验结果见图5。
图5
由图5可知,随着催化剂投加量的增加,体系对废水COD的去除率逐渐提升,这说明催化臭氧氧化反应效率随着固相表面催化活性位的增多而提高。当催化剂投加质量浓度为20 g/L,在反应时间40 min时废水COD的去除率达到75.92%。此外,从图5还可以看出,当催化剂投加质量浓度由6 g/L增大至10 g/L时,废水COD的去除率提高了10.31%,继续提升催化剂投加质量浓度至20 g/L,COD去除率仅提高了6.65%,增幅明显减小。说明当催化剂投加量达到一定程度时,其就不再是催化臭氧氧化反应效率的限制因素,因此在工程应用中可以根据处理成本选择适宜的催化剂投加量。本研究中综合考虑反应经济性,后续实验采用的催化剂投加质量浓度为10 g/L。
2.3.2 臭氧流速
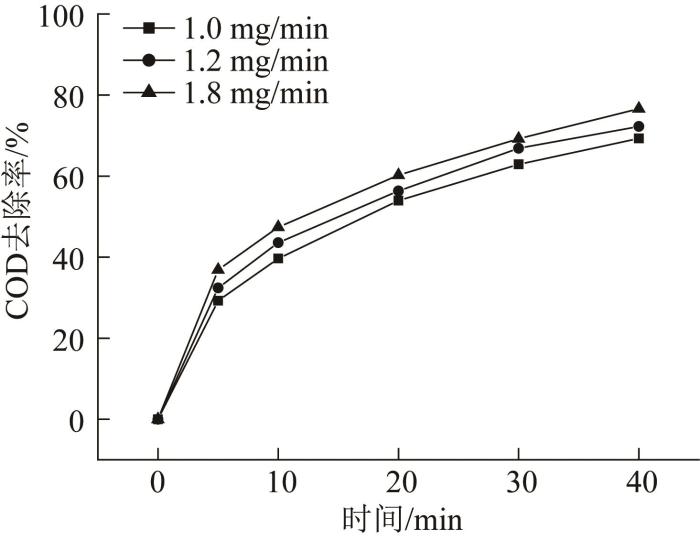
在温度22 ℃、初始pH 7.8、催化剂投加质量浓度10 g/L条件下,考察了臭氧流速对煤化工废水处理效果的影响,实验结果见图6。
图6
虽然增大臭氧流速可以提高废水处理效率,但综合考虑臭氧利用率等问题,后续实验中仍然选择臭氧流速为1.0 mg/min。
2.3.3 溶液初始pH
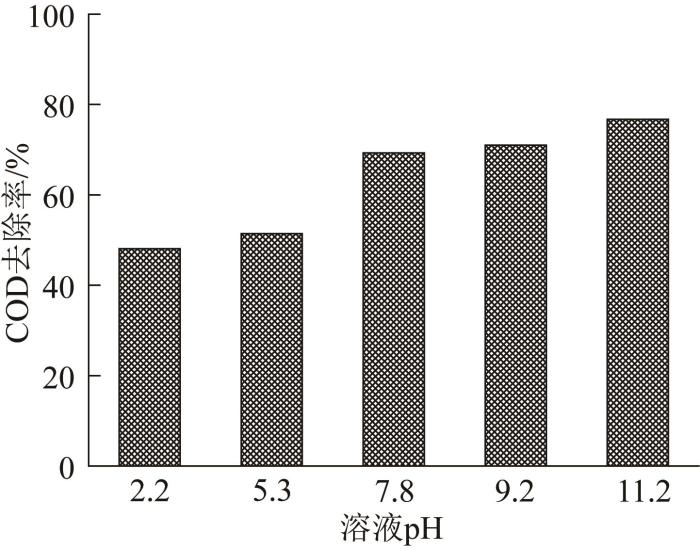
煤化工废水原水的初始pH约为7.8,采用酸、碱调节废水pH,考察溶液初始pH对煤化工废水处理效果的影响。由于极端酸、碱条件均不利于催化臭氧氧化反应的进行,因此确定pH的调节范围约为2~11,其它实验条件为温度22 ℃、催化剂投加质量浓度10 g/L、臭氧流速1.0 mg/min、反应时间40 min,实验结果见图7。
图7
图7
溶液初始pH对COD去除率的影响
Fig. 7
Effect of initial pH of solution on COD removal rate
由图7可知,废水COD的去除率随着溶液pH的升高而提高。当溶液初始pH为11.2时,废水COD去除率可以达到76.73%。由表2可知,Mn-Ti-Mg/Al2O3催化剂的等电点为6.6,催化剂表面在酸性溶液中显正电性,在中性和偏碱性条件下显负电性。根据实验结果推测,可能有2个原因导致有机物在碱性环境下更易被臭氧催化氧化降解:(1)催化剂显负电性的羟基化表面(Me-O-)具有较高的局部电荷密度,更易和亲电性的臭氧分子发生相互作用,导致臭氧更易被催化剂吸附、分解,进而产生强氧化性的自由基类物质;(2)随着溶液pH的升高,溶液中OH-的浓度不断增大,对臭氧分子的均相催化作用增强,促使臭氧分子转化为更多的羟基自由基,从而对有机物进行更彻底的氧化降解。
由图7还可以看出,煤化工废水由原水pH调至11.2过程中,COD的去除率虽有所提高,但提高幅度并不大,为节约成本,同时减少操作的复杂性,因此选择原水pH(7.8)为研究的最佳pH。
2.4 复合催化剂的稳定性
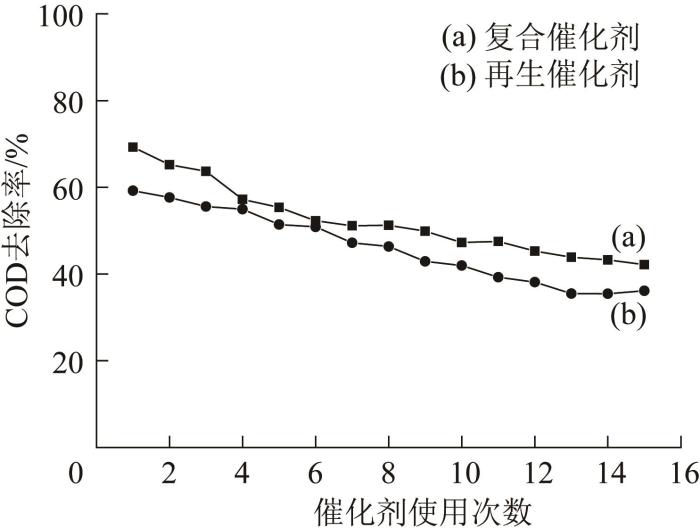
为考察复合催化剂的稳定性,在温度22 ℃、溶液初始pH 7.8、催化剂投加质量浓度10 g/L、臭氧流速1.0 mg/min、反应时间40 min条件下将Mn-Ti-Mg/Al2O3催化剂连续重复使用,煤化工废水COD去除率的变化情况见图8(a)。
图8
表3 使用前后复合催化剂的EDS
Table 3
| 原子分数/% | |||||
|---|---|---|---|---|---|
| Al | O | Mn | Mg | Ti | |
| 使用前 | 40.18 | 57.80 | 0.23 | 0.74 | 1.05 |
| 使用后 | 39.22 | 59.36 | 0.09 | 0.36 | 0.97 |
监测煤化工废水在催化臭氧氧化过程中pH的变化,发现处理后废水pH被大幅降低,说明废水中有较大量的酸性物质生成。废水环境由中性转至酸性是导致催化剂中Mn、Mg元素大量溶出的关键原因。因此,为了提高催化剂的稳定性,可在处理过程中适量投入无机碱以减轻酸性物质的影响。
2.5 煤化工废水的处理效果
2.5.1 常规指标分析
在温度22 ℃、溶液初始pH 7.8、催化剂投加质量浓度10 g/L、臭氧流速1.0 mg/min、反应时间40 min条件下,采用Mn-Ti-Mg/Al2O3催化剂催化臭氧氧化处理煤化工废水,处理后常规水质指标分析结果见表4。
表4 处理前后煤化工废水的常规水质指标
Table 4
| 项目 | 原水样 | 处理后水样 |
|---|---|---|
| COD/(mg·L-1) | 156.0 | 53.6 |
| BOD5/(mg·L-1) | 23.8 | — |
| UV254/cm-1 | 1.25 | 0.13 |
| TOC/(mg·L-1) | 40.12 | 20.07 |
| NH3-N/(mg·L-1) | 5.7 | 2.3 |
| pH | 7.8 | 3.4 |
如表4所示,煤化工废水进水COD平均值约为156.0 mg/L,经过催化臭氧氧化处理之后降低至53.6 mg/L,进水BOD5平均值约为23.8 mg/L,处理之后未检出,废水UV254和TOC的去除率分别达到90.01%、49.98%。以上4种有机污染指标的变化情况说明Mn-Ti-Mg/Al2O3催化臭氧氧化对煤化工废水具有良好的深度处理效果。另外,废水中的NH3-N含量较低,经过处理后得到更进一步的降低。根据炼焦化学工业污染物排放标准(GB 16171—2012),处理后废水的COD、BOD5、NH3-N等指标满足排放要求。
2.5.2 GC-MS分析
表5 煤化工废水原水中检出的有机物种类
Table 5
| 编号 | 分子式 | 有机物名称 | 有机物类别 |
|---|---|---|---|
| 1 | C6H6O | 苯酚 | 酚类 |
| 2 | C7H8O | 2-甲基苯酚 | 酚类 |
| 3 | C7H8O | 4-甲基苯酚 | 酚类 |
| 4 | C8H10O | 3-乙基苯酚 | 酚类 |
| 5 | C14H22O | 2,4-双(1,1-二甲基乙基)-苯酚 | 酚类 |
| 6 | C10H22 | 癸烷 | 烷烃类 |
| 7 | C13H28 | 2-甲基十二烷 | 烷烃类 |
| 8 | C15H32 | 十五烷 | 烷烃类 |
| 9 | C18H38 | 2,6,10-三甲基十五烷 | 烷烃类 |
| 10 | C16H34 | 十六烷 | 烷烃类 |
| 11 | C17H36 | 2-甲基十六烷 | 烷烃类 |
| 12 | C20H42 | 2,6,10,14-四甲基十六烷 | 烷烃类 |
| 13 | C17H36 | 十七烷 | 烷烃类 |
| 14 | C19H40 | 2,6-二甲基十七烷 | 烷烃类 |
| 15 | C18H38 | 十八烷 | 烷烃类 |
| 16 | C20H42 | 二十烷 | 烷烃类 |
| 17 | C6H8O3 | 3,4-二甲基-2,5-呋喃二酮 | 酮类 |
| 18 | C7H10O | 2,3-二甲基-2-环戊烯酮 | 酮类 |
| 19 | C9H6O3 | 4-甲基-1,3-异苯并呋喃二酮 | 酮类 |
| 20 | C10H10O4 | 邻苯二甲酸二甲酯 | 酯类 |
| 21 | C30H63O4P | 磷酸三癸基酯 | 酯类 |
| 22 | C16H22O4 | 邻苯二甲酸二异丁酯 | 酯类 |
| 23 | C8H16O2 | 辛酸 | 酸类 |
| 24 | C20H34O | 香叶基香叶醇 | 醇类 |
| 25 | C16H13N | N-苯基-1-萘胺 | 胺类 |
| 26 | C8H9N | N-苯亚甲基甲胺 | 胺类 |
| 27 | C10H14N2O3S | 4-(吗啉磺酰)苯胺 | 胺类 |
| 28 | C19H23NO | N-苄基-N-乙基-对异丙基苯甲酰胺 | 胺类 |
表6 Mn-Ti-Mg/Al2O3催化臭氧氧化处理后废水中有机物的种类
Table 6
| 编号 | 分子式 | 有机物名称 | 有机物类别 |
|---|---|---|---|
| 1 | C14H22O | 2,5-双(1,1-二甲基乙基)苯酚 | 酚类 |
| 2 | C10H20 | 1-甲基-2-丙基环己烷 | 烷烃类 |
| 3 | C13H28 | 2-甲基十二烷 | 烷烃类 |
| 4 | C18H38 | 2,6,10-三甲基十五烷 | 烷烃类 |
| 5 | C19H40 | 2,6,10,14-四甲基十五烷 | 烷烃类 |
| 6 | C12H14O4 | 邻苯二甲酸异丁酯 | 酯类 |
| 7 | C16H22O4 | 丁基仲-丁基邻苯二甲酸酯 | 酯类 |
| 8 | C24H38O4 | 邻苯二甲酸二异辛酯 | 酯类 |
| 9 | C19H38O2 | 14-甲基十五烷酸异丙酯 | 酯类 |
| 10 | C19H23NO | N-苄基-N-乙基对异丙基苯甲酰胺 | 胺类 |
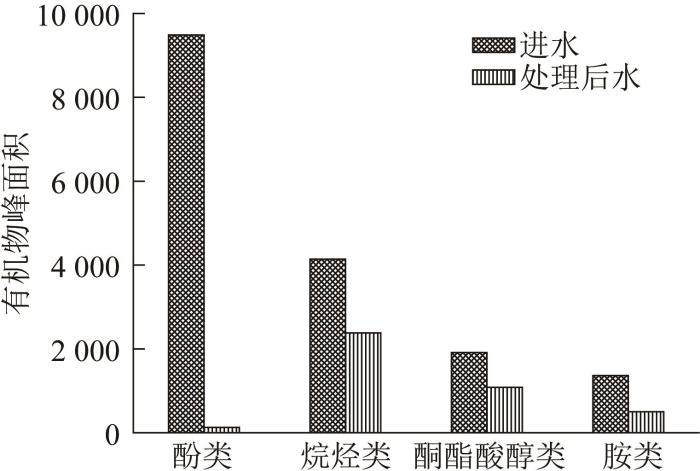
由表5可以看出,煤化工废水中共检出28种有机污染物,其中包含5种酚类物质、11种烷烃类物质、8种酮酯酸醇类物质和4种胺类物质。GC-MS谱图中有机物的峰面积可以在一定程度上反映有机物的含量,因此可以得出结论,煤化工废水中的有机污染物以酚类、烷烃类、酮酯酸醇类和胺类等物质为主。经过Mn-Ti-Mg/Al2O3催化臭氧氧化处理之后,废水中检出有机物的种类数降低为10种,比进水减少了18种。如表6所示,废水中酚类减少了4种,烷烃类减少了7种,酮酯酸醇类减少了4种,胺类减少了3种。有机物的总峰面积降低了75.78%,其中酚类、烷烃类、酮酯酸醇类、胺类的峰面积分别降低了98.65%、42.51%、43.50%、75.78%(如图9所示)。可以看出,复合催化剂对废水中的各类有机污染物均有良好的催化臭氧氧化降解效能,对酚类、胺类的催化降解效果尤其突出。
图9
图9
废水GC-MS图谱中有机物峰面积的变化情况
Fig. 9
Variation of peak area of organic matters in GC-MS spectra
3 结论
(1)采用浸渍法制备复合金属催化剂Mn-Ti-Mg/Al2O3,并对煤化工废水进行催化臭氧氧化降解,可使废水COD的去除率达到69.27%,分别比单独臭氧氧化、Al2O3催化臭氧氧化效果提高了35.80%、28.38%。Mn-Ti-Mg/Al2O3的催化活性明显强于单组分催化剂,说明3种金属复合具有协同催化作用。催化剂的比表面积、分解臭氧的能力与其催化活性之间存在良好的相关性。
(2)提高催化剂投加量和臭氧流速有助于提高对煤化工废水的处理效果,废水在碱性条件下的处理效率高于在中性和酸性条件下的处理效率。Mn-Ti-Mg/Al2O3催化剂在使用过程中会出现金属活性成分溶出现象,其中Mn、Mg元素流失比较严重,Ti元素相对负载得比较牢固。
(3)经过Mn-Ti-Mg/Al2O3催化臭氧氧化处理之后,废水的COD、BOD5、NH3-N等指标满足炼焦化学工业污染物排放标准(GB 16171—2012),GC-MS检出的有机物种类数由28种降低至10种,且Mn-Ti-Mg/Al2O3催化臭氧氧化对酚类和胺类的去除效果非常显著。
参考文献
煤化工废水难降解有机物的处理技术研究进展
[J].
Research progress in the treatment of refractory organic compounds in coal-chemical industrial wastewater
[J].
催化臭氧化法处理煤化工废水的研究进展
[J].
Research progress in treating coal chemical effluent by catalytic ozonation
[J].
Reactive oxygen species and catalytic active sites in heterogeneous catalytic ozonation for water purification
[J].
Revisiting the role of reactive oxygen species for pollutant abatement during catalytic ozonation:The probe approach versus the scavenger approach
[J].
改性ZSM-5分子筛催化臭氧氧化含硅间甲酚
[J].
Catalytic ozonation silicon-containing m-cresol by modified ZSM-5 molecular sieve
[J].
臭氧催化氧化降解煤化工生化进水有机物的实验及机理
[J].
Experimental and mechanism studies on degradation of the organics in biochemical influent of coal chemical industry by ozone catalytic oxidation
[J].
臭氧催化氧化降解煤化工高盐废水有机物的机理
[J].
Catalytic oxidation mechanism of organics degradation by ozone in highsalt wastewater of coal chemical industry
[J].
High surface area mesoporous nanocast LaMO3(M=Mn,Fe) perovskites for efficient catalytic ozonation and an insight into probable catalytic mechanism
[J].
Enhanced mineralization of pharmaceuticals by surface oxidation over mesoporous γ-Ti-Al2O3 suspension with ozone
[J].
纳米MgO催化臭氧氧化深度处理煤化工废水
[J].
Nano-MgO catalytic ozonation for advanced treatment of coal gasification wastewater
[J].
Mn-Fe-Mg-Ce loaded Al2O3 catalyzed ozonation for mineralization of refractory organic chemicals in petroleum refinery wastewater
[J].
The degradation and mineralization of catechol using ozonation catalyzed with MgO/GAC composite in a fluidized bed reactor
[J].
金属掺杂改性TiO2催化臭氧氧化水中有机污染物研究
[D].
Catalytic ozonation by metal doped-TiO2 for degradation of organic pollutants in water
[D].
载铈活性氧化铝对水中氟离子的吸附特性研究
[D].
Adsorption of fluoride ions from aqueous solutions by Ce(Ⅲ)-impregnated activated alumina
[D].
锰氧化物改性沸石(MOCZ)对罗丹明B和4-氯苯酚的吸附研究
[D].
Study of biosorption of rhodamine B and p-chlorophenol from the aqueous solutions by manganese oxide coated zeolite(MOCZ)
[D].
不同UV工艺中阿特拉津的降解效果与机理研究
[J].
Degradation effect and mechanism of atrazine in UV-based oxidation processes
[J].
FeOOH catalytic ozonation of oxalic acid and the effect of phosphate binding on its catalytic activity
[J].
Development of nanofluids for the inhibition of formation damage caused by fines migration:Effect of the interaction of quaternary amine(CTAB) and MgO nanoparticles
[J].
Mechanism of catalytic ozonation in Fe₂O₃/Al₂O₃@SBA-15 aqueous suspension for destruction of ibuprofen
[J].
臭氧催化氧化处理造纸厂二级生物处理出水
[J].
Ozone catalytic advanced oxidation technology for secondary effluent of paper-making mill
[J].






 津公网安备 12010602120337号
津公网安备 12010602120337号