高铁酸盐作为一种环保型绿色水处理药剂,具有很强的氧化能力〔4〕,氧化还原电位甚至高于臭氧等一些强氧化剂。高铁酸盐经反应后生成的Fe3+具有很好的吸附性,可以通过更深层次的强化吸附去除水体中污染物。本研究对高铁酸盐的实际应用现状进行综述。
1 高铁酸盐的制备方法
1.1 湿式氧化法
1.2 电解法
电解法即电化学氧化法,此法以铁单质或铁化合物为电极,在一定浓度NaOH溶液中,利用电氧化制得高铁酸盐,温度对其氧化效率有一定的影响,若温度发生变化,高铁酸盐的分解速率也会产生相应的改变。为解决这个问题,有研究者采用Pt或掺杂B的材料做阳极,以熔融态碱做相应的电解质,降低了制备过程中温度的影响〔7〕。
1.3 高温氧化法
高温氧化法又称干式氧化法,该法是将铁氧化物和硝酸钾进行混合,然后加热到1 100 ℃煅烧制得高铁酸钾,但是此法得到的高铁酸钾纯度很低〔5〕,产物中铁的价态也不唯一,且易吸收水分,因此不太适用于制备纯度很高的高铁酸盐。
2 高铁酸盐应用于单一重金属的去除
2.1 高铁酸盐对铅的去除研究
铅是一种具有毒性的元素,生物体内若含铅较高,就会造成铅中毒〔8〕。高铁酸盐对铅的去除,主要依靠反应所生成Fe(OH)3的吸附作用,而且在碱性条件下,铅会以络合态存在,最终形成Pb(OH)2沉淀,从而将其从水中去除。何文丽等〔9〕对高铁酸钾处理模拟高浓度含铅矿井水中的铅进行了研究,结果表明,铅的去除率随pH的改变而变化,pH在8~10范围内,铅去除率达到95%,去除效果好。苑志华等〔10〕利用高铁酸钾处理模拟重金属废水,研究表明,pH是影响模拟水样中铅去除率的一个重要因素,不同pH条件下去除率有所不同,但是在一定投加量下,高铁酸钾能够使水中的铅达到国家排放标准。如上所述,高铁酸钾对模拟的含铅废水具有较好的去除效果,但是面对成分复杂、污染物浓度各异的实际水体,其具体去除效果和机理还需深入研究。
2.2 高铁酸盐对铬的去除研究
2.3 高铁酸盐对类金属砷的去除研究
砷广泛分布于自然界,具有生物毒性,常称其为类金属。砷的化合物一般分为有机砷和无机砷,其中无机砷具有较强毒性〔13〕。研究表明在生物体内砷的价态可互相转变〔14〕;砷在水体中主要以亚砷酸离子和砷酸离子两种形态存在,在一定条件下,亚砷酸会转化成砷酸。对砷的去除方法一般有化学沉淀法、铁氧化法、膜法等,主要是经过反应生成难溶的砷化物沉淀,或者通过高铁酸钾反应生成Fe(Ⅲ)对其进行吸附絮凝,最终通过固液分离去除。As(Ⅲ)在水中的存在形式并不单一,且Fe(Ⅵ)被还原的过程中存在Fe(Ⅴ)、Fe(Ⅳ)等中间产物,所以FeO42-对As(Ⅲ)的氧化可能较为复杂。M. Fan等〔15〕以H2AsO3-和HAsO32-为例提出2种可能存在的反应,反应方程见式(1)~式(2)。
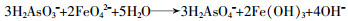
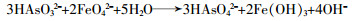
总反应见式(3)。
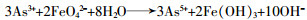
Y. Lee等〔16〕对pH=7时Fe(Ⅵ)、As(Ⅲ)和As(Ⅴ)的主要存在形式进行分析,探究Fe(Ⅵ)氧化As(Ⅲ)的机理,结果表明,高铁酸盐对As(Ⅲ)的氧化过程实际上是氧原子的转移机制,由于氧原子的转移,最终使As(Ⅲ)被氧化为As(Ⅴ),同时Fe(Ⅵ)被还原为Fe(Ⅲ)。
Fe(Ⅵ)可以通过单电子转移过程氧化底物,产生Fe(Ⅴ)和自由基。然而,这种自由基的产生仅在Fe(Ⅵ)与有机分子(如苯酚、苯胺)的反应中可以观察到。Y. Lee等〔16〕提出由Fe(Ⅵ)对As(Ⅲ)氧化的双电子转移过程也得到了实验数据的验证,与关于Fe(Ⅵ)氧化其他无机含氧阴离子(SO32-、SeO32-)的研究一致。其中,双电子转移过程中包含的从FeO42-到SO32-的氧传递也可由同位素18O示踪实验证明〔17〕。但Fe(Ⅵ)对As(Ⅲ)的氧化是通过氧转移的双电子转移这一理论仍缺少实验数据验证。孙玉林〔18〕对废水中As(Ⅴ)的处理研究表明,pH为2.0~3.0时,As(Ⅴ)的去除率最高达到98.0%。蒋国民〔19〕对高浓度含砷废水进行了深度处理研究,结果表明,在一定工艺条件下,利用高铁酸盐处理后砷的出水浓度可达到国家标准。
3 高铁酸盐对多种复杂重金属的去除
3.1 高铁酸盐同时去除多种重金属
废水中的重金属离子主要由化工、冶炼等企业排入水体,不同企业排出的重金属种类、含量及各自的存在形态也不同。待处理废水中同时含有两种或两种以上重金属离子时高铁酸盐的去除效果是否受到影响也是一个值得探究的问题。M. Lim等〔20〕利用高铁酸钾同时去除河水中的重金属(Cu、Mn和Zn),结果表明,高铁酸钾对重金属的去除过程中,其氧化絮凝作用非常显著,且去除效率与pH相关,而总体温度对高铁酸盐和重金属之间的反应没有任何影响。王颖馨等〔21〕利用K2FeO4有效地处理了砷、铅复合污染,在K2FeO4投加量为24 mg/L时,对砷、铅的去除率分别可达到99.30%、100%,且溶液pH小于7时,同时去除砷、铅效果较好。但与单独污染相比,低K2FeO4投加量下砷与铅存在明显的竞争关系,且K2FeO4的投加量并不是越多越好,这可能与吸附容量有关。B. Lan等〔22〕将高铁酸钾用于处理砷和锑的组合污染,As(Ⅲ)和Sb(Ⅲ)被氧化后通过Fe(Ⅵ)的还原产物从溶液中吸附分离。结果表明,在双溶质溶液中2种元素的吸附速率较单溶质溶液有显著提高,证明砷和锑之间存在协同作用。
3.2 高铁酸盐去除重金属络合物
由于大量工业废水排入水环境中,导致产生重金属络合污染物,该络合污染物成分极其复杂,一般情况下,水体中都是游离态重金属、络合态重金属以及有机络合物共存。有一些研究利用Fe(Ⅵ)对这种混合体系进行处理,同样得到了较为理想的效果。
L. Sailo等〔23〕将高铁酸盐(Ⅵ)用于处理被金属(Ⅱ)-络合物〔即Cu(Ⅱ)-NTA、Cu(Ⅱ)-EDTA和Cd(Ⅱ)-EDTA〕污染的废水,提出在高铁酸盐(Ⅵ)的存在下,酸性条件有利于金属(Ⅱ)-络合物的降解/矿化,且提高pH至12.0的条件下可有效地同时去除游离铜或镉。同样,Cu(Ⅱ)-IDA、Zn(Ⅱ)-IDA、Cd(Ⅱ)-IDA和Ni(Ⅱ)-IDA等水中的金属-亚氨基二乙酸络合物也可先通过降低pH来提高Fe(Ⅵ)对M(Ⅱ)-IDA的解络合速率,在总有机碳(TOC)显著降低且获得游离态金属离子的情况下再将Fe(Ⅵ)处理的样品在pH=12.0时,利用Fe(Ⅵ)的氧化作用进一步去除水中的金属离子〔24-25〕。S. M. Lee等〔26〕在CN-Cu、CN-Ni或CN-Cu-Ni的混合/络合体系中使用高铁酸盐(Ⅵ)用于氰化物的氧化和同时去除铜或镍。结果表明对于CN-Cu和CN-Ni系统,在pH=10.0时CN可以发生快速且有效的氧化,在pH=13.0时铜几乎完全被去除,在CN-Cu-Ni体系中也可观察到类似的结果,其中通过用Fe(Ⅵ)处理实现CN和Cu的降解,并且部分地除去Ni。
4 高铁酸盐应用于其他污染物的处理
目前,富营养化问题也极为严重。通过大量研究总结发现,磷是造成多数水体富营养化的关键因素。目前单独依靠生物法除磷很难满足要求。因此,利用化学方法辅助除磷已势在必行。利用高铁酸盐除磷是利用其很高的氧化性来氧化含磷化合物,形成难溶磷酸盐沉淀物,在反应过程中,会生成一些复杂的中间络合产物,起到吸附和网捕作用,形成沉淀,从而得到去除。吴晓荣〔27〕通过研究得到了最佳的除磷工艺条件,利用高铁酸钾联合聚合硫酸铁在相应的工艺条件下对磷的去除率可以达到80%左右,达到国家城镇污水排放标准的一级A标准。
高铁酸钾在去除有机物、抗生素以及有毒物质等方面也有很好的效果。Jing Zhang等〔28〕研究表明,高铁酸盐和亚硫酸盐的联合,会提高反应的活性,快速去除有机物。Mingbao Feng〔29〕对比了吩嗪硫酸甲酯(PMS)和Fe(Ⅵ)单独对抗生素的去除效果,还通过对比二者不同比例的混合去除抗生素的效果发现,二者协同效果更好。V. K. Sharma等〔30〕的研究表明,高铁酸盐对含氮、含硫污染物、抗生素、有毒物质以及重金属的去除具有显著效果。S. N. Malik等〔31〕的研究结果表明单独用高铁酸盐处理色度、COD、有毒物质效果不明显,但是,将高铁酸盐和硫酸亚铁按照一定比例混合,可以提高对色度、COD、有毒物质的去除率,分别为96.5%、83%、75%。
还有研究证明高铁酸盐也可应用于水处理工艺的优化中,C. Wu等〔32〕提出500 mg/L的K2FeO4能够有效氧化分解污泥,提高污泥脱水性能和污泥生物降解性。E. Gombos等〔33〕在细菌100%灭活的情况下分别用低浓度和较高浓度的Fe(Ⅵ)对二级处理后的污水进行净化,结果表明,可以降低生物处理废水中的TOC,高铁酸钾氧化有机物的机理得到了更深层次的探讨,在一定条件下Ag+的存在可以促进反应过程中·OH的产生,进一步强化了高铁酸钾氧化有机物的效果,其对芳香化合物邻氯苯酚同样具有处理速度快、处理率高等优势,并且通过合理利用反应过程中不同价态Fe的化学特性,能极大提高污水处理厂的处理效率〔34-36〕。综上所述,高铁酸盐这种具有独特性质的处理药剂将会有更好的发展前景,具有高效的实用价值。
5 结论
高铁酸盐在污水深度处理中的应用研究远不止上述几项,重金属污染问题日趋严峻,其造成的后果也极其严重。高铁酸盐独特的优势在于极强的氧化性和良好的混凝效果。高铁酸盐在降解污染物的过程中,通过单电子和双电子转移的机制,Fe(Ⅵ)最终被还原为Fe(Ⅲ)或Fe(Ⅱ),反应过程中,中间价态还会产生复杂络合物,产生吸附、电中和以及网捕等正向效果,其具体的反应机理途径与处理污染物本身的化学特性相关。高铁酸盐的处理效果与溶液pH的高低密不可分,因此在利用高铁酸盐处理污染物时,pH的控制也至关重要。
高铁酸盐在污水深度处理中具有很高的实际应用价值,然而在实际的生产和制备过程中,也存在着很多问题,比如其稳定性以及高昂的成本限制了大规模的制备和应用,但随着高铁酸盐的合成方法不断优化、日渐成熟,这已不能成为阻碍其广泛应用的因素。虽然目前利用高铁酸盐处理水中重金属还处于实验室的研究阶段,但是近年来这个方法已经得到了广泛的认可与关注。随着对多项污染物处理条件和降解机理研究的不断深入、不断完善,将很快体现出高效的应用价值。
参考文献
Selected elemental composition of the muscle tissue of three species of fish:tilapia niltica cirrhina ntrigala and clarius batrachus from fresh water Dhanmondi Lake in Bangledesh
[J].DOI:10.1016/j.foodchem.2004.10.021 [本文引用: 1]
Advances in the development and application of ferrate(Ⅵ) for water and wastewater treatment
[J].DOI:10.1002/jctb.2014.89.issue-2 [本文引用: 1]
高铁酸盐:一种绿色的多功能水处理剂
[J].DOI:10.11944/j.issn.1000-0518.2016.11.160337 [本文引用: 2]
高铁酸盐的制备、性质及在水处理中的应用
[J].DOI:10.3969/j.issn.1005-2992.2015.04.006 [本文引用: 1]
Research progress in the electrochemical synthesis of Ferrate(Ⅵ)
[J].DOI:10.1016/j.electacta.2008.11.034 [本文引用: 1]
水环境中铬的存在形态及迁移转化规律
[J].DOI:10.3969/j.issn.1001-425X.2006.08.001 [本文引用: 1]
Preliminary studies of the oxidation of Arsenic(Ⅲ) by potassium ferrate
[J].
Arsenic(Ⅲ) oxidation by Iron(Ⅵ)(Ferrate) and subsequent removal of Arsenic(Ⅴ) by Iron(Ⅲ) coagulation
[J].
Mechanism of isotopic oxygen exchange and reduction of Ferrate(Ⅵ) ion(FeO42-)
[J].
Effectiveness of potassium ferrate(K2FeO4) for simultaneous removal of heavy metals and natural organic matters from river water
[J].
高铁酸钾的制备及其对水中As(Ⅲ)、Pb(Ⅱ)的去除效能研究
[J].
Aqueous Arsenic(As) and antimony (Sb) removal by potassium ferrate
[J].DOI:10.1016/j.cej.2016.02.019 [本文引用: 1]
Efficient use of Ferrate(Ⅵ) for the remediation of wastewater contaminated with metal complexes
[J].DOI:10.4491/eer.2014.079 [本文引用: 1]
Ferrate(Ⅵ) in wastewater treatment contaminated with metal(Ⅱ)-iminodiacetic acid complexed species
[J].
Remediation of aquatic environment contaminated with the iminodiacetic acid metal complexes using ferrate(Ⅵ)
[J].
Application of ferrate(Ⅵ) in the treatment of industrial wastes containing metal-complexed cyanides:a green treatment
[J].DOI:10.1016/S1001-0742(08)62425-0 [本文引用: 1]
Rapid removal of organic pollutants by activation sulfite with ferrate
[J].DOI:10.1016/j.chemosphere.2017.07.102 [本文引用: 1]
Synergistic effect of aqueous removal of fluoroquinolones by a combined use of peroxymonosulfate and ferrate(Ⅵ)
[J].DOI:10.1016/j.chemosphere.2017.03.008 [本文引用: 1]
Ferrates:greener oxidants with multimodal action in water treatment technologies
[J].DOI:10.1021/ar5004219 [本文引用: 1]
Comparison of coagulation, ozone and ferrate treatment processes for color, COD and toxicity removal from complex textile wastewater
[J].
Effects of potassium ferrate oxidation on sludge disintegration, dewaterability and anaerobic biodegradation
[J].
Removal of organic matters in wastewater treatment by ferrate(Ⅵ)-technology
[J].
高铁酸钾氧化处理废水中邻氯苯酚的研究
[J].DOI:10.3969/j.issn.1009-2455.2018.02.007
An overview on production and application of ferrate(Ⅵ) for chemical oxidation, coagulation and disinfection of water and wastewater
[J].DOI:10.1016/j.jece.2017.03.025 [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号