本研究依据硫酸钠、氯化钠和硝酸钠的溶解度曲线和Na+//Cl-、SO42--H2O三元水盐体系相图〔6〕制定了详细的分盐结晶实验方案,通过对高盐废水中的杂盐进行分质结晶,实现了硫酸钠、氯化钠和硝酸钠的分离,产品达到工业标准。
1 实验部分
1.1 实验原料
某煤制油外排废水,先进行预处理(生物处理、氧化降COD、软化过滤、反渗透等),将盐质量分数提高到15%以上,得到浓盐水,其组成见表1。
1.2 实验原理
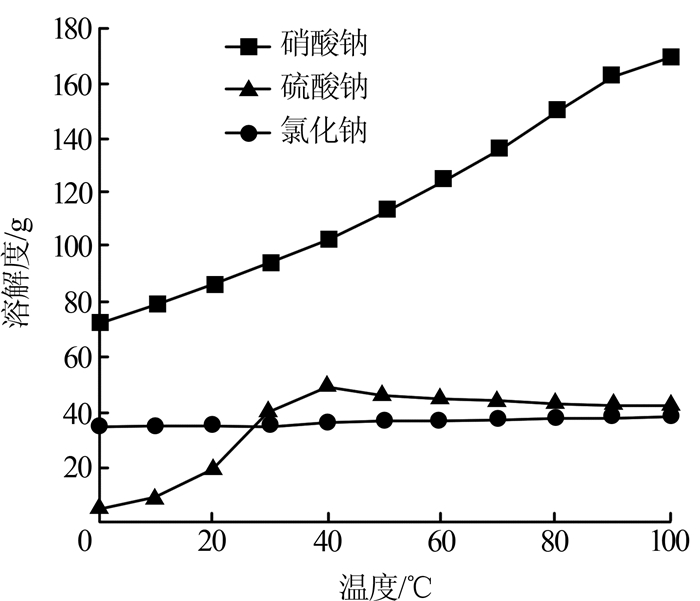
图1
由图1可知,硝酸钠的溶解度远高于硫酸钠和氯化钠,并且随温度的上升而显著增加,而且硝酸钠含量低,在蒸发过程中,先结晶的必然是硫酸钠和氯化钠,因此实验方案中先对硫酸钠和氯化钠进行分离。
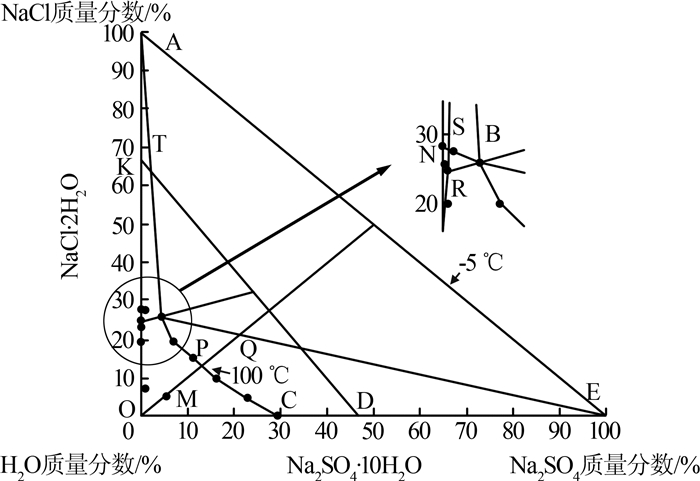
图2
其中NBC为100 ℃时氯化钠、硫酸钠饱和溶解度曲线,BAN是氯化钠结晶区,BCE是硫酸钠结晶区,ABE是氯化钠、硫酸钠的混合结晶区。M点为废水初始浓度点,首先进行蒸发浓缩,系统沿OM到达P点,进入硫酸钠结晶区,控制一次蒸发率(蒸发量与废水质量比)使蒸发点不超过Q点,结晶析出硫酸钠,液相点到达B点。在B点时降温至-5 ℃,析出十水硫酸钠和二水氯化钠晶体,此时液相点落在R点上,再蒸发浓缩,进入氯化钠结晶区,液相点落在100 ℃饱和溶解度曲线S点上,控制二次蒸发率(蒸发量与母液质量比)使蒸发点不超过T点,析出氯化钠结晶,从而实现硫酸钠和氯化钠的分离。
1.3 分盐结晶工艺方案
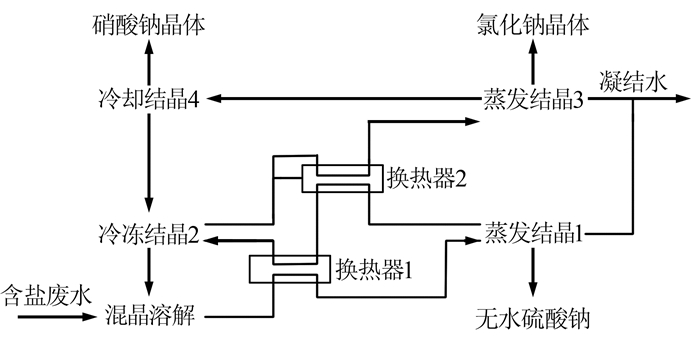
图3
2 结果与讨论
2.1 一次蒸发率对硫酸钠结晶纯度的影响
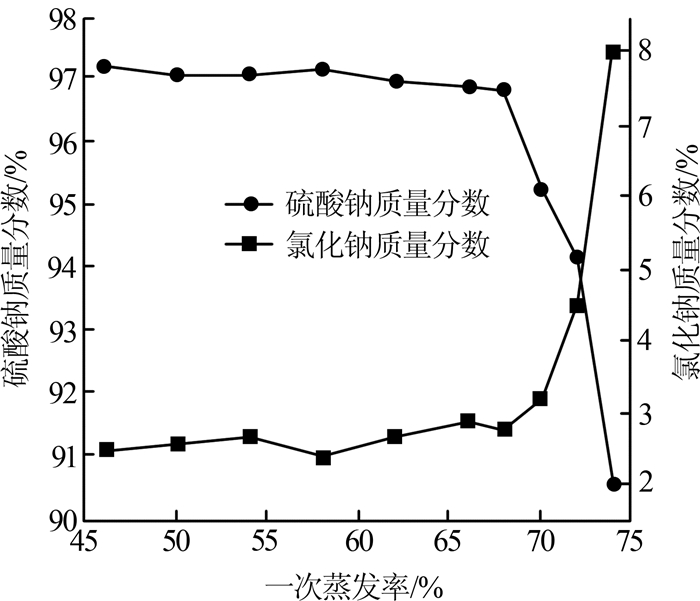
对一次蒸发析出的结晶趁热过滤、烘干,并分析硫酸钠纯度,考察一次蒸发率对硫酸钠结晶纯度的影响,结果见图4。
图4
2.2 冷冻温度对母液的影响
对一次蒸发过滤后的高温滤液进行降温冷冻,因硫酸钠的溶解度随温度下降而急剧降低,冷冻会析出晶体,此时母液的组成发生改变,硫酸钠质量分数进一步降低,二次蒸发进入氯化钠结晶区,保证了氯化钠的纯度,考察不同冷冻温度对母液的影响,结果见表2。
2.3 二次蒸发率对氯化钠结晶纯度的影响
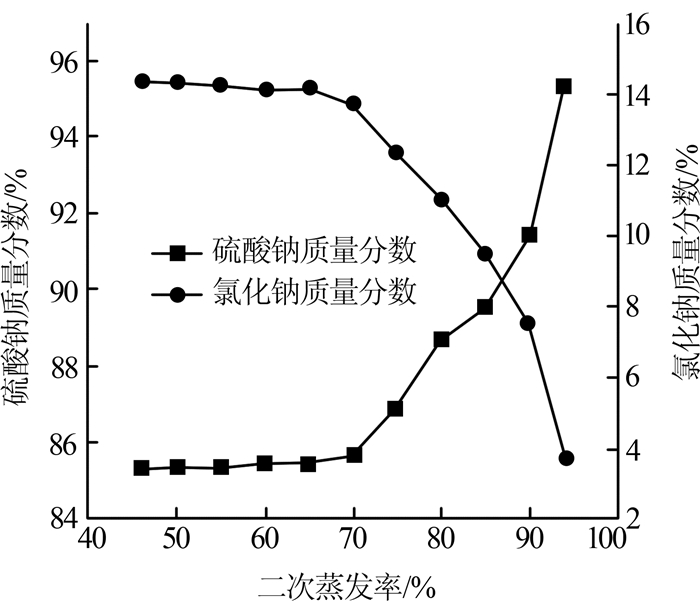
对二次蒸发析出的结晶趁热过滤、烘干,并分析氯化钠纯度,考察二次蒸发率对氯化钠结晶纯度的影响,结果见图5。
图5
2.4 硝酸钠的分离
实验过程中,二次蒸发结晶后的滤液中含微量硫酸钠、氯化钠和大量的硝酸钠,考虑到硝酸钠的溶解度随温度的变化比较大,将二次蒸发结晶后的滤液再次降温,可大量析出硝酸钠晶体。为此,对二次蒸发结晶后的滤液再一次冷却,得到结晶产品,晶体组成分析见表3。
表3 冷却温度对晶体组成的影响
| 冷却温度/℃ | 硝酸钠 /% | 硫酸钠 /% | 氯化钠 质量分数/% |
| 20 | 98.7 | 0.4 | 0.9 |
| 10 | 98.4 | 0.5 | 1.1 |
| 5 | 98.0 | 0.6 | 1.4 |
| 0 | 97.8 | 0.7 | 1.6 |
由表3可知,0~20 ℃下冷却对结晶产品的组成影响不大,结晶所得的硝酸钠纯度达到98%,达到了GB/T 4553—2002工业硝酸钠合格品的标准,基本能够满足工业品要求。
硝酸钠结晶后的滤液组成见表4。
表4 结晶后的滤液组成
| 冷却温度/℃ | 硝酸钠 质量分数/% | 硫酸钠 质量分数/% | 氯化钠 质量分数/% |
| 20 | 28.8 | 2.2 | 14.2 |
| 10 | 27.6 | 1.8 | 15.6 |
| 5 | 30.6 | 2.8 | 13.6 |
| 0 | 31.2 | 1.8 | 14.6 |
由表5可知,硝酸钠结晶后的滤液返回低温冷冻阶段进行二次蒸发,对晶体组成影响不大,分盐结晶出的产品都达到了工业品标准。
3 结论
(1)根据硫酸钠、氯化钠和硝酸钠溶解度曲线和硫酸钠-氯化钠-H2O三元水盐体系相图,制定了分盐结晶工艺方案,先对硫酸钠和氯化钠进行了分离,实验结果表明,硫酸钠晶体达到了GB/T6009—2014工业无水硫酸钠Ⅲ类合格品(>92%),氯化钠晶体达到了GB/T 5462—2003日晒工业盐Ⅱ类标准(>92%)。
(2)将氯化钠二次蒸发结晶后的母液再次降温,析出硝酸钠晶体纯度高达98%,达到了GB/T 4553—2002工业硝酸钠合格品的标准,硝酸钠结晶后的滤液返回低温冷冻阶段对结晶产品无影响。
(3)实验表明分盐结晶工艺技术可行,操作方便,是实现废水中盐的资源化利用,减少杂盐危废排放的有效手段。
参考文献
Salt recovery from wastewater by air-cooled eutectic freeze crystallization
[J].DOI:10.1016/j.cej.2017.05.136 [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号