光催化氧化法近年来被广泛用于去除水体中的HA〔5〕。作为一种常用的半导体光催化剂,TiO2具有催化效率高、价格便宜、无毒、化学稳定性好等优点〔6〕。但TiO2颗粒以悬浮状态独自使用时存在吸附性差、回收困难等问题〔7〕。研究人员以Fe3O4颗粒作为磁核,设计核壳结构的磁性光催化材料,使其能在外加磁场的条件下快速回收。但TiO2直接沉积在Fe3O4表面时,Fe3O4磁核与TiO2包覆层之间会产生不利异质结,使电子空穴复合的能力变强,光催化活性降低〔8〕。在Fe3O4和TiO2层间引入性质稳定的SiO2隔离层可降低磁核对TiO2活性的影响〔9〕。有研究将TiO2负载在活性炭(AC)表面制备出负载型光催化剂用于降解污染物,AC的加入可提高催化剂的吸附性能,从而提高材料的光催化性能〔10〕。
本文以纳米Fe3O4颗粒为磁核,硅酸四乙酯和钛酸丁酯分别作为SiO2和TiO2的原材料,采用共沉淀法耦合溶胶-凝胶法制备了核壳结构的磁性颗粒Fe3O4@SiO2@TiO2,将其负载在载体AC表面,制备出新型光催化材料Fe3O4@SiO2@TiO2-AC,考察其对天然有机物HA的光催化降解效能,以期为有效去除水源水中的有机污染物探求新的技术途径。
1 材料与方法
1.1 主要仪器与试剂
材料:钛酸丁酯(TBOT),化学纯;腐殖酸、硫酸亚铁、氢氧化钠、硅酸四乙酯(TEOS)、月桂酸、氨水、活性炭粉、无水乙醇、盐酸、硝酸、十二烷基磺酸钠、氯化铁、氯化锌,均为分析纯。试验用水为超纯水。
仪器:Quanta FEG 250扫描电子显微镜,美国FEI公司;7400振动样品磁强计,美国Lakeshore公司;TU-1900紫外可见分光光度计,北京普析通用仪器有限责任公司;D8 advance X射线衍射仪,德国布鲁克公司;Sartorious PB-10 pH计,德国Sartorious公司;Nicolet 460傅氏转换红外线光谱分析仪,美国赛默飞世尔科技公司;F48010-33CN马弗炉,上海寰熙医疗器械有限公司;GDZ400高压汞灯,上海季光特种照明厂。
1.2 Fe3O4@SiO2@TiO2-AC的制备
1.2.1 Fe3O4纳米微粒的制备
将适量Fe3+、Fe2+(物质的量比2:1)溶于稀盐酸中,在80 ℃、恒温搅拌条件下滴加3 mol/L的NaOH溶液,调节溶液pH至9~10,出现黑色沉淀即为Fe3O4,充分反应后用水和无水乙醇各洗涤3次至中性,得到纳米Fe3O4微粒。
1.2.2 Fe3O4@SiO2纳米微粒的制备
将制得的Fe3O4纳米微粒加入到无水乙醇和水的混合液中,超声10 min后加入氨水并充分搅拌。搅拌完成后在25 ℃下逐滴加入硅酸四乙酯溶液,搅拌反应4 h,用水和无水乙醇将沉淀物各洗涤3次,105 ℃烘干,得到Fe3O4@SiO2纳米微粒。
1.2.3 Fe3O4@SiO2@TiO2纳米微粒的制备
在无水乙醇中加入适量钛酸丁酯和Fe3O4@ SiO2,超声10 min后搅拌20 min,加入冰乙酸后继续搅拌30 min。将一定比例的水、无水乙醇、硝酸构成的混合液,滴加到上述溶液中,继续搅拌60 min,70 ℃下水浴3 h得到湿凝胶,105 ℃干燥,于马弗炉中450 ℃煅烧3 h,冷却后将煅烧后的产物研磨、过0.074 mm(200目)筛,得到Fe3O4@SiO2@TiO2微粒,储存备用。
1.2.4 Fe3O4@SiO2@TiO2-AC催化剂的制备
取适量月桂酸及氢氧化钠溶于超纯水中,加入一定质量的Fe3O4@SiO2@TiO2,在90 ℃水浴锅中反应30 min,调节pH至4~5,水洗至中性,加入适量十二烷基磺酸钠,60 ℃下反应1 h后升温至80 ℃,加入一定量经过ZnCl2活化的AC反应3 h,水洗,干燥,得到Fe3O4@SiO2@TiO2-AC光催化剂。
1.3 HA模拟水样配制与标准曲线绘制
准确称取25 mg HA粉末于一定量稀NaOH(0.1 mol/L)热溶液中,充分溶解后用稀盐酸(0.1 mol/L)调节pH至中性,转移至500 mL容量瓶中,用超纯水定容得到质量浓度为50 mg/L的HA溶液,储存于4 ℃冰箱备用,试验时根据所需浓度进行稀释。
HA对波长254 nm的紫外光有较好的吸收,因此常用254 nm处的吸光度UV254衡量水样中HA的含量。将HA储备液稀释成不同浓度的溶液,以超纯水为参比测定吸光度UV254。以质量浓度为横坐标,吸光度为纵坐标拟合标准曲线,得到曲线方程UV254=0.027C-0.001 2(R2=0.999 7)。
1.4 试验装置与方法
光催化反应在400 W高压汞灯作光源、有循环冷却水的自制反应器中进行。将光催化剂加入到200 mL HA水样中进行光催化试验,每次取样5 mL进行磁分离,对上清液过0.45 μm滤膜后测定其UV254数值,按1.3中标准曲线方程计算HA质量浓度,并计算HA去除率。考察试验条件对光降解HA的影响时,在试验开始60 min时取样测定并计算相关参数;进行光催化动力学及比较不同体系下HA降解情况时每隔10 min取样测定并计算相关参数。
2 结果与讨论
2.1 Fe3O4@SiO2@TiO2-AC表征
2.1.1 扫描电镜(SEM)
图 1为Fe3O4@SiO2@TiO2与Fe3O4@SiO2@TiO2-AC颗粒的SEM照片。
图1
2.1.2 X射线衍射(XRD)
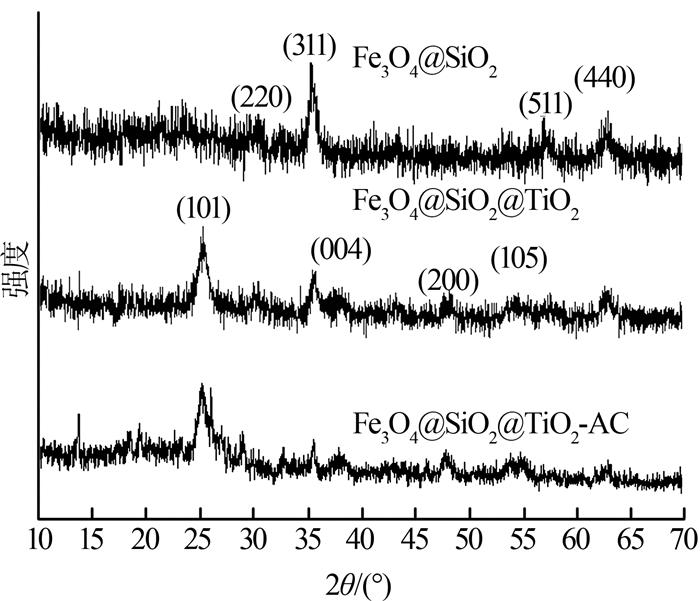
Fe3O4@SiO2、Fe3O4@SiO2@TiO2、Fe3O4@SiO2@TiO2- AC的XRD谱图如图 2所示。
图2
由图 2可见,30.1°、35.4°、57.1°、62.7°处的衍射峰分别对应尖晶石型Fe3O4结构的(220)、(311)、(511)及(440)晶面,23.5°左右出现1个宽峰,为不定形SiO2的特征衍射峰,说明磁性粒子Fe3O4与SiO2结合成功〔9〕;在Fe3O4@SiO2@TiO2谱线上,25.3°、37.9°、48.0°、54.1°的衍射峰对应于锐钛矿型TiO2结构的(101)、(004)、(200)、(105)晶面,表明TiO2纳米颗粒已经成功包覆Fe3O4@SiO2颗粒〔11〕;Fe3O4@SiO2@ TiO2-AC的XRD谱线上,Fe3O4、SiO2、TiO2的特征峰均有出现,虽然峰强变小,但结构未发生明显改变,可以判断AC表面成功负载了Fe3O4@SiO2@TiO2。
2.1.3 傅里叶转换红外光谱(FTIR)
对比了Fe3O4@SiO2、Fe3O4@SiO2@TiO2及Fe3O4@ SiO2@TiO2-AC颗粒的FTIR谱图。1 627、3 409 cm-1处出现的是—OH的特征吸收峰,956、1 091 cm-1处分别对应Si—OH伸缩振动吸收峰和Si—O—Si反对称吸收振动峰,469、799 cm-1处的吸收峰分别对应Si—O—Si键的弯曲振动和Si—O键的对称伸缩振动峰;583 cm-1为Fe—O键的特征吸收峰,表明SiO2已成功包覆在Fe3O4表面〔12〕。Fe3O4@SiO2@TiO2的红外光谱中,SiO2在400~600 cm-1的特征吸收峰基本被TiO2中Ti—O的伸缩振动峰掩盖〔12〕,表明TiO2成功覆盖在SiO2表面。Fe3O4@SiO2@TiO2-AC的红外谱图中,1 080 cm-1处为TiO2与AC接触界面生成的Ti—C键吸收峰〔13〕,表明Fe3O4@SiO2@TiO2成功与AC结合。
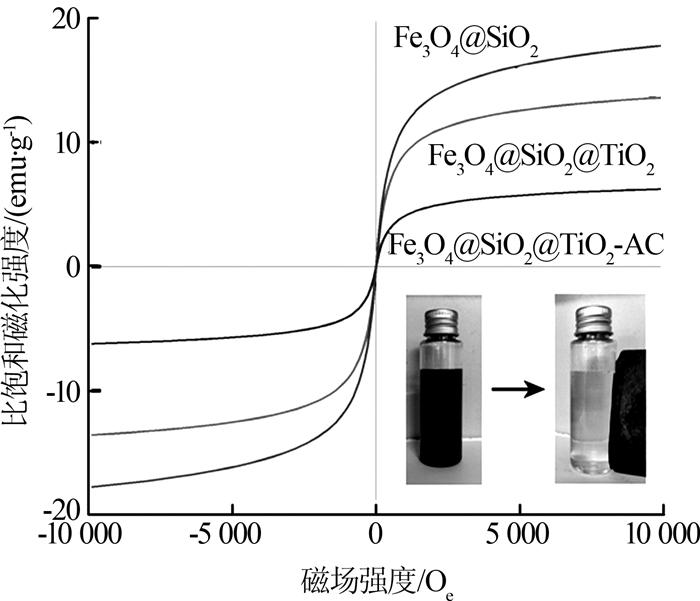
2.1.4 磁滞回线(VSM)
Fe3O4@SiO2、Fe3O4@SiO2@TiO2、Fe3O4@SiO2@TiO2- AC的VSM分析见图 3。
图3
2.2 试验条件对去除效果的影响
2.2.1 材料投加量对HA降解的影响
对于初始质量浓度为5 mg/L、pH为7的HA水样,考察了Fe3O4@SiO2@TiO2-AC不同投加量下光降解60 min的情况,如表 1所示。
试验发现,一定范围内HA的去除率与催化剂投加量呈正相关。分析认为,投加量增加可使光催化体系获得更多的电子-空穴对,提高光催化效率。但当体系中的催化剂达到一定浓度后,溶液中密度过高的催化剂颗粒对光源产生一定遮挡效应,阻碍了光催化剂对光源的利用〔14〕。此外,数量较多的催化剂颗粒会形成聚集体,不利于催化剂表面活性点位对污染物质的吸附及对光源的利用。兼顾使用成本,催化剂用量应存在一个最优值。在本研究中,催化剂投加量为200 mg/L时,HA降解率可达96.1%。
2.2.2 HA初始浓度对HA降解的影响
催化剂投加量为200 mg/L,HA水样pH为7,光降解60 min时,HA初始质量浓度对降解率的影响如表 2所示。
随着HA初始质量浓度的增加,HA去除率降低。一方面,单位时间内溶液中催化剂所产生的电子空穴对数量为定值,即氧化分解的污染物量一定,随着溶液中HA质量浓度的增加,所需完全降解的时间也就越长,即单位时间的去除率减少。另一方面,HA溶液自身有颜色,且色度会随浓度的增加而增加,致使紫外光的穿透率越来越低,影响催化剂对光的利用,降低光催化反应速率。
2.2.3 溶液pH对HA降解的影响
催化剂投加量为200 mg/L,HA水样初始质量浓度为5 mg/L,光降解60 min时,溶液pH对HA降解率的影响如表 3所示。
由表 3可见,溶液pH对HA的降解效果影响显著,HA降解率与溶液pH呈负相关:当溶液pH>9时,HA去除效果开始急剧降低。
另一方面,HA在不同pH条件下的水溶性不同:酸性条件下,HA在水中的溶解度下降,部分HA会以胶体析出,该部分HA在测样前或被滤膜直接截留,使得水样UV254测量值偏低。实际地表水体一般为中性,而Fe3O4@SiO2@TiO2-AC在pH为7时对HA有良好的去除效果,表明其具有实际应用价值。
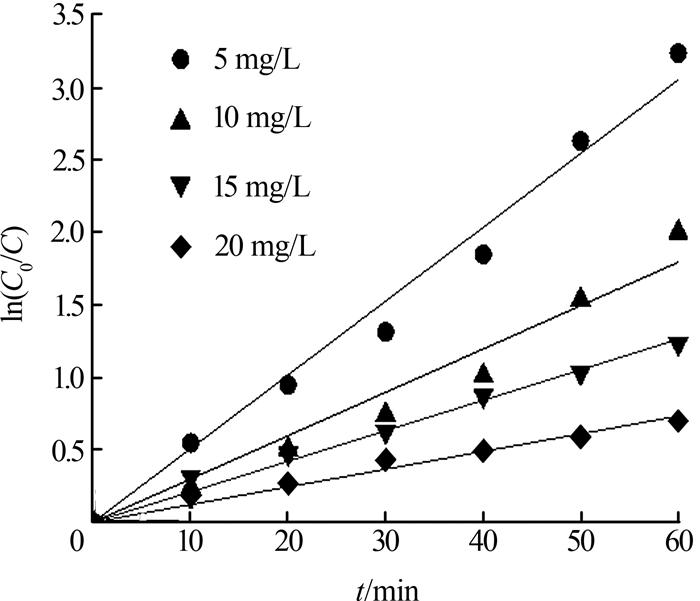
2.3 光催化反应动力学
光催化属于非均相反应,一般来说,光催化动力学遵循Langmuir-Hinshelwood模型(L-H模型),模型的最终表达式如式(1)所示〔17〕。
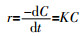
式中:r——HA在反应中的总反应速率,mg/(L·min);
C——t时刻HA质量浓度,mg/L;
K——光催化反应的表观一级降解速率常数,min-1。
对式(1)积分可得式(2)。
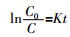
式中:C0—HA的初始质量浓度,mg/L。
图4
表4 不同HA质量浓度下的一级反应常数
| C0/(mg·L-1) | R2 | K/min-1 |
| 5 | 0.993 7 | 0.050 9 |
| 10 | 0.983 8 | 0.029 9 |
| 15 | 0.995 5 | 0.021 0 |
| 20 | 0.991 0 | 0.012 2 |
2.4 不同体系下HA的降解情况
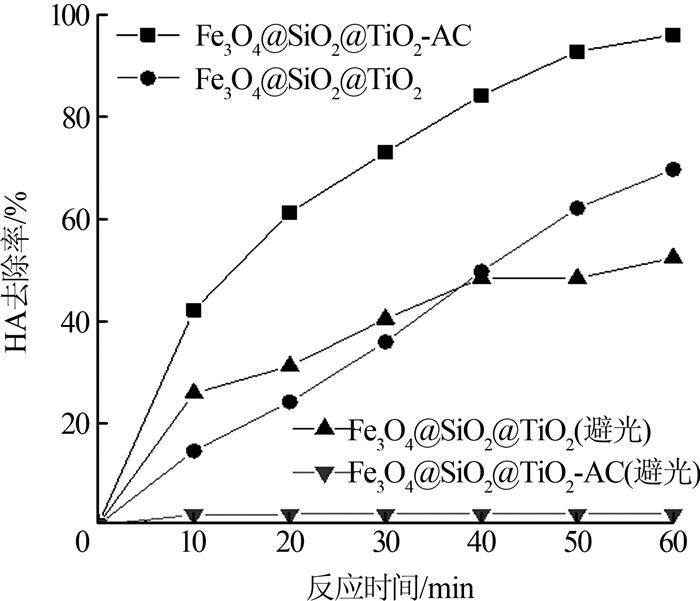
在催化剂投加量为200 mg/L、HA初始质量浓度为5 mg/L、pH为7的条件下,考察不同催化体系对HA的降解效果,如图 5所示。
图5
由图 5可见,避光条件下Fe3O4@SiO2@TiO2-AC与Fe3O4@SiO2@TiO2通过吸附作用去除HA,60 min时去除率分别为52.3%、2.1%,可见,AC的复合可有效提高材料的吸附性能;在紫外光下,Fe3O4@SiO2@ TiO2-AC对HA的去除效果明显优于Fe3O4@SiO2@ TiO2,60 min后去除率分别为96.1%、69.66%。
在紫外光照射下,TiO2价带的电子激发进入导带,具有还原能力的光生电子在导带上形成,具有氧化能力的光生载流子(空穴)在价带上形成。在水溶液中,一般认为OH-和H2O俘获载流子产生·OH,氧分子和光生电子产生O2·-,具有强氧化性的·OH和O2·-可氧化分解HA;HA也可直接作为俘获剂俘获载流子进行氧化分解〔16〕。AC使复合材料的吸附性能得到提高,从而使HA分子在复合光催化剂表面更快速富集,更高效地俘获游离·OH进行降解,复合光催化剂表面的吸附点位也得到再生,恢复强大的吸附性能,以此循环,Fe3O4@SiO2@TiO2与AC这种协同作用使得复合光催化剂具有更好的催化效能。此外,AC还可防止有机污染物分解的中间产物游离挥发,使降解更为彻底。
2.5 催化剂的循环使用性能
可重复利用性是衡量催化剂实际应用价值的重要因素。将40 mg Fe3O4@SiO2@TiO2-AC投加到200 mL初始质量浓度为5 mg/L、pH为7的HA水样中,光催化降解60 min后磁分离,测定上清液UV254并计算HA降解率。催化剂分离后,用超纯水清洗、烘干,重复如上试验,5次循环试验数据依次为96.1%、92.1%、89.9%、87.2%、84.7%。以上数据表明,HA降解率在5次重复使用后仍可达到84.7%,所制备光催化剂具有良好的可重复利用性。
3 结论
(1)采用共沉淀法耦合溶胶-凝胶法制备了Fe3O4@SiO2@TiO2颗粒,并将其负载在AC表面,制备出新型光催化剂Fe3O4@SiO2@TiO2-AC。制备的光催化剂呈结晶度良好的锐钛矿型结构,比饱和磁化强度值6.25 emu/g,具备良好的超顺磁性,可在外加磁场作用下实现快速高效分离。
(2)光催化剂Fe3O4@SiO2@TiO2-AC对pH适应范围较宽,在酸性、中性和弱碱性条件下对水样中的HA均有优良的光催化降解效能。在400 W高压汞灯照射下,光催化剂投加量为200 mg/L时,对于初始质量浓度为5 mg/L、pH为7的HA水样,经60 min的光催化降解,HA去除率可达96.1%。
(3)Fe3O4@SiO2@TiO2-AC对HA的光催化降解反应符合Langmuir-Hinshelwood动力学模型;Fe3O4@ SiO2@TiO2与AC的协同作用可有效提高光催化剂的活性。Fe3O4@SiO2@TiO2-AC具有良好的循环使用能力,在实际天然水体净化领域具有应用价值。
参考文献
Effect of UV wavelength on humic acid degradation and disinfection by-product formation during the UV/chlorine process
[J].
Surfactant modified zeolite as adsorbent for removal of humic acid from water
[J].
Characterization of persistent colors and decolorization of effluent from biologically treated cellulosic ethanol production wastewater
[J].
Multiple dynamic Al-based floc layers on ultrafiltration membrane surfaces for humic acid and reservoir water fouling reduction
[J].
Removal of humic acid from aqueous solution using UV/ZnO nano-photocatalysis and adsorption
[J].
Visible-light photocatalysis in nitrogen-doped titanium oxides
[J].
Understanding TiO2 photocatalysis:mechanisms and materials
[J].
Preparation and characterization of magnetic TiO2 nanoparticles and their utilization for the degradation of emerging pollutants in water
[J].
磁性光催化剂Fe3O4/SiO2/TiO2的制备及光催化降解苯酚
[J].
Preparation and enhanced photocatalytic performance of a novel photocatalyst:Hollow network Fe3O4/mesoporous SiO2/TiO2(FST) composite microspheres
[J].
Evaluation of photocatalytic degradation of 2, 4-dinitrophenol from synthetic wastewater using Fe3O4@SiO2@TiO2/rGO magnetic nanoparticles
[J].
Effect of sodium persulfate as electron acceptor on antipyrine degradation by solar TiO2 or TiO2/rGO photocatalysis
[J].






 津公网安备 12010602120337号
津公网安备 12010602120337号