液体推进剂废水主要包括火箭发动机试车产生的污水、火箭发射产生的污水、推进剂槽车、贮罐、管道洗消污水、推进剂库房地面清洗污水、推进剂泄漏事故洗消污水。本实验处理的推进剂废料主要成分是无水肼和硝酸肼。无水肼具有易燃、强还原性、强腐蚀性、剧毒等特点,其蒸汽能与空气形成爆炸性混合物。遇明火、高热极易燃烧爆炸。受热分解放出有毒的氧化氮烟气。硝酸肼是一种高能猛炸药。该污染物若不经处理直接排放,对周围大气、农作物、土壤及地表水会造成严重危害,其分解中间产物可致突变、致畸和致癌〔1〕。对推进剂废水处理的研究方法有很多,常用的处理方法如离子交换法、光催化法、氯化处理法、吸附法、自然净化法、臭氧氧化法等,但这些方法的处理效率低,反应时间长。
无水肼和硝酸肼属于肼类物质,氮的质量分数比偏二甲肼高,处理难度更大。笔者对催化超临界氧化技术处理硝酸肼和无水肼废水进行了实验研究,考察了温度、压力、反应时间、过氧系数和催化剂对COD和NH3-N降解效果的影响,使其出水达到了航天推进剂污水排放标准(GB 14374—93)。
1 实验部分
1.1 水样水质
来自某发射基地液体推进剂废料,其主要成分是无水肼(67%)和硝酸肼(24%)。用蒸馏水稀释100倍后为实验水样,其COD为7 310 mg/L,NH3-N为1 664 mg/L,pH为9.05,显碱性,无色无味。
1.2 实验装置与过程
本实验采用由中北大学自主设计的间歇式超临界水氧化设备,见图1。
图1
图1
间歇式超临界水氧化实验装置
1—进料瓶;2—高压柱塞泵;3—氧气罐;4—水泵压力传感器;5—温度感应器;6—加热套;7—反应釜;8—无机盐收集罐;9—反应釜压力传感器;10—热交换器;11—气液分离器;12—气体收集罐;13—液体收集罐。
反应釜的有效体积为0.3 L,设计最高压力为30 MPa,温度为600 ℃。实验开始前,将一定量的催化剂放入反应釜,通过氧气瓶打入反应需要氧气量,关闭所有阀门保持一段时间,如果压力表示数稳定,设定反应需要的温度,打开加热开关。当温度达到设定值时,将推进剂废水通过高压柱塞泵打入反应釜内,当反应釜压力传感器示数达到预设值时,停止加料。开始记录反应时间,达到设定的反应时间后,关闭加热开关。打开出料阀门,釜内物质经过热交换器和气液分离器,分离器上端排出气体,下端排出液体,收集液体,对收集的液体采用国标法测COD和快速测定仪测NH3-N。
1.3 分析方法
用德国罗威邦制造的多参数水质快速测定仪测NH3-N;用国标GB 11914—89化学需氧量的测定方法来测COD;XRD用XRD-6000型X射线衍射仪(日本岛津公司)测定;SEM用Quanta 400F型扫描电镜(日本FEI公司)测定。
1.4 过氧系数的计算
压力表显示的压强经过理想气体状态方程换算成氧气量。过氧系数的计算方式见式(1)。
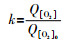
式中:k——过氧系数;
Q[O2]——反应初始时加入的氧气量,L;
Q[O2]0——液体推进剂废料氧化所需要的理论氧气量,L。
2 结果与讨论
2.1 反应条件的影响
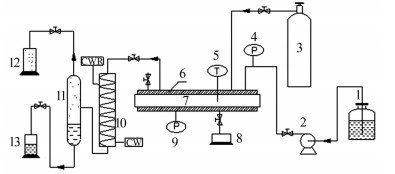
在压力为24 MPa,反应时间为3 min的条件下,研究温度和过氧系数对出水COD和NH3-N的影响,结果见图2。
图2
由图2(a)可知,随着温度的提高,硝酸肼和无水肼的降解效率显著提高,温度对COD去除效果的影响很显著。这主要是因为随着温度的升高,硝酸肼和无水肼中的活性物质增加以及分子热运动加快,增加了分子间的碰撞几率,使氧化反应速率加快,从而提高了降解率。温度在500~550 ℃时,折线比较平缓,继续升高温度效果不显著,此时的处理效率已经达到了99%,所以反应温度为550 ℃时最佳。过氧系数也影响了出水COD,但温度较高时,过氧系数不是主要的影响因素。
由图2(b)可知,在无氧气条件下,NH3-N随着温度增加反而增高,这是由于硝酸肼和无水肼的分解造成的。继续升高温度,NH3-N没有明显的变化,与N. Segond等〔4〕的研究一致。他的研究表明,在873 K和24.5 MPa的条件下,停留时间为2 min,过氧系数为0时,氨分解率最高仅为2%。温度为550 ℃时,随着过氧系数从2增加到6,NH3-N从834 mg/L降低到113 mg/L,综合上述各个实验结果可知,NH3-N的降解和过氧系数有关。在过氧系数一定的条件下,温度从450 ℃上升到550 ℃,NH3-N降解速率变化比较大,说明温度也是影响NH3-N降解的重要因素,升高温度有利于NH3-N的降解,但B. Al-Duri等〔5〕报告说,由于氨的顽固性,即使在650 ℃仍很丰富,需要催化剂来提高转化率,所以继续提高温度只会增加耗能,最佳反应温度范围应为500~550 ℃。过氧系数高时NH3-N降解效果明显,为了满足航天推进剂污水排放标准(NH3-N低于40 mg/L),反应条件中过氧系数应不低于6。
在实际应用中,由于反应放热,可以自行维持反应,不需要一直外部加热。维持较高的温度,有利于反应的高效进行。过氧系数对NH3-N的降解效果影响显著,但提高过氧系数能耗较高,实现难度较大。可以根据实际需求,取适当的过氧系数。
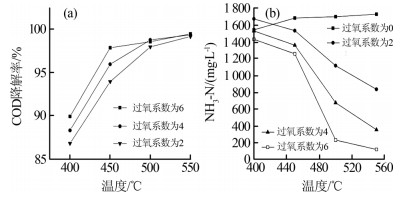
在温度为550 ℃,过氧系数为6的条件下,考察反应时间和压力对出水COD和NH3-N的降解效果的影响,结果见图3。
图3
改变压力和停留时间对NH3-N去除效果的影响很小。M. Koo等〔7〕在400 ℃和860%过量氧的间歇反应器中降解苯酚。通过增加氦气来提高压力。结果发现,氧化速率不依赖于压力本身,压力主要是通过改变氧气和苯酚浓度影响反应。高温下,只需加入少量的硝酸肼和无水肼就可以改变压力,超临界水中NH3-N浓度没有发生大的变化,所以压力从20 MPa提高到24 MPa,NH3-N降解效果变化不明显。延长反应时间不会改变反应体系中的活性物质,从而NH3-N不会随着反应时间的改变而变化。综上所述,最佳反应条件:温度为550 ℃,压力为24 MPa,反应时间为3 min,过氧系数为6。
2.2 催化剂的影响
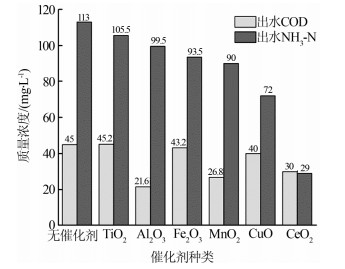
在上述条件下,将投加量为硝酸肼和无水肼废液质量0.5%的MnO2、Al2O3、Fe2O3、TiO2、CuO、CeO2分别加入到反应釜,考察不同催化剂对出水COD和氨氮的降解效果的影响,结果见图4。
图4
由图4可知,与非催化反应相比,催化剂可以促进硝酸肼和无水肼的分解。根据COD降解效果,催化性能顺序为Al2O3 > MnO2 > CeO2 > CuO > Fe2O3 > TiO2。Al2O3、MnO2和CeO2对提高COD的降解有明显的作用。在NH3-N的降解中,CeO2的催化效果最佳,催化性能顺序是CeO2 > CuO > MnO2 > Fe2O3 > Al2O3 > TiO2。Al2O3对NH3-N的降解催化效果不显著,但对COD的降解有显著的催化效果,说明Al2O3在超临界水中可以促进硝酸肼和无水肼的分解,提升处理效率,但对氨的去除性能差。CuO对NH3-N的降解有显著的催化效果,对COD降解的催化效果不显著,可能是由于CuO具有强还原性,为吸附的氨提供了较多的晶格氧,但表面阴离子空穴较少,不利于无水肼和硝酸肼中间产物的吸附。加入CeO2后,COD的降解率可以达到99%以上,处理后氨氮为29 mg/L,根据报道,CeO2有优异的储存和释放氧气的能力,可以经历连续的Ce4+/Ce3+氧化还原循环,在还原环境或较高温度下,可被还原为低价态,失去晶格氧形成氧缺陷,处于氧化环境时,低价态很容易再被氧化为CeO2〔8-10〕。CeO2所表现出的优异活性归功于其完成氧化还原循环的能力。
表面氧反应性和金属氧化物的还原性是决定金属氧化物的氧化还原水平的重要因素。根据现有的研究〔11-12〕,氧气程序升温脱附(O2-TPD)可以分析表面氧的反应性。CuO、Fe2O3脱附峰面积相近,Al2O3、TiO2表现出很小的氧解吸,MnO2脱附峰面积较大。脱附峰面积大,催化剂则具有较多的固有阴离子空穴和较多的表面缺陷位,有利于吸附和活化气相氧;氢气程序升温还原(H2-TPR)可以分析金属氧化物的还原性,CuO的TPR谱在300 ℃以上呈现了1个宽而相对低温的峰(Cu2+→Cu0),MnO2在300~ 500 ℃有2个还原峰(MnO2→Mn3O4→MnO),Fe2O3的TPR谱中,发现在400 ℃以上有显著的H2吸收(Fe3+→Fe2+→Fe0),单独还原Al2O3或TiO2很困难,并且在50~750 ℃没有观察到TPR峰。通过金属氧化物还原温度和耗氢速度、耗氢量可以对比其还原性,综合考虑金属氧化物的表面氧反应性和还原性,MnO2的氧化还原能力最佳,Al2O3、TiO2最差,CuO、Fe2O3比较接近。CuO表现出很好的还原性,但表面氧反应性比较差。Al2O3氧化还原能力不强,但具有较高的孔容、比表面积和热稳定性。催化剂性能顺序基本与氧化还原性吻合。
2.3 催化剂稳定性能的表征
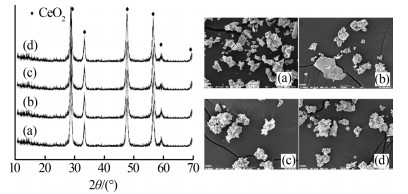
对硝酸肼和无水肼中COD和NH3-N的降解考察结果表明,CeO2的综合效果最佳。在压力为24 MPa,过氧系数为6,反应时间为3 min的条件下,考察不同温度下,CeO2的XRD和SEM,结果见图5。
图5
通过比较不同温度下回收的催化剂和新鲜催化剂的XRD图谱,可以考察反应前后催化剂的稳定性。在高温和高压条件下,没有观察到催化剂发生相变的峰,CeO2没有被还原,催化剂可以保持最高氧化状态。这些结果表明,超临界水中具有完全氧化还原循环,可以再生还原催化剂。
通过比较SEM可知,CeO2前后的结构没有发生大的变化。CeO2是广泛使用的稀土氧化物,有出色的“储氧”能力和稳定的晶型结构,这样的结构有利于阻止体积的收缩,从而提高催化剂的活性和稳定性。CeO2对于硝酸肼和无水肼中NH3-N和COD的降解,有很好的催化效果,其结构也比较稳定,可以应用于大规模的废水处理中。
2.4 反应机理和催化作用机理
无水肼和硝酸肼中N—N键弱于N—H键(分别为296.4 kJ/mol和413.6 kJ/mol),结合葛红光对偏二甲肼反应路径的研究〔17〕,反应机理第一步最有可能是:

链的引发期,O2直接参与反应,生成初始的自由基:
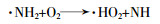

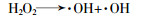
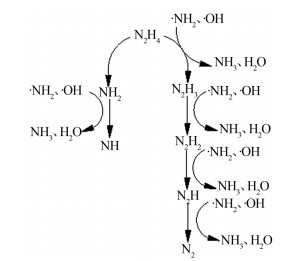
根据图2可知,在无氧条件下,在出水中有新的NH3-N生成,说明肼中的氮可能转化为NH3:
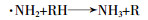

图6
反应物硝酸肼含有硝酸根,其可能的反应机理如下:
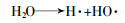
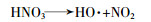

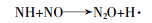
当添加催化剂后,非均相催化剂在超临界水中大部分以固体形式沉积下来,无水肼和硝酸肼可以在固相沉积表面发生吸附催化降解。在SCWO中,首先由金属氧化物催化剂的晶格氧提供氧化用氧,然后催化剂还原至较低氧化态。由于晶格氧的消耗,催化剂表面形成氧缺位,系统外部的分子氧吸附在氧缺位。同时氧缺位也可以吸附超临界水中的中间产物,使反应高效率进行。最后超临界水供应的活性氧再生转化催化剂,从而完成氧化还原循环。其中氨的催化降解如下:

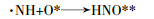

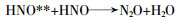
式中“*”为催化剂的活性位点。
3 结论
(1)硝酸肼和无水肼中NH3-N和COD降解的最佳反应条件:温度为550 ℃,压力为24 MPa,反应时间为3 min,过氧系数为6,此时COD的降解率达到99%,NH3-N降到113 mg/L。
(2)催化剂对NH3-N降解效果的排序是CeO2 > CuO > MnO2 > Fe2O3 > Al2O3 > TiO2。其中CeO2可以使NH3-N降到29 mg/L,达到了航天废水排放标准。
(3)在高温和高压条件下,CeO2没有被还原,催化剂可以保持最高氧化状态。
(4)根据自由基机理的研究,·OH和·NH2可能有竞争,所以升高温度和过氧系数有利于NH3-N的降解。
参考文献
Gasification of unsymmetrical dimethylhydrazine in supercritical water:Reaction pathway and kinetics
[J].DOI:10.1016/j.ijhydene.2018.03.092 [本文引用: 1]
Determination of ammonia oxidation rate in suband supercritical water
[J].
Thermal abatement of nitrogen-containing hydrocarbons by non-catalytic supercritical water oxidation(SCWO)
[J].DOI:10.1007/s10853-007-2285-3 [本文引用: 1]
Supercritical water for environmental technologies
[J].
New reactor system for supercritical water oxidation and its application on phenol destruction
[J].DOI:10.1016/S0009-2509(96)00477-0 [本文引用: 1]
Oxygen vacancy clusters promoting reducibility and activity of ceria nanorods
[J].DOI:10.1021/ja808433d [本文引用: 1]
Oxygen vacancies and catalysis on ceria surfaces
[J].
Size-dependent oxygen storage ability of nano-sized ceria
[J].DOI:10.1039/c3cp51959g [本文引用: 1]
Enhanced pyrolysis and oxidation of asphaltenes adsorbed onto transition metal oxides nanoparticles towards advanced in-situ combustion EOR processes by nanotechnology
[J].
Generalized kinetic model for wet oxidation of organic compounds
[J].DOI:10.1002/aic.690371112 [本文引用: 1]
Catalytic oxidation in supercritical water
[J].
Supercritical water oxidation of NH3 over a MnO2/CeO2 catalyst
[J].
The fate of nitrogen in supercritical water oxidation
[J].DOI:10.1016/0896-8446(92)90044-K [本文引用: 1]





 津公网安备 12010602120337号
津公网安备 12010602120337号