燃煤电厂脱硫废水处理技术研究进展
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
Research progress on treatment technology for desulfurization wastewater from coal-fired power plants
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
燃煤电厂脱硫废水重金属脱除技术研究进展
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
Research progress on removal technology for heavy metals in desulfurization wastewater from coal-fired power plants
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
燃煤电厂脱硫废水零排放工艺的应用进展
1
2021
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
Application progress on zero discharge process for desulfurization wastewater from coal-fired power plants
1
2021
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
燃煤电厂脱硫废水处理技术工程应用现状与展望
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
Application progress and prospect of desulfurization wastewater treatment technologies in coal-fired power plants
1
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
燃煤电厂脱硫废水重金属处理技术研究进展
1
2019
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
Research progress of heavy metal treatment technology for desulfurization wastewater from coal-fired power plants
1
2019
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
层状双金属氢氧化物及其复合材料去除水体中重金属离子的研究进展
6
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
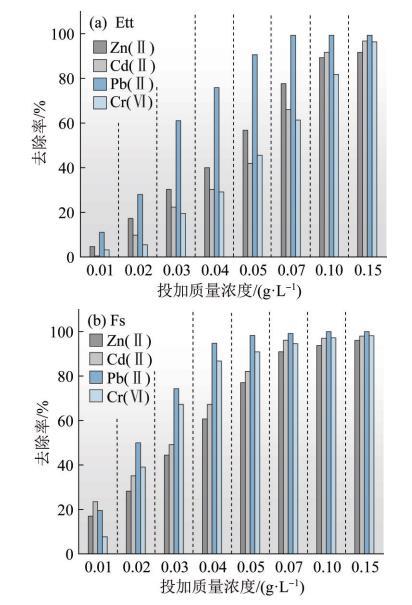
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
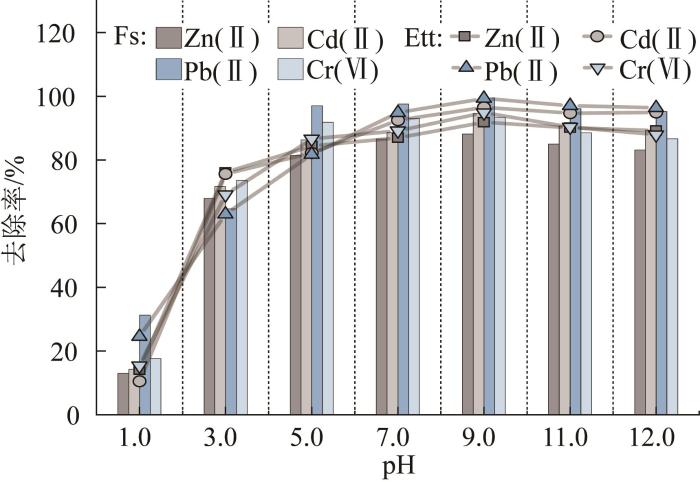
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
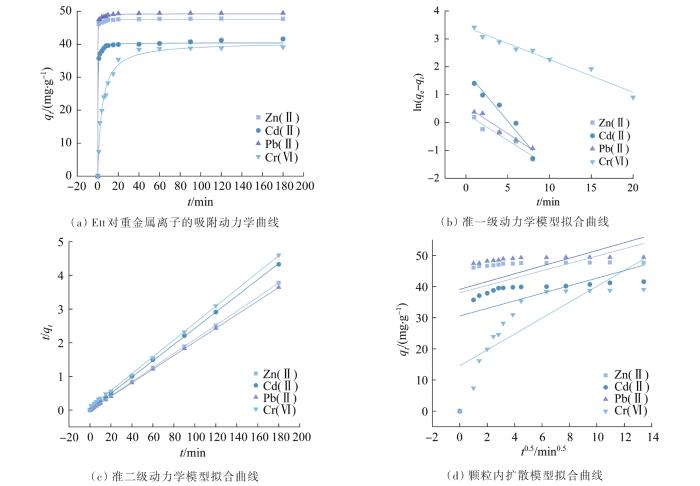
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
Research progress on removal of heavy metal ions from water by layered double hydroxides and its composites
6
2020
... 燃煤电厂广泛使用的石灰石-石膏湿法脱硫技术会导致大量脱硫废水的产生,该类脱硫废水含盐量高,且因存在多种重金属离子,排放进入环境会对生态系统和人体健康造成严重威胁〔1-3〕.目前,脱硫废水处理主要以传统的“三联箱”工艺为基础,通过中和、反应、混凝沉淀实现废水中重金属及其他污染物的去除〔4〕.然而该方法针对不同重金属需添加多种化学药剂分步去除,往往会引入新的污染物(如硫化物)〔2,5〕.随着纳米环境功能材料的发展,纳米零价铁、活性碳纤维网等吸附材料也被逐渐应用于重金属的去除,但这些材料因成本较高、性能不稳定、易受外界环境干扰而止步于实际工程应用〔6〕. ...
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
A review on heavy metal ions adsorption from water by layered double hydroxide and its composites
5
2022
... 近年来,大量研究表明,层状双金属氢氧化物(Layered double hydroxides,LDHs)因其固有的结构特性和较大的比表面积而在污染物吸附领域展现出很大的应用潜力〔7-8〕.Bo ZHANG等〔9〕采用共沉淀法合成了MgAl-LDHs,并在其层间插入乳酸分子形成无机-有机纳米复合材料后将其剥离成单层LDHs纳米片,用于对Cr(Ⅵ)的吸附去除,最大吸附容量可达125.97 mg/g.I. PAVLOVIC等〔10〕通过离子交换作用将二乙基三胺五乙酸(DTPA)嵌入LDHs层间,用于吸附水中Cu2+、Cd2+、Pb2+,实验结果表明,经修饰的LDHs对3种金属阳离子均具有较好的吸附效果.可见,LDHs对水中阴、阳金属离子表现出较好的吸附性能.此外,LDHs制备过程相对简单、成本较低,使其在实际工程中应用具有较高的可行性.此外,脱硫废水含有较高浓度的Ca2+、Mg2+等阳离子和Cl-、SO42-等阴离子,会严重干扰重金属的去除,而对于高盐环境条件下低含量重金属废水处理的研究尚未见报道.基于此,本研究针对脱硫废水水质特点,采用共沉淀法制备了Cl-插层的LDHs吸附剂弗里德尔盐(Friedel’s salt,Fs)和SO42-插层的LDHs吸附剂钙矾石(Ettringite,Ett),探究了各吸附剂投加量、废水初始pH和废水中存在的干扰离子对重金属去除效果的影响,并通过考察其吸附动力学对吸附剂的吸附特征进行了研究,阐释了LDHs对重金属吸附的内在机制和机理,为脱硫废水中重金属的去除提供了新思路. ...
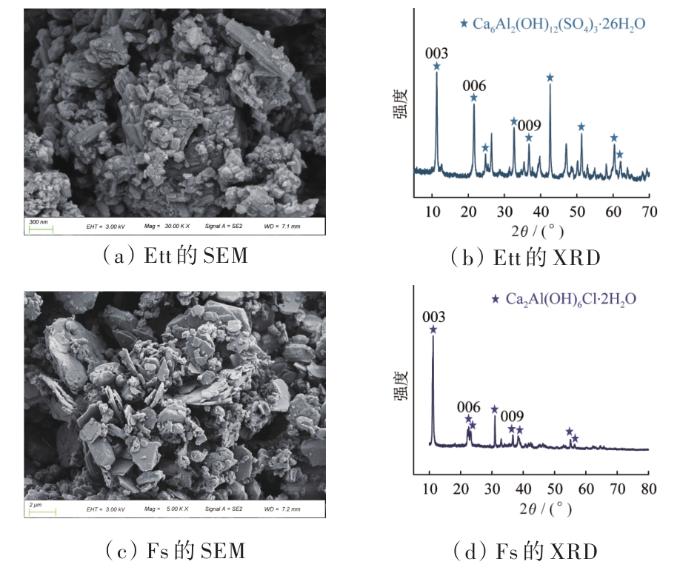
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 由图2还可知,当投加量相同时,无论是对以阳离子态存在的Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ),还是对以阴离子态存在的Cr(Ⅵ),相较于Ett,Fs均表现出更优的去除效果.尤其是当投加质量浓度为0.04 g/L时,与Ett相比,Fs对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)、Cr(Ⅵ)去除率分别高出20.7%、37%、18.9%、57.7%.究其原因,可能由于Ett的分子质量约为Fs的3倍,相同质量下,Fs表面存在更多OH-,更多重金属阳离子可与其发生化学键合而得以去除,此外,由于与SO42-相比,Cl-更易与CrO42-发生层间阴离子交换反应,因而Fs可更加容易地去除阴离子形式存在的Cr(Ⅵ)〔7〕. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
LDHs及其复合材料处理重金属废水的研究进展
1
2022
... 近年来,大量研究表明,层状双金属氢氧化物(Layered double hydroxides,LDHs)因其固有的结构特性和较大的比表面积而在污染物吸附领域展现出很大的应用潜力〔7-8〕.Bo ZHANG等〔9〕采用共沉淀法合成了MgAl-LDHs,并在其层间插入乳酸分子形成无机-有机纳米复合材料后将其剥离成单层LDHs纳米片,用于对Cr(Ⅵ)的吸附去除,最大吸附容量可达125.97 mg/g.I. PAVLOVIC等〔10〕通过离子交换作用将二乙基三胺五乙酸(DTPA)嵌入LDHs层间,用于吸附水中Cu2+、Cd2+、Pb2+,实验结果表明,经修饰的LDHs对3种金属阳离子均具有较好的吸附效果.可见,LDHs对水中阴、阳金属离子表现出较好的吸附性能.此外,LDHs制备过程相对简单、成本较低,使其在实际工程中应用具有较高的可行性.此外,脱硫废水含有较高浓度的Ca2+、Mg2+等阳离子和Cl-、SO42-等阴离子,会严重干扰重金属的去除,而对于高盐环境条件下低含量重金属废水处理的研究尚未见报道.基于此,本研究针对脱硫废水水质特点,采用共沉淀法制备了Cl-插层的LDHs吸附剂弗里德尔盐(Friedel’s salt,Fs)和SO42-插层的LDHs吸附剂钙矾石(Ettringite,Ett),探究了各吸附剂投加量、废水初始pH和废水中存在的干扰离子对重金属去除效果的影响,并通过考察其吸附动力学对吸附剂的吸附特征进行了研究,阐释了LDHs对重金属吸附的内在机制和机理,为脱硫废水中重金属的去除提供了新思路. ...
Research progress on treatment of heavy metal wastewater by layered double hydroxides and their composites
1
2022
... 近年来,大量研究表明,层状双金属氢氧化物(Layered double hydroxides,LDHs)因其固有的结构特性和较大的比表面积而在污染物吸附领域展现出很大的应用潜力〔7-8〕.Bo ZHANG等〔9〕采用共沉淀法合成了MgAl-LDHs,并在其层间插入乳酸分子形成无机-有机纳米复合材料后将其剥离成单层LDHs纳米片,用于对Cr(Ⅵ)的吸附去除,最大吸附容量可达125.97 mg/g.I. PAVLOVIC等〔10〕通过离子交换作用将二乙基三胺五乙酸(DTPA)嵌入LDHs层间,用于吸附水中Cu2+、Cd2+、Pb2+,实验结果表明,经修饰的LDHs对3种金属阳离子均具有较好的吸附效果.可见,LDHs对水中阴、阳金属离子表现出较好的吸附性能.此外,LDHs制备过程相对简单、成本较低,使其在实际工程中应用具有较高的可行性.此外,脱硫废水含有较高浓度的Ca2+、Mg2+等阳离子和Cl-、SO42-等阴离子,会严重干扰重金属的去除,而对于高盐环境条件下低含量重金属废水处理的研究尚未见报道.基于此,本研究针对脱硫废水水质特点,采用共沉淀法制备了Cl-插层的LDHs吸附剂弗里德尔盐(Friedel’s salt,Fs)和SO42-插层的LDHs吸附剂钙矾石(Ettringite,Ett),探究了各吸附剂投加量、废水初始pH和废水中存在的干扰离子对重金属去除效果的影响,并通过考察其吸附动力学对吸附剂的吸附特征进行了研究,阐释了LDHs对重金属吸附的内在机制和机理,为脱硫废水中重金属的去除提供了新思路. ...
Rapid and effective removal of Cr(Ⅵ) from aqueous solution using exfoliated LDH nanosheets
1
2017
... 近年来,大量研究表明,层状双金属氢氧化物(Layered double hydroxides,LDHs)因其固有的结构特性和较大的比表面积而在污染物吸附领域展现出很大的应用潜力〔7-8〕.Bo ZHANG等〔9〕采用共沉淀法合成了MgAl-LDHs,并在其层间插入乳酸分子形成无机-有机纳米复合材料后将其剥离成单层LDHs纳米片,用于对Cr(Ⅵ)的吸附去除,最大吸附容量可达125.97 mg/g.I. PAVLOVIC等〔10〕通过离子交换作用将二乙基三胺五乙酸(DTPA)嵌入LDHs层间,用于吸附水中Cu2+、Cd2+、Pb2+,实验结果表明,经修饰的LDHs对3种金属阳离子均具有较好的吸附效果.可见,LDHs对水中阴、阳金属离子表现出较好的吸附性能.此外,LDHs制备过程相对简单、成本较低,使其在实际工程中应用具有较高的可行性.此外,脱硫废水含有较高浓度的Ca2+、Mg2+等阳离子和Cl-、SO42-等阴离子,会严重干扰重金属的去除,而对于高盐环境条件下低含量重金属废水处理的研究尚未见报道.基于此,本研究针对脱硫废水水质特点,采用共沉淀法制备了Cl-插层的LDHs吸附剂弗里德尔盐(Friedel’s salt,Fs)和SO42-插层的LDHs吸附剂钙矾石(Ettringite,Ett),探究了各吸附剂投加量、废水初始pH和废水中存在的干扰离子对重金属去除效果的影响,并通过考察其吸附动力学对吸附剂的吸附特征进行了研究,阐释了LDHs对重金属吸附的内在机制和机理,为脱硫废水中重金属的去除提供了新思路. ...
Adsorption of Cu2+,Cd2+ and Pb2+ ions by layered double hydroxides intercalated with the chelating agents diethylenetriaminepentaacetate and meso-2,3-dimercaptosuccinate
1
2009
... 近年来,大量研究表明,层状双金属氢氧化物(Layered double hydroxides,LDHs)因其固有的结构特性和较大的比表面积而在污染物吸附领域展现出很大的应用潜力〔7-8〕.Bo ZHANG等〔9〕采用共沉淀法合成了MgAl-LDHs,并在其层间插入乳酸分子形成无机-有机纳米复合材料后将其剥离成单层LDHs纳米片,用于对Cr(Ⅵ)的吸附去除,最大吸附容量可达125.97 mg/g.I. PAVLOVIC等〔10〕通过离子交换作用将二乙基三胺五乙酸(DTPA)嵌入LDHs层间,用于吸附水中Cu2+、Cd2+、Pb2+,实验结果表明,经修饰的LDHs对3种金属阳离子均具有较好的吸附效果.可见,LDHs对水中阴、阳金属离子表现出较好的吸附性能.此外,LDHs制备过程相对简单、成本较低,使其在实际工程中应用具有较高的可行性.此外,脱硫废水含有较高浓度的Ca2+、Mg2+等阳离子和Cl-、SO42-等阴离子,会严重干扰重金属的去除,而对于高盐环境条件下低含量重金属废水处理的研究尚未见报道.基于此,本研究针对脱硫废水水质特点,采用共沉淀法制备了Cl-插层的LDHs吸附剂弗里德尔盐(Friedel’s salt,Fs)和SO42-插层的LDHs吸附剂钙矾石(Ettringite,Ett),探究了各吸附剂投加量、废水初始pH和废水中存在的干扰离子对重金属去除效果的影响,并通过考察其吸附动力学对吸附剂的吸附特征进行了研究,阐释了LDHs对重金属吸附的内在机制和机理,为脱硫废水中重金属的去除提供了新思路. ...
钙矾石法去除脱硫废水硫酸根沉淀物沉降特性研究
2
2022
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
... 〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
Settleability of ettringite precipitate for sulfate removal from flue gas desulfurization wastewater
2
2022
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
... 〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
层状双金属氢氧化物的制备、表征及硫酸根和氟离子吸附性能研究
1
2015
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
Study on preparation,characterization and sulfate,fluoride adsorption by layer double hydroxides
1
2015
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
Sulfate removal from wastewater using ettringite precipitation:Magnesium ion inhibition and process optimization
2
2017
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
... 〔13-15〕. ...
钙矾石对重金属离子的吸附固化及稳定性研究
2
2017
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
The immobilization and stability of heavy metal ions by ettringite
2
2017
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
混合金属氧化物/碳复合材料的制备及其对Pb(Ⅱ)的吸附性能
3
2021
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
Preparation of mixed metal oxide/carbon composites and its adsorption performance for Pb(Ⅱ)
3
2021
... 图1(a)与图1(b)所示分别为所制备Ett的SEM和XRD.图1(a)SEM显示,制备所得产物表面呈现出不规则的短棒状和颗粒状晶体结构,符合Ett的典型形貌特征〔11-12〕,粒子间存在明显团聚,可能是搅拌速率较高将晶体打散所致.图1(b)XRD分析结果显示,制备所得产物的主要成分为Ca6Al2(OH)12(SO4)3·26H2O,表明Ett已成功制备〔11,13〕,其主要特征峰中(003)、(006)、(009)为层状结构的典型晶面〔13-15〕. ...
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
Improving settleability and dewaterability of Friedel’s salt for chloride removal from saline wastewater
2
2021
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
不同金属离子层状双氢氧化物制备及表征
1
2009
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
Preparation and characterization of layered double hydroxide with different metallic ions
1
2009
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
原位合成LDH处理脱硫废水的实验研究
2
2018
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... ,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
Treatment of desulfurization wastewater by in situ synthesis of LDH
2
2018
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... ,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
Friedel’s salt,Ca2Al(OH)6(Cl,OH)·2H2O:Its solid solutions and their role in chloride binding
1
1998
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
层状双氢氧化物基吸附剂制备及性能研究
3
2015
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 由表2可知,分别投加0.15 g/L Ett和0.15 g/L Fs后,由于竞争吸附和废水pH上升导致阳离子Ca2+、Mg2+浓度有所下降.对于阴离子,SO42-质量浓度分别降低了7.2%和1.9%,Cl-质量浓度则仅降低了0.31%和0.18%.这归因于与Cl-相比,SO42-的电负性更高,溶液中的SO42-更易进入Fs层间与Cl-发生离子交换,因此,溶液中SO42-浓度下降更为显著.根据物质守恒定理,Cl-浓度由于层间离子交换理应增大,但由于LDHs层板具有大量正电荷和较大的比表面积,使其很容易通过表面吸附的方式固定溶液中的阴离子〔20,27〕,导致Cl-浓度变化不明显.综上,Ett和Fs不但对脱硫废水中的重金属具有良好的吸附效果,同时也能使同体系中共存的其他阴离子和阳离子得到一定程度的去除. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
Synthesis and properties of layered double hydroxide-based adsorbents
3
2015
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
... 由表2可知,分别投加0.15 g/L Ett和0.15 g/L Fs后,由于竞争吸附和废水pH上升导致阳离子Ca2+、Mg2+浓度有所下降.对于阴离子,SO42-质量浓度分别降低了7.2%和1.9%,Cl-质量浓度则仅降低了0.31%和0.18%.这归因于与Cl-相比,SO42-的电负性更高,溶液中的SO42-更易进入Fs层间与Cl-发生离子交换,因此,溶液中SO42-浓度下降更为显著.根据物质守恒定理,Cl-浓度由于层间离子交换理应增大,但由于LDHs层板具有大量正电荷和较大的比表面积,使其很容易通过表面吸附的方式固定溶液中的阴离子〔20,27〕,导致Cl-浓度变化不明显.综上,Ett和Fs不但对脱硫废水中的重金属具有良好的吸附效果,同时也能使同体系中共存的其他阴离子和阳离子得到一定程度的去除. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
Identification of chromate binding mechanisms in Friedel’s salt
1
2013
... 图1(c)与图1(d)所示分别为所制备Fs的SEM和XRD.图1(c)SEM显示,制备所得产物呈现出明显的片层状晶体结构,且其相互交错重叠,与文献报道的Fs形貌结构一致〔16-18〕.图1(d)XRD分析结果显示,制备所得产物主要成分为Ca2Al(OH)6Cl·2H2O,说明Fs被成功制备〔16,19〕.此外,图1(d)还显示了Fs的主要特征峰,其中晶面(003)对应的衍射峰相较于Ett峰宽较窄,峰强度较大,说明Fs结晶度更高〔20〕.另据报道,Ett和Fs表面因存在很多不规则空隙及沟壑,使其具有较大比表面积〔7,18〕,同时表面布满大量正电荷,使其在溶液中具有较好分散性能〔7,14,21〕,因此二者在吸附领域具有较大的应用潜力. ...
Removal of heavy metals from simulated wastewater by in situ formation of layered double hydroxides
1
2016
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
脱硫石膏吸附水体中重金属离子行为的研究
6
2018
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... ,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
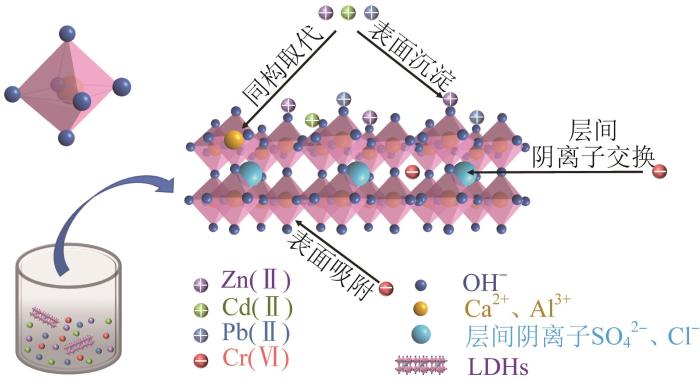
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
Adsorption behavior of heavy metal ions by desulfurization gypsum in water
6
2018
... 由图2可知,随Ett和Fs投加量的增加,各重金属离子去除率均逐渐升高,这归因于投加量的增加会使反应体系中Ett和Fs表面及内部的吸附位点增加,从而为吸附质提供更多的结合位点〔6,22〕,至投加质量浓度为0.07 g/L时,Ett和Fs对Pb(Ⅱ)的去除率均达到最高值99%,即Pb(Ⅱ)几近被完全去除,此后Ett和Fs投加量继续增加,其他3种重金属离子去除率仍有不同程度增加,直至Ett和Fs投加质量浓度为0.15 g/L时,各离子去除率均达90%以上.由此可见,LDHs对Pb(Ⅱ)具有一定的吸附选择性,对其去除效果最佳,这可能由于与另外3种重金属相比,Pb(Ⅱ)的水合半径更小,当Pb(Ⅱ)与其他离子竞争吸附位点时,因水合半径较小导致传质阻力更小,因此可被优先吸附〔15,23〕,同时,由于Ksp Pb(OH)2较小,相同pH条件下热力学因素导致Pb(Ⅱ)比Zn(Ⅱ)和Cd(Ⅱ)更容易通过生成氢氧化物沉淀而被去除〔17〕.此外,在投加质量浓度为0.02~0.10 g/L时,Ett对Cr(Ⅵ)的去除率相对较低,而Fs对Cr(Ⅵ)的去除率则高于对Zn(Ⅱ)和Cd(Ⅱ)的去除率,这说明Fs对重金属阴离子表现出较好的吸附性能. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... ,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
改性水滑石对Cr(Ⅵ)、Mn(Ⅱ)的吸附研究
6
2015
... 废水初始pH不仅影响溶质在溶液中的存在形态,而且对吸附材料或分子的表面性质也具有一定影响〔24〕.脱硫废水中弱酸性环境可能会对LDHs的吸附效果造成影响,因此,本研究在不同初始pH条件下通过Fs和Ett对模拟废水中各重金属离子的去除效果探究pH的影响,结果见图3. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... -24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
Adsroption of Cr(Ⅵ) and Mn(Ⅱ) by different modified layered double hydroxides(LDHs)
6
2015
... 废水初始pH不仅影响溶质在溶液中的存在形态,而且对吸附材料或分子的表面性质也具有一定影响〔24〕.脱硫废水中弱酸性环境可能会对LDHs的吸附效果造成影响,因此,本研究在不同初始pH条件下通过Fs和Ett对模拟废水中各重金属离子的去除效果探究pH的影响,结果见图3. ...
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... -24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
A review of the removal of anions and oxyanions of the halogen elements from aqueous solution by layered double hydroxides
3
2014
... 由图3可知,在强酸性条件(pH<1.0)下,LDHs微溶,其晶体和层状结构在一定程度上被破坏〔6,25〕,导致各重金属去除率较低(10.6%~31.2%).随着pH的上升,重金属去除率随之升高,当pH增至3.0时,各重金属去除率显著上升,最大增幅可达65.0%,但由于仍有部分活性位点在酸性条件下质子化〔6,15〕,该条件下重金属去除率依然处于较低水平.当废水初始pH进一步提升至5.0~9.0范围内,重金属去除率保持较高水平,这是因为LDHs在溶液中具有强碱性,对模拟废水中的酸度具有一定的中和作用〔6〕,按最佳投加量分别投加LDHs后,废水pH均升高到11.0以上,当废水初始pH为9.0时,2种LDHs对各重金属去除率达最大(88.1%~99.5%).继续增大溶液pH,去除率下降,这是因为对阳离子而言,初始pH过高,可能导致重金属阳离子Zn(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)快速与溶液中OH-形成配合物,从而减少LDHs对重金属的吸附作用〔23〕.与重金属阳离子相比,Cr(Ⅵ)的去除率受到强碱性条件的影响更为明显,当废水初始pH由9.0上升至12.0,其去除率降低了7%左右,这主要是因为溶液中OH-不仅在LDHs的表面与CrO42-发生竞争吸附〔7〕,同时其也抑制了CrO42-与Cl-或SO42-的层间离子交换作用〔24-25〕,从而导致Cr(Ⅵ)去除效果下降. ...
... -25〕,从而导致Cr(Ⅵ)去除效果下降. ...
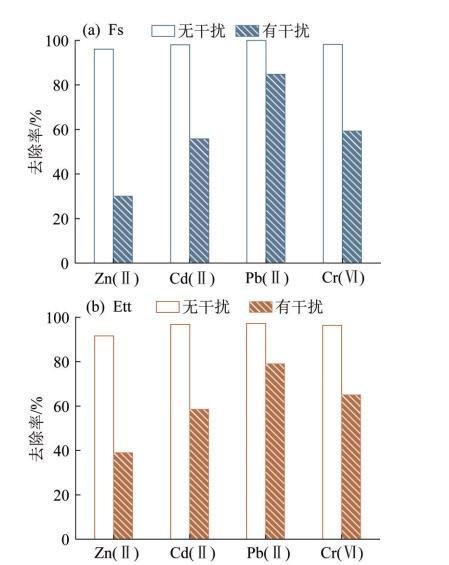
... 由表1和图4可知,共存离子的存在严重影响了Fs和Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)的去除,尤其是对于Zn(Ⅱ),当共存离子存在时,Fs和Ett对其去除率分别降低了66%和52.6%.这是因为硬度离子会与重金属阳离子形成竞争关系,大量的Ca2+和Mg2+会占据吸附材料的吸附位点,从而影响吸附材料对重金属离子的吸附,而Zn(Ⅱ)的吸附竞争性最弱,受影响较为严重.同理,SO42-和Cl-也会与CrO42-竞争吸附位点〔25〕,导致Ett和Fs对Cr(Ⅵ)的去除率分别下降了31.3%和38.9%.无干扰离子存在时,Ett和Fs对各重金属离子去除效果均满足《火电厂石灰石-石膏湿法脱硫废水水质控制指标》(DL/T 997—2020)排放标准〔26〕;存在高浓度干扰离子时,LDHs对各重金属离子去除效果有所降低,但Zn(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)仍可达标排放,Cd(Ⅱ)也可通过适当提高Fs和Ett的投加量使其满足排放要求.因此,Ett和Fs对脱硫废水中重金属的去除具有实际应用价值. ...
1
... 由表1和图4可知,共存离子的存在严重影响了Fs和Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)的去除,尤其是对于Zn(Ⅱ),当共存离子存在时,Fs和Ett对其去除率分别降低了66%和52.6%.这是因为硬度离子会与重金属阳离子形成竞争关系,大量的Ca2+和Mg2+会占据吸附材料的吸附位点,从而影响吸附材料对重金属离子的吸附,而Zn(Ⅱ)的吸附竞争性最弱,受影响较为严重.同理,SO42-和Cl-也会与CrO42-竞争吸附位点〔25〕,导致Ett和Fs对Cr(Ⅵ)的去除率分别下降了31.3%和38.9%.无干扰离子存在时,Ett和Fs对各重金属离子去除效果均满足《火电厂石灰石-石膏湿法脱硫废水水质控制指标》(DL/T 997—2020)排放标准〔26〕;存在高浓度干扰离子时,LDHs对各重金属离子去除效果有所降低,但Zn(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)仍可达标排放,Cd(Ⅱ)也可通过适当提高Fs和Ett的投加量使其满足排放要求.因此,Ett和Fs对脱硫废水中重金属的去除具有实际应用价值. ...
1
... 由表1和图4可知,共存离子的存在严重影响了Fs和Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)的去除,尤其是对于Zn(Ⅱ),当共存离子存在时,Fs和Ett对其去除率分别降低了66%和52.6%.这是因为硬度离子会与重金属阳离子形成竞争关系,大量的Ca2+和Mg2+会占据吸附材料的吸附位点,从而影响吸附材料对重金属离子的吸附,而Zn(Ⅱ)的吸附竞争性最弱,受影响较为严重.同理,SO42-和Cl-也会与CrO42-竞争吸附位点〔25〕,导致Ett和Fs对Cr(Ⅵ)的去除率分别下降了31.3%和38.9%.无干扰离子存在时,Ett和Fs对各重金属离子去除效果均满足《火电厂石灰石-石膏湿法脱硫废水水质控制指标》(DL/T 997—2020)排放标准〔26〕;存在高浓度干扰离子时,LDHs对各重金属离子去除效果有所降低,但Zn(Ⅱ)、Pb(Ⅱ)和Cr(Ⅵ)仍可达标排放,Cd(Ⅱ)也可通过适当提高Fs和Ett的投加量使其满足排放要求.因此,Ett和Fs对脱硫废水中重金属的去除具有实际应用价值. ...
Pb(Ⅱ)在层状双金属氢氧化物上的吸附规律研究
6
2008
... 由表2可知,分别投加0.15 g/L Ett和0.15 g/L Fs后,由于竞争吸附和废水pH上升导致阳离子Ca2+、Mg2+浓度有所下降.对于阴离子,SO42-质量浓度分别降低了7.2%和1.9%,Cl-质量浓度则仅降低了0.31%和0.18%.这归因于与Cl-相比,SO42-的电负性更高,溶液中的SO42-更易进入Fs层间与Cl-发生离子交换,因此,溶液中SO42-浓度下降更为显著.根据物质守恒定理,Cl-浓度由于层间离子交换理应增大,但由于LDHs层板具有大量正电荷和较大的比表面积,使其很容易通过表面吸附的方式固定溶液中的阴离子〔20,27〕,导致Cl-浓度变化不明显.综上,Ett和Fs不但对脱硫废水中的重金属具有良好的吸附效果,同时也能使同体系中共存的其他阴离子和阳离子得到一定程度的去除. ...
... 图5(a)为Ett对重金属离子的吸附动力学曲线,由图5(a)可知,反应过程分为快速吸附和慢速吸附2个阶段.由于重金属阳离子与Ett表面OH-键合速度较快〔27〕,使得动力学反应过程迅速且短时间内达到吸附平衡,在反应时间为1.0 min时,Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)的吸附速率分别为46.1、35.7、47.5 mg/(g·min),Ett对三者的吸附量均可达到对其最大吸附容量的86%以上.随着吸附时间的延长,Ett对3种阳离子的吸附量逐渐趋于平缓,并在反应时间为20 min左右达到吸附平衡,平衡吸附容量分别为47.5、40.0、49.3 mg/g.相同条件下,Pb(Ⅱ)、Cd(Ⅱ)和Zn(Ⅱ)的最大吸附容量有所差异,可能与其竞争性吸附有关〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
... 〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
Studies on the sorption of Pb(Ⅱ) on layered double hydroxides
6
2008
... 由表2可知,分别投加0.15 g/L Ett和0.15 g/L Fs后,由于竞争吸附和废水pH上升导致阳离子Ca2+、Mg2+浓度有所下降.对于阴离子,SO42-质量浓度分别降低了7.2%和1.9%,Cl-质量浓度则仅降低了0.31%和0.18%.这归因于与Cl-相比,SO42-的电负性更高,溶液中的SO42-更易进入Fs层间与Cl-发生离子交换,因此,溶液中SO42-浓度下降更为显著.根据物质守恒定理,Cl-浓度由于层间离子交换理应增大,但由于LDHs层板具有大量正电荷和较大的比表面积,使其很容易通过表面吸附的方式固定溶液中的阴离子〔20,27〕,导致Cl-浓度变化不明显.综上,Ett和Fs不但对脱硫废水中的重金属具有良好的吸附效果,同时也能使同体系中共存的其他阴离子和阳离子得到一定程度的去除. ...
... 图5(a)为Ett对重金属离子的吸附动力学曲线,由图5(a)可知,反应过程分为快速吸附和慢速吸附2个阶段.由于重金属阳离子与Ett表面OH-键合速度较快〔27〕,使得动力学反应过程迅速且短时间内达到吸附平衡,在反应时间为1.0 min时,Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)的吸附速率分别为46.1、35.7、47.5 mg/(g·min),Ett对三者的吸附量均可达到对其最大吸附容量的86%以上.随着吸附时间的延长,Ett对3种阳离子的吸附量逐渐趋于平缓,并在反应时间为20 min左右达到吸附平衡,平衡吸附容量分别为47.5、40.0、49.3 mg/g.相同条件下,Pb(Ⅱ)、Cd(Ⅱ)和Zn(Ⅱ)的最大吸附容量有所差异,可能与其竞争性吸附有关〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
... 〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
... 如图6所示,LDHs具有疏松多孔的层状结构,这是其具有良好的重金属离子吸附性能的关键.对于Ett和Fs,除该结构外二者还具有较强的碱性〔24〕,能够使溶液中的重金属阳离子形成氢氧化物沉淀并附着在吸附剂表面〔27〕.此外,双金属氢氧化物由八面体结构的晶格单元构成,八面体的中心是1个金属离子,6个顶点分别由OH-占据,八面体通过共享边界形成单元层〔23〕.由于其独特的分子结构,在双金属氢氧化物的层板上,八面体晶格中的阳离子可被半径接近的其他金属阳离子所取代〔23〕,层间的阴离子也可以与溶液中阴离子交换.因此,除表面沉淀外,Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)还可与LDHs层板晶格中的Ca2+发生同构取代,并同时通过提高废水pH将析出的Ca2+迅速沉淀为Ca(OH)2. ...
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...
Kinetics of sorptive removal of chromium(Ⅵ) from aqueous solutions by calcined Mg-Al-CO3 hydrotalcite
2
2003
... 图5(a)为Ett对重金属离子的吸附动力学曲线,由图5(a)可知,反应过程分为快速吸附和慢速吸附2个阶段.由于重金属阳离子与Ett表面OH-键合速度较快〔27〕,使得动力学反应过程迅速且短时间内达到吸附平衡,在反应时间为1.0 min时,Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)的吸附速率分别为46.1、35.7、47.5 mg/(g·min),Ett对三者的吸附量均可达到对其最大吸附容量的86%以上.随着吸附时间的延长,Ett对3种阳离子的吸附量逐渐趋于平缓,并在反应时间为20 min左右达到吸附平衡,平衡吸附容量分别为47.5、40.0、49.3 mg/g.相同条件下,Pb(Ⅱ)、Cd(Ⅱ)和Zn(Ⅱ)的最大吸附容量有所差异,可能与其竞争性吸附有关〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
... 图5(b)所示为准一级动力学模型对快速吸附过程的拟合曲线,如表3所示,其R2均高于0.9.图5(c)所示为准二级动力学模型对整个吸附过程的拟合曲线,其R2相较于准一级动力学拟合的R2更高,拟合得出的qe与实际值吻合度也较高,因此,Ett对各重金属的吸附量随时间变化遵循准二级动力学规律〔23-24〕.准二级动力学包含了包括液膜扩散、表面吸附、内部扩散、化学吸附在内所有的吸附过程,说明Ett对重金属的高效去除是在多种机制协同作用下实现的〔14,23-24〕.图5(d)所示为颗粒内扩散模型对快速吸附阶段的拟合曲线.材料的吸附过程通常分为吸附剂表面吸附和孔道缓慢扩散2个过程〔6〕,对于Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ) 3种重金属阳离子的吸附来讲,其颗粒内扩散模型拟合R2均低于0.25,说明颗粒内扩散并不是控制吸附过程的主要步骤,表面吸附在Ett去除重金属阳离子过程中占主导地位;对于Cr(Ⅵ)而言,颗粒内扩散R2相对较高(R2=0.673 5),且与另外3种重金属阳离子相比,准一级动力学计算出的Cr(Ⅵ)平衡吸附容量更接近实际平衡容量,由此可知,在前20 min快速吸附阶段,Ett对Cr(Ⅵ)的吸附主要发生在吸附剂表面,随着吸附速率逐渐减缓,阴离子态Cr(Ⅵ)进入层间与Cl-和SO42-发生离子交换,使吸附容量得到进一步提升〔27-28〕.因此,物理吸附和内扩散是Cr(Ⅵ)去除的重要机理. ...
Calcined graphene/MgAl-layered double hydroxides for enhanced Cr(Ⅵ) removal
0
2013
Selective removal of heavy metals by hydrotalcites as adsorbents in diverse wastewater:Different intercalated anions with different mechanisms
0
2019
Adsorption mechanisms of chromate and phosphate on hydrotalcite:A combination of macroscopic and spectroscopic studies
1
2019
... 图5(a)为Ett对重金属离子的吸附动力学曲线,由图5(a)可知,反应过程分为快速吸附和慢速吸附2个阶段.由于重金属阳离子与Ett表面OH-键合速度较快〔27〕,使得动力学反应过程迅速且短时间内达到吸附平衡,在反应时间为1.0 min时,Ett对Zn(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)的吸附速率分别为46.1、35.7、47.5 mg/(g·min),Ett对三者的吸附量均可达到对其最大吸附容量的86%以上.随着吸附时间的延长,Ett对3种阳离子的吸附量逐渐趋于平缓,并在反应时间为20 min左右达到吸附平衡,平衡吸附容量分别为47.5、40.0、49.3 mg/g.相同条件下,Pb(Ⅱ)、Cd(Ⅱ)和Zn(Ⅱ)的最大吸附容量有所差异,可能与其竞争性吸附有关〔27〕.由图5(a)还可知,Ett对Cr(Ⅵ)的吸附速率相对较慢,反应时间为1 min时吸附速率仅为7.4 mg/(g·min),反应90.0 min后,趋于吸附平衡,最大吸附容量为38.8 mg/g.这可能是由于LDHs层板上的正电荷对阴离子的静电吸附作用较弱,且与阳离子表面沉淀过程相比,层间阴离子交换过程较慢所致〔28-31〕. ...
Characteristics of a novel adsorbent Fe-Mg-type hydrotalcite and its adsorption capability of As(Ⅲ) and Cr(Ⅵ) from aqueous solution
1
2018
... 此外,LDHs是一类带有结构正电荷和较大表面积的物质,因此对阴离子具有一定的吸附能力〔20,27〕,同时LDHs因其层状结构而具有较大的阴离子交换容量,使阴离子态重金属Cr(Ⅵ)通过外表面静电吸附和层间离子交换被高效去除〔24,32〕. ...





 津公网安备 12010602120337号
津公网安备 12010602120337号